Chimica dei Lipidi: struttura e metabolismo degli acidi grassi
Documento da Università su Chimica dei Lipidi. Il Pdf, un approfondimento di Chimica per l'Università, esplora la struttura e le proprietà degli acidi grassi, il processo di beta-ossidazione e le rese energetiche, arricchito da tabelle e diagrammi esplicativi.
Mostra di più20 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
CHIMICA DEI LIPIDI
Passiamo ora a parlare della chimica e del metabolismo lipidico: si tratta di un gruppo di composti molto variegato, con in comune la caratteristica di essere insolubili. Nonostante quando parliamo di lipidi subito vengano alla mente trigliceridi e catene alifatiche di acidi grassi, queste sono solo una delle famiglie che compongono la classe di macromolecole; sono infatti molecole di riserva, ma abbiamo anche i fosfolipidi e gli steroli, componenti di membrane, lipidi che svolgono ruoli di ormoni e cofattori enzimatici, chaperon molecolari, trasportatori di elettroni, e così via. Vediamo allora le caratteristiche delle classi più rilevanti e le loro funzioni, a partire ovviamente dai lipidi di riserva.
Acidi Grassi: Struttura e Proprietà
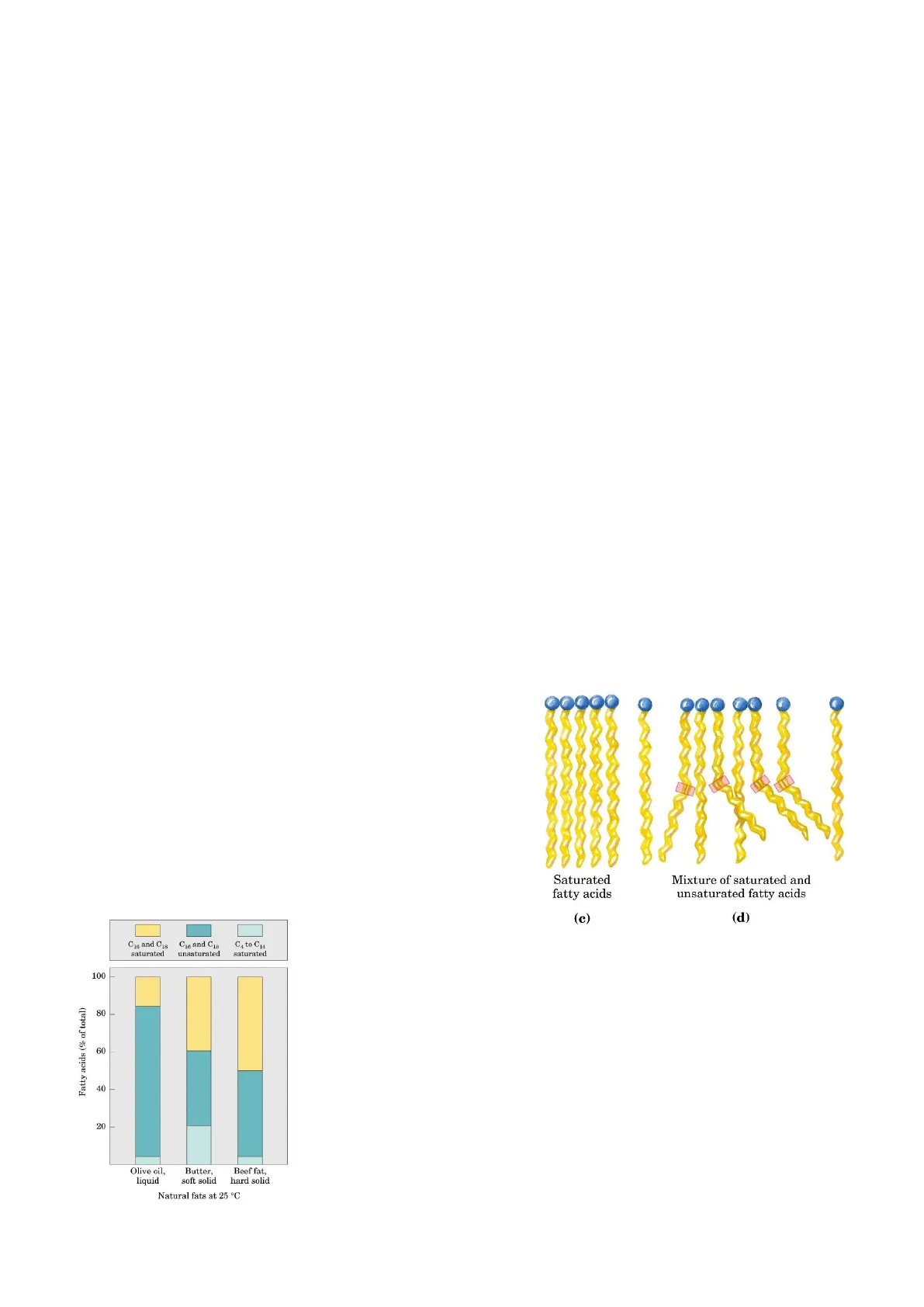
Quasi tutti i lipidi di riserva sono derivati degli acidi grassi, ossia lunghe catene alifatiche analoghe agli idrocarburi e praticamente completamente ridotte, legate ad un gruppo carbossilico terminale che gli fornisce la proprietà acida. La loro lunghezza può variare ampiamente, dai 4 ai 36 atomi di carbonio, e possono essere completamente saturi oppure contenere uno o più doppi legami in uno stato insaturo e ramificato; per definirli si indica il numero di atomi di carbonio che contengono e il numero di doppi legami, separati con due punti. Quindi per esempio l'acido palmitico (molti hanno nomi comuni derivati dalle piante da cui sono stati estratti) viene indicato con 16:0, mentre l'oleico 18:1; se sono presenti più doppi legami la loro posizione va indicata all'apice del simbolo delta, quindi per esempio 20:2 (49,12). Oltre a questa rappresentazione semplificata si può indicare nome dell'acido grasso con il numero di carboni + -oico, quindi tetra-ecosanico se ha 24C, dodecadenoico se ne ha 12, ed esso a sua volta è preceduta dall'indicazione della forma cis o trans del doppio legame e dalle posizioni. Gli acidi grassi più comuni hanno catene tra i 12 e 24 atomi di carbonio e non sono ramificati, mentre se presentano doppi legami i più frequenti sono tra i C9 e C10 o tra 12 e 15 in caso di polinsaturi; inoltre i doppi legami non si trovano quasi mai in modo coniugato, quindi alternati a singoli, ma sono sempre separati da uno o più gruppi metilici. Esso infine sono quasi sempre doppi legami di tipo cis, per cui i sostituenti si trovano dalla stessa parte causando dei ripiegamenti nella catena; questo fattore è responsabile dello stato liquido degli acidi grassi insaturi a temperatura ambiente. Il punto di fusione (e quindi lo stato fisico) degli acidi grassi è infatti fortemente influenzato da lunghezza e saturazione della catena: i saturi riescono a compattarsi in modo molto saldo tra loro, formando molte interazioni e rimanendo solidi e a temperature di fusione più alte, mentre la presenza di ramificazioni influisce sulla possibilità di un impacchettamento così stretto. Quindi gli acidi grassi insaturi hanno temperature di fusione più basse (temperatura necessaria per il cambio di stato) e sono spesso liquidi; i doppi legami multipli fanno abbassare ancora di più il limite di fusione fino a temperature negative. La lunghezza e saturazione influiscono poi anche su altre proprietà fisiche, come la solubilità; grazie al gruppo carbossilico alcuni acidi grassi a catena corta sono debolmente solubili in acqua, ma appena la catena inizia ad allungarsi questa solubilità diventa pressoché inesistente. Lo stesso per catene molto lunghe avviene anche in solventi apolari, ma rimane comunque una solubilità consistente. Per esempio l'olio di oliva, liquido a temperatura ambiente, è prevalentemente formato da acidi grassi insaturi, con meno del 20% saturi e di questi anche alcuni a catena corta. Il burro invece, un solido morbido, ha molti più acidi grassi saturi e soprattutto a catena più lunga, anche se i numerosi a catena corta e qualche insaturo lo rendono comunque malleabile, mentre il grasso animale che è ancora più solido ha più della metà acidi grassi saturi a catena lunga.
Acidi Grassi Trans e Salute
Quasi mai in natura i doppi legami negli acidi grassi sono in forma trans; tuttavia ciò può avvenire durante la cottura di grassi e oli, o con il processo di idrogenazione che li permette di resistere più a lungo in condizioni di esposizione all'ossigeno, che altrimenti li ossiderebbe. Tuttavia gli acidi grassi trans sono molto dannosi, in quanto aumentano il livello nel sangue di trigliceridi e colesterolo delle LDL (cattivo) causando l'insorgenza di malattie coronariche con maggiore frequenza.
Tabella 11-1: Acidi Grassi Naturali
table 11-1 Some Naturally Occurring Fatty Acids Solubility at 30 ℃ (mg/g solvent) Carbon skeleton Structure* Systematic name™ Common name (derivation) Melting point (C) Water Benzene 12:0 CH3(CH2) 10COOH n-Dodecanoic acid Lauric acid 44.2 0.063 2,600 14:0 CH3(CH2) 12COOH n-Tetradecanoic acid Myristic acid 53.9 0.024 874 16:0 CH3(CH2) 14COOH n-Hexadecanoic acid Palmitic acid 63.1 0.0083 348 18:0 CH3(CH2) 16COOH n-Octadecanoic acid Stearic acid 69.6 0.0034 124 "hard fat") 20:0 CH3(CH2) 18COOH n-Eicosanoic acid Arachidic acid 76.5 (Latin Arachis, legume genus) 24:0 CH3(CH2) 22COOH n-Tetracosanoic acid Lignoceric acid 86.0 (Latin lignum, "wood" + cera, "wax") 16:1(49) CH3(CH2)5CH=CH(CH2)7COOH cis-9-Hexadecenoic acid Palmitoleic acid -0.5 18:1(49) CH3(CH2)7CH=CH(CH2),COOH cis-9-Octadecenoic acid Oleic acid 13.4 (Latin oleum, "oil") 18:2 CH3(CH2)4CH=CHCH2CH= CH(CH2)7COOH cis-, cis-9,12-Octadecadienoic acid Linoleic acid -5 18:3(49,12,15) CH3CH2CH=CHCH2CH= cis-,cis-,cis-9,12,15- Octadecatrienoic acid @-Linolenic acid -11 20:4(45,8,11,14) CH3(CH2)4CH=CHCH2CH= CHCH2CH=CHCH2CH= CH(CH2)3COOH cis-,cis-,cis-,cis-5,8,11,14- Icosatetraenoic acid Arachidonic acid -49.5 *All acids are shown in their nonionized form. At pH 7, all free fatty acids have an ionized carboxylate. Note that numbering of carbon atoms begins at the carboxyl carbon. "The prefix n- indicates the "normal" unbranched structure. For instance, "dodecanoic" simply indicates 12 carbon atoms, which could be arranged in a variety of branched forms; "n-dodecanoic" specifies the linear, unbranched form. For unsaturated fatty acids, the configuration of each double bond is indicated; in biological fatty acids the configuration is almost always cis.
Triacilgliceroli: Riserva Energetica
Andando ora a parlare di strutture più complesse, gli acidi grassi si organizzano in triacilgliceroli, ossia composti di tre acidi grassi esterificati con i gruppi OH del glicerolo; in natura sono per la maggior parte misti, con diversi tipi di acidi grassi che compongono il trio. Dato che sia il gruppo COOH che l'OH del glicerolo sono uniti nella reazione, queste molecole sono completamente apolari, e fungono da riserva energetica nelle cellule e in alcuni organismi nello strato sottocutaneo anche da isolamento termico. Essi si accumulano infatti in forma di gocce oleose all'interno del citosol acquoso, soprattutto nelle cellule specializzate degli adipociti in cui possono formare anche l'80% della massa cellulare; possono poi essere liberati e diffusi nel sangue o in altri tessuti grazie a proteine lipasi, che ne catalizzano l'idrolisi liberando acidi grassi. Sono particolarmente utili come elementi di riserva in quanto un acido grasso è più ridotto di un glucosio o una proteina, e quindi può liberare con la sua ossidazione completa quasi il doppio dell'energia; inoltre non essendo idratati in quanto idrofobici non causano problemi osmotici alla cellula, anche se necessitano di più tempo per essere mobilizzati e non sono quindi una fonte immediata di energia come i polisaccaridi.
Cere: Protezione e Idratazione
Un altro composto formato da acidi grassi a catena lunga esterificati con alcoli a catena lunga sono le cere, più solide e con punti di fusione più alti rispetto ai triacilgliceroli; esse hanno proprietà idrorepellenti che le rendono adatte a proteggere e idratare pelle e peli, oltre che proteggere molte piante dai parassiti.
Lipidi di Membrana: Classificazione e Funzioni
Passiamo quindi alla prossima classe, i lipidi di membrana, che sono tra loro molto più variegati e si distribuiscono a formare un doppio strato con le teste polari rivolte all'esterno e le code apolari isolate all'interno; non hanno poi solo funzioni strutturali ma ricoprono anche molti altri ruoli. Li possiamo classificare in:
- Fosfolipidi - o glicerofosfolipidi, sono formati da due acidi grassi, di cui solitamente uno insaturo, legati a due OH del glicerolo, mentre il terzo è occupato da un gruppo fosfato legato a sua volta a un gruppo X, che formano la testa polare. Ci potrebbero essere in questa posizione molecole di fosfatidilcolina, fosfatidiletanolammina, fosfatidilserina, fosfatidilinositolo, o anche fosfatidilglicerolo come avviene nella cardiolipina, un secondo messaggero che vedremo in futuro. Possono essere fosfolipidi anche gli sfingolipidi, che invece di possedere un glicerolo hanno una molecola di sfingosina, con amminoalcol con una catena alifatica lunga già presente, che può legare un acido grasso ed una testa polare; la struttura base, solo con l'acido grasso legato, è nota come cerammide. Se al cerammide è poi unita una testa polare di fosfocolina o fosfoetanolammina abbiamo allora una sfingomielina, abbondante nella membrana cellulare e soprattutto nella mielina dei neuroni; questo è appunto un fosfolipide. Tuttavia la testa polare potrebbe essere anche uno zucchero; passiamo qui ai glicolipidi (vedi dopo).
Glicerofosfolipidi: Nomi e Carica Netta
Name of glycerophospholipid Name of X Formula of X Net charge (at pH 7) Phosphatidic acid - H -1 Phosphatidylethanolamine Ethanolamine CH2-CH2-NH3 0 Phosphatidylcholine Choline CH2-CH2-N(CH3)3 0 Phosphatidylserine Serine - CH2-CH-NH3 -1 COO Phosphatidylglycerol Glycerol CH2-CH-CH2-OH -1 OH H 0-P 6 5 Phosphatidylinositol 4,5-bisphosphate myo-Inositol 4,5- bisphosphate OH H H -4 1 OH HO 0-P 2 3 H H Cardiolipin Phosphatidyl- glycerol CH -2 CHOH O CH2-0-P-O-CH2 O CH-O-C-R1 O CH2-0-C-R2
Lipid-Eteri nei Glicerofosfolipidi
Tra i glicerofosfolipidi troviamo anche lipid-eteri, in cui una delle catene aciliche è legata al glicerolo con un legame etere invece di estereo; questo accade per esempio nei plasmogeni del tessuto cardiaco.
- Glicolipidi - sono degli sfingolipidi appunto, in cui la testa polare è rappresentata da uno zucchero legato al gruppo OH della sfingosina; si può trattare di un monosaccaride come nei cerebrosidi, o di oligosaccaridi più complessi come i gangliosidi e i globosidi, con due o più zuccheri spesso di glucosio, galattosio e N-acetil-glicosammina. Spesso essi hanno funzioni di riconoscimento nelle membrane biologiche, e sono significanti nella determinazione del gruppo sanguigno umano: una struttura oligosaccaridica base è legata ad una sfingosina e ad un acido grasso, formando il gruppo 0. Con l'addizione di una N-acetil-glucosammina si ha il gruppo A, mentre con un galattosio il gruppo B; ci sono quindi dei geni specifici per codificare l'enzima necessario a questa addizione extra, e chi non li possiede e non manifesta una determinata modifica la percepisce come "estranea" ed attacca i globuli rossi differenti; per questo è così importante il gruppo sanguigno nelle trasfusioni.