Metastasi: meccanismi di diffusione delle cellule tumorali
Documento di Biologia sulle metastasi. Il Pdf esplora il fenomeno delle metastasi, focalizzandosi sui meccanismi di diffusione delle cellule tumorali e sui fattori che ne influenzano la capacità metastatica. Il Pdf descrive le diverse vie di disseminazione, come quella ematica, linfatica e transcelomatica, e la specificità d'organo delle metastasi.
Mostra di più21 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
METASTASI
Prof. Maier| Lezione n.34 | data 31/10/2023 | Pausa pag.10 METASTASI
Abbiamo visto nella lezione precedente quali sono i meccanismi che portano una cellula a divenire invasiva. Però, essere invasiva non basta a dare metastasi. Ora vedremo quali sono le caratteristiche che deve avere la cellula per diventare metastatica.
Innanzitutto, si definisce metastasi la propagazione a distanza di un processo patologico. Infatti, il termine deriva dal greco e significa "spostamento". Oggi noi associamo subito questo termine alle neoplasie maligne, ma che i tumori maligni fossero capaci di avere manifestazioni a distanza lo avevano già osservato gli antichi. Le prime descrizioni risalgono al Settecento, ma il New England Journal of Medicine ci dice che la prima pubblicazione scientifica che utilizza il termine metastasi in contesto oncologico è del 1911. Molto di ciò che sappiamo oggi sui meccanismi molecolari alla base delle metastasi è stato studiato tramite il modello del "nude mouse", un topo atipico.
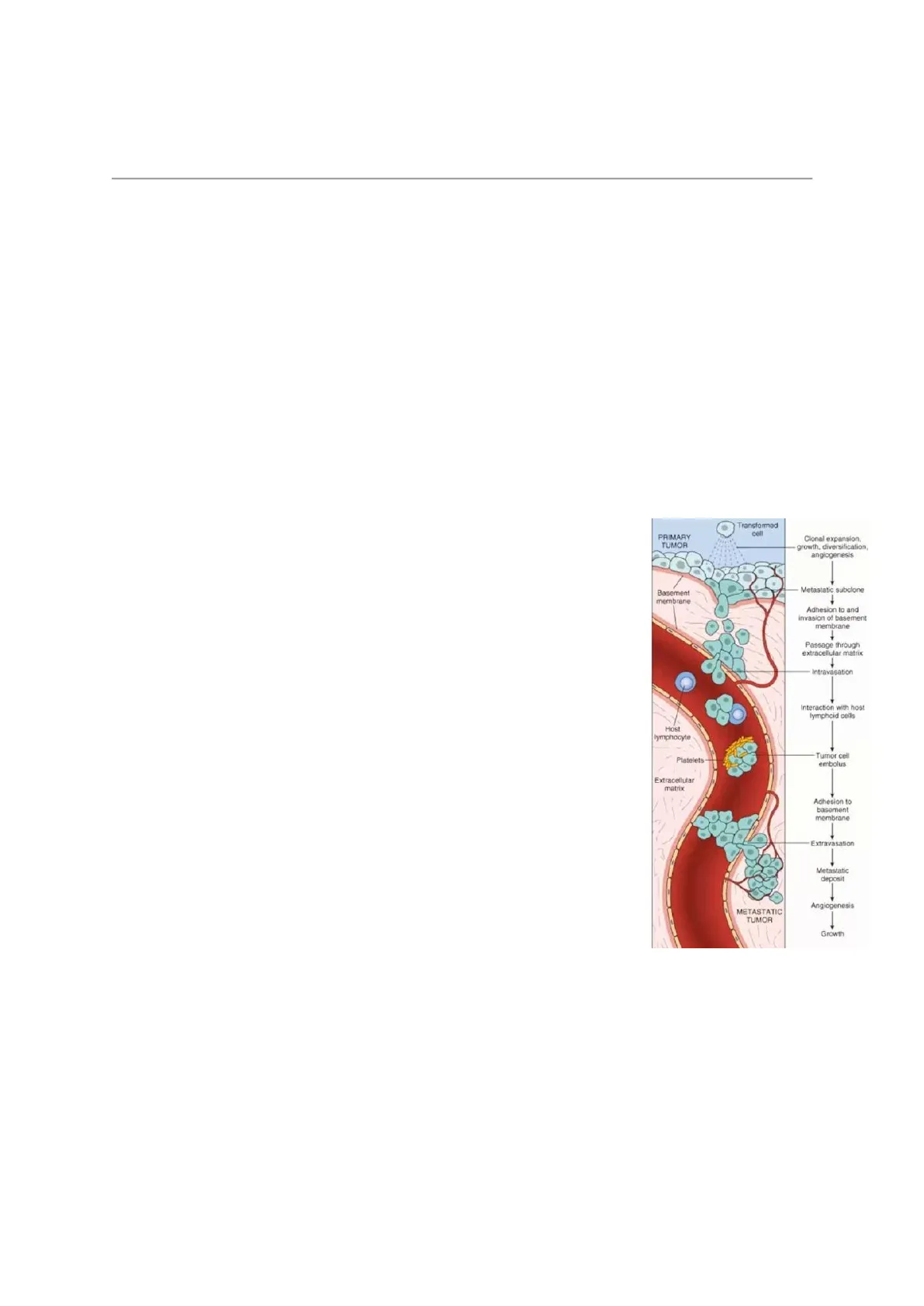
Questa immagine ci descrive il lungo e difficile viaggio che una cellula neoplastica maligna con capacità metastatica deve affrontare. La cellula, o piccolo gruppo di cellule, acquisisce un potenziale che le permette di entrare - ad esempio, ma non solo - nel torrente ematico. Il primo step, quindi, è l'intravasazione. Dopodiché, a un certo punto del suo viaggio si arresta in prossimità di un determinato distretto corporeo per compiere il percorso inverso, ovvero l'extravasazione. Nel determinato tessuto la cellula potra dare origine a una popolazione figlia, che lì potrà sopravvivere e accrescere oppure morire.
Il processo metastatico è un processo inefficiente. Circa l'1% delle cellule di una neoplasia maligna è capace di spostarsi, di invadere e colonizzare un tessuto. Bisogna però considerare che la massa più piccola rilevabile è costituita da 1 miliardo di cellule, per cui il suo 1% sarà comunque un numero importante. In ogni caso, una volta che si staccano dalla neoplasia primaria ed entrano nel circolo ematico si trovano ad essere sottoposte a un ambiente stressante: pressione arteriosa, shear stress (stress da sfregamento, attrito), calibro vasale, cellule dell'immunità circolanti rappresentano tutti un pericolo per la sopravvivenza di queste cellule. Di tutte le cellule maligne metastatiche che arrivano in periferia, molte si attaccano alle cellule endoteliali, ma poche sopravvivono in quanto l'endotelio, al quale si attaccano, rilascia fattori quali NO, tossico in grandi quantità per le prime. Inoltre, una volta che una cellula tumorale si è fermata in un determinato distretto può essere più facilmente attaccata dalle cellule del sistema immune. Tutto ciò per dire che si tratta di un processo inefficiente, cosa che però appare un controsenso dal momento che 1/3 dei pazienti in cui si evidenzia un tumore maligno ha già metastasi evidenti.
Transformed cell PRIMARY TUMOR Cional expansion. growth, diversification, angiogenesis 1 Metastatic subclone Basement membrane 1 Adhesion to and invasion of basement membrane 1 Passage through extracellular matrix 1 Intravasation Interaction with host lymphoid cells Host lymphocyte Platelets Extracellular matrix Tumor cell embolus 1 Adhesion to basement membrane Extravasation Metastatic deposit 1 Angiogenesis 1 Growth
Fattori che regolano la crescita e la metastatizzazione
I fattori che regolano la crescita e la metastatizzazione sono tanti: Pag. 1 di 21- Cinetica della crescita cellulare - Angiogenesi e linfangiogenesi - Progressione tumorale e grado di eterogeneità (se sono presenti diversi tipi cellulari all'interno della massa neoplastica).
Correlazione tra dimensione della neoplasia e rischio di metastasi
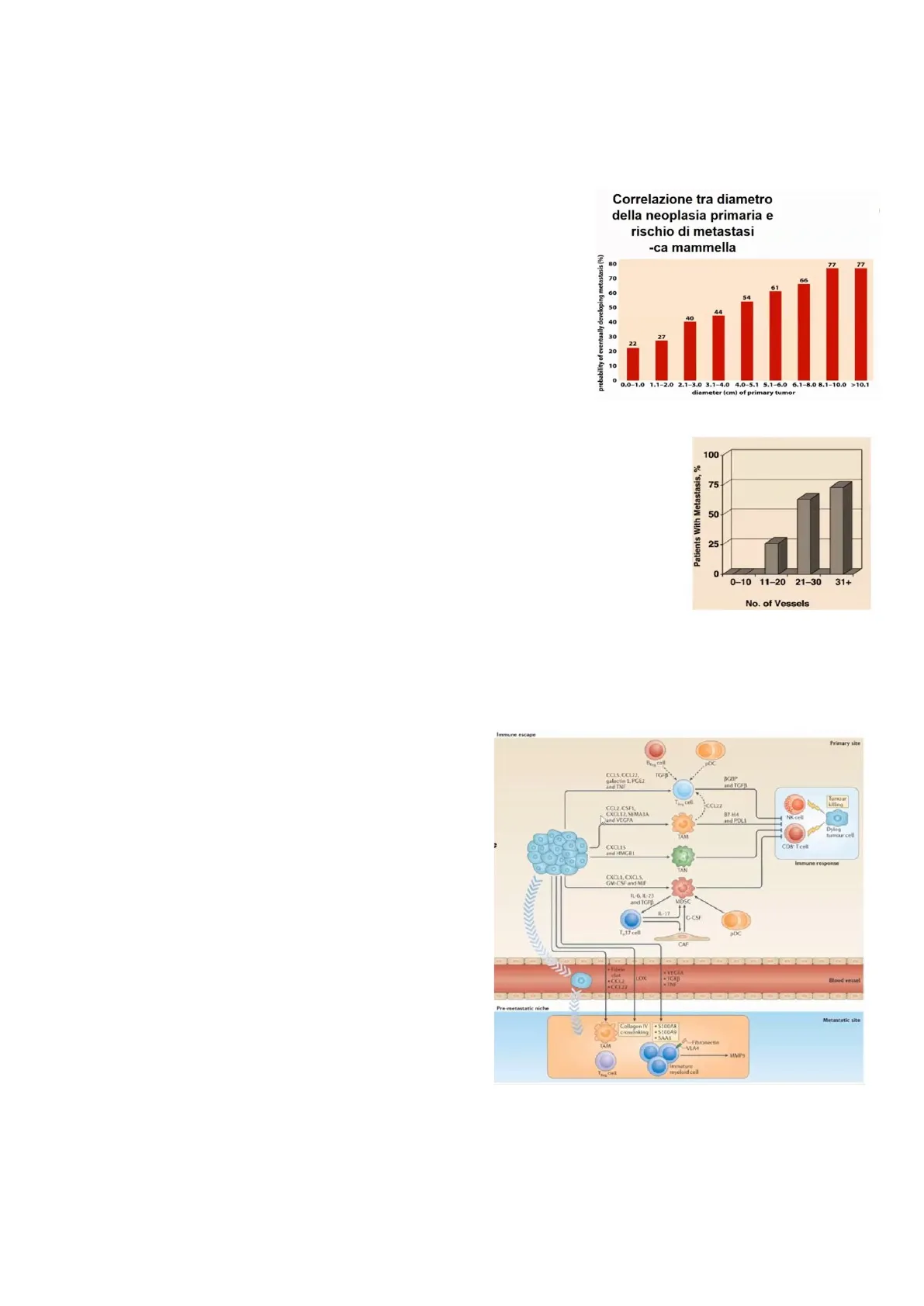
Vi è poi anche una correlazione con la dimensione della neoplasia. Qui viene riportato un grafico che mostra come esiste una correlazione diretta tra il diametro della neoplasia primaria - in questo caso carcinoma della mammella - e il rischio di metastasi. Per cui il 22% delle donne che hanno un carcinoma relativamente piccolo, meno di 1 cm di diametro, hanno alte probabilità di avere metastasi già presenti o future.
probability of eventually developing metastasis (%) 77 77 66 61 54 A4 40 30 27 20 10 0.0-1.0 1.1-2.0 2.1-3.0 3.1-4.0 4.0-5.1 5.1-6.0 6.1-8.0 8.1-10.0 >10.1 diameter (cm) of primary tumor
Correlazione tra angiogenesi e rischio di metastasi
Allo stesso modo c'è una correlazione tra angiogenesi nella neoplasia primaria e rischio di metastasi. In questo caso vengono riportati dei dati ottenuti da uno studio riguardante il carcinoma del colon. Più vasi ci sono, più è alta la probabilità 100 di metastatizzazione, perché i vasi neoformati non essendo completamente 75 maturi sono molto più facili da invadere, e in alcuni casi non presentano 50 nemmeno il rivestimento endoteliale, consentendo alla cellula neoplastica il diretto contatto con il sangue. 25
Inoltre, più una cellula è capace di crescere, ovvero più riacquisisce delle caratteristiche staminali, più è invasiva, e dunque capace di formare metastasi.
Patients With Metastasis, % 0 0-10 11-20 21-30 31+ No. of Vessels
STEP DELLA METASTATIZZAZIONE
1. Preparazione
Il primo momento del processo di metastatizzazione è quello in cui la cellula (o gruppo di cellule, dipende dal tipo di tumore e la modalità di migrazione) invasiva e metastatica arriva nelle prossimità del vaso. È sicuramente importante nel guidare la metastatizzazione come è fatta la matrice del tessuto che ospita la neoplasia: una matrice extracellulare densa favorisce la formazione di gruppi di cellule che poi si spostano verso la parete dei capillari.
Ma le cellule metastatiche, già prima del processo di intravasazione, si preparano. Infatti rilasciano chemochine e citochine in modo tale da reclutare:
Immune escape Primary site Diag cell CCLS. CCL22. galectin 1, POEZ and INF BGBP and TGFB T ... cell CCL22 CCL2.CSFI. CXCLIZ, SEMAJA und VEGFA B7-H4 and POLI NK cel 0 Dying TAM tumour cell CXCLIS CDB' T cell and HMC81 Immune response TAN CXCLL. CXCLS. GM-CSF and MIE IL-6, IL-73 and TGFB MDSC G-CSF T_17 cell PDC O CAF . VEGEN . TGIB - TNF Mood vessel - CCLZI Pre-metastatic niche Collagen IV crosslinking . S10048 . 510049 . SAAI Fibronectin TAM -VLA4 · MMP9 Immature nyeloid cell Tang cell
Correlazione tra diametro della neoplasia primaria e rischio di metastasi -ca mammella 80 TGFØ ** Tumour ling- Metastatic site LOX · CCL2
- Macrofagi: diventeranno in quel microambiente specifico macrofagi associati alla neoplasia con fenotipo M2, ovvero che promuovono la proliferazione e l'angiogenesi. Prendono il nome di TAM (tumor associated macrophages). Pag. 2 di 21
- Neutrofili: saranno anche loro associati al tumore, quindi sempre con funzione di supporto alla crescita e all'inibizione del sistema immune. Prendono il nome di TAN (tumor associated neutrophils).
- Precursori mieloidi
- Linfociti Treg
Tutte queste cellule cooperano, provocando un'inibizione sull'attività delle cellule NK e dei linfociti CD8+. Si tratta quindi di un sistema per tenere sotto controllo negativo il sistema immune. Questa fase preparatoria è necessaria dunque per sfuggire al controllo immunitario. In più le cellule del tumore primario rilasciano fattori angiogenici e linfangiogenici, preparando una rete vascolare e linfatica matura e pertanto più facile da superare in quanto più permeabile. Infine vengono rilasciate anche proteasi che rimodellano la matrice extracellulare.
Questi sono i meccanismi tramite cui una cellula metastatica può raggiungere nel torrente circolatorio ed eventualmente dare metastasi. È quindi il tumore primario a condizionare i tessuti a distanza, in maniera tale che diventino favorevoli all'impianto e si possa creare una nicchia premetastatica.
2. Intravasazione e sopravvivenza nel sangue
La cellula neoplastica quindi, a seguito di tutto il processo di condizionamento e preparazione da parte del tumore primario, si sposta, arriva in prossimità di un vaso, qui rilascia proteasi per poter superare la membrana basale e facendosi spazio tra una cellula endoteliale e l'altra giunge all'interno dell'albero circolatorio.
Generalmente la migrazione di una singola cellula è tipica di leucemie e sarcomi, mentre le cellule che originano da carcinomi e adenocarcinomaendono a migrare in gruppi, in veri e propri aggregati di cellule neoplastiche.
Tumour cell Cohesion Platelet microparticles · Growth factors · Chemokines Activated platelet · Proteases Coagulation Leukocyte Tissue factor and FVIla activate thrombin
Questi aggregati si formano anche per sopravvivere meglio all'ambiente ostile rappresentato dal sangue. Questo perché, come abbiamo detto prima, il flusso sanguigno all'interno dei vasi crea il cosiddetto "shear stress", ovvero l'attrito da sfregamento, che rappresenta una fonte di stress per la cellula metastatica non abituata a sollecitazioni meccaniche di questo genere. Questa deve anche far fronte alla pressione idrostatica vasale, decisamente maggiore di quella dell'interstizio in cui si trovava. La sopravvivenza di queste cellule inadatte a sostenere stimoli meccanici viene quindi resa possibile dalla presenza nel circolo sanguigno di sostanze anioniche, quali i polifosfati, che attivano il fattore XII della coagulazione. Questo, a sua volta, attiva una cascata enzimatica che termina con la sintesi di fibrina, la quale precipita e stabilizza l'embolo neoplastico, oltre che permettergli di sfuggire al controllo del sistema immune. Pag. 3 di 21Gli emboli neoplastici sono dovuti all'instaurarsi di interazioni omotipiche o eterotipiche. La possibilità di viaggiare in gruppo è un meccanismo che facilita la sopravvivenza.
Abbiamo diverse possibilità:
- Il gruppo di cellule neoplastiche arriva in prossimità di un vaso che è molto permeabile e pertanto fa poca fatica ad entrare in circolo.
- Il gruppo emette pseudopodi e intravasano facendosi spazio tra le cellule endoteliali.
- Il gruppo passa tramite l'aiuto di macrofagi, in quando grandi elaboratori di proteasi che agiscono sulle cellule endoteliali.
Quelle che sopravvivono all'ambiente ostile del sangue possono arrivare in vasi di calibro più piccolo, interagire con il tessuto endoteliale, extravasare e invadere altri tessuti. Questo è possibile sia per gli emboli omotipici sia per quelli eterotipici che sono stati rivestiti da piastrine. Anzi, gli emboli rivestiti da piastrine hanno notevoli vantaggi, in quanto le piastrine contengono fattori di sopravvivenza e di crescita, oltre che a ripararlo in modo da sfuggire al controllo del sistema immune.
A questo punto questi gruppi di cellule possono extravasare: nel determinato tessuto possono morire, formare metastasi dormienti o crescere e dare luogo a una popolazione figlia alquanto simile al tumore primario. È anche possibile che questi gruppi vengano disaggregati.
Quindi noi possiamo trovare in circolo, ed è una ricerca utilizzata a fini clinici, le cosiddette cellule tumorali circolanti (CTC). Esistono criteri e protocolli che ci permettono di caratterizzare la presenza di cellule tumorali circolanti nel sangue.
Metastatic site 210 0000 Embolic arrest Extravasation Apoptosis 0 Dormancy 0 Attachment to vessel wall 0 Proliferation within or outside vessels
Quindi, nelle interazioni omotipiche abbiamo aggregati di sole cellule neoplastiche; nelle interazioni eterotipiche oltre alle cellule neoplastiche troviamo anche cellule di altro tipo, ad esempio le piastrine, fonte importante di fattori di crescita, riparazione e proteasi. In alcuni casi possono anche essere rivestiti da leucociti.
A tumor cell Growth of intravascular micrometastases EMT 4ke tumge cell 1 Escape from immunosurveillance Stromal Trapping in microvessels Stromal Immune cells Istravpsation through A dopodia o Intravésation through leaky endothelium O Heterogeneous HOMOTYPIC duster Disaggregation 1 Macrophage mediated intravasation Single-cell file O Polycional tumor cell cooperativity and crosstalk facilitating survival Epithelial cell-cell Interactions Isolated CTCs Primary tumor/metastasis B Heterogeneous tumor cells Micrometastatic niches Tumor darmancy EMT-like tumor cell Hybrid tumor cell Apoptotic TCS HETEROTYPIC cluste Pag. 4 di 21