Reacciones y compuestos inorgánicos: formulación e identificación en Química
Diapositivas sobre Reacciones y Compuestos Inorgánicos. El Pdf, de Química para Bachillerato, detalla la formulación e identificación de compuestos inorgánicos, incluyendo óxidos, hidruros, hidróxidos y sales, con diagramas y un repaso de la tabla periódica.
Ver más32 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Unidad 5: Reacciones y Compuestos Inorgánicos
Objetivos de la Unidad
- A formular compuestos inorgánicos
- A identificar el tipo de compuesto inorgánico
- A colocar la nomenclatura del compuesto o a identificar el compuesto en base a la nomenclatura
- A identificar que tipo de enlace se establece en función de los componentes del compuesto... repasando Unidad 4
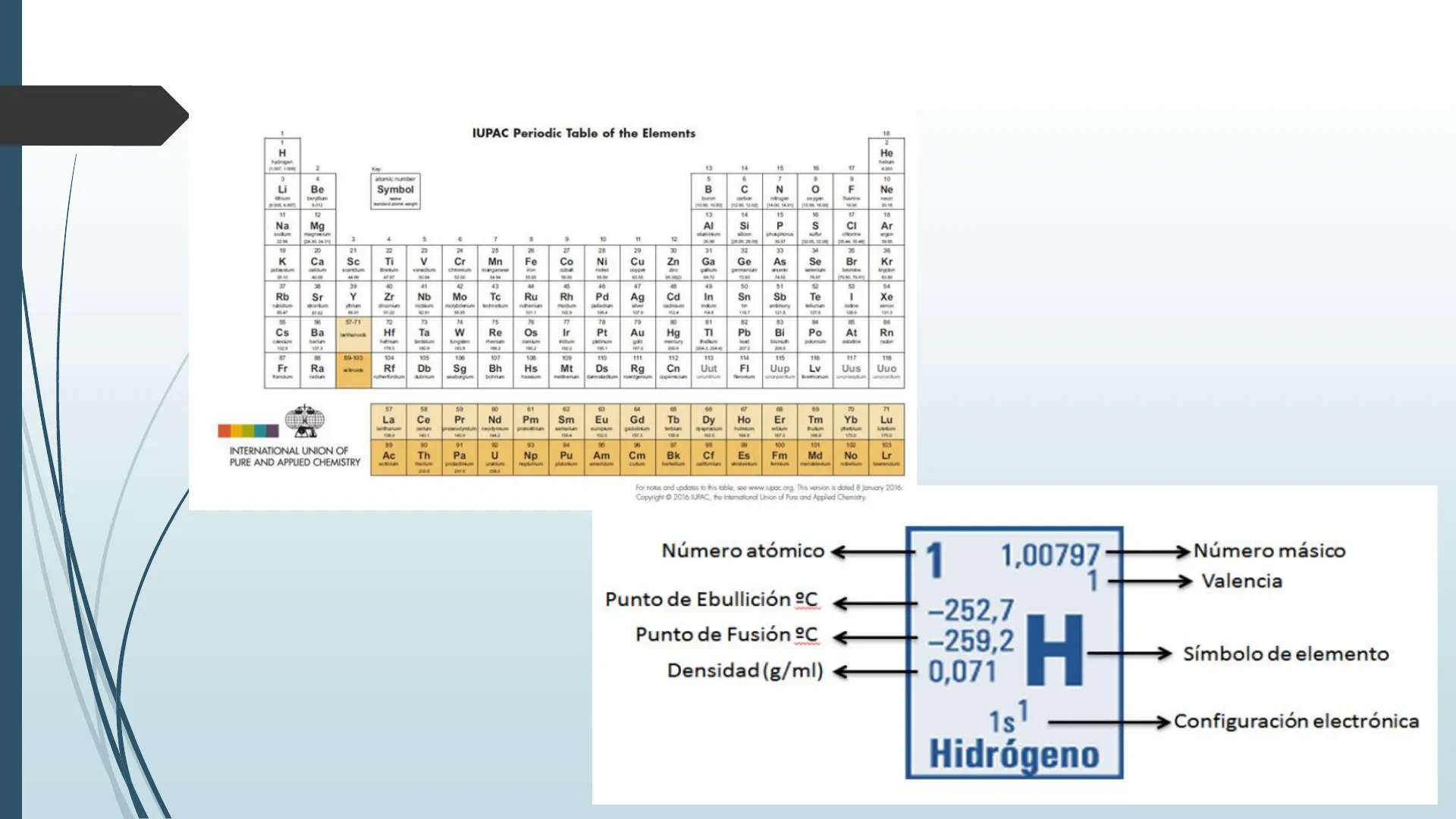
IUPAC Periodic Table of the Elements
15
H
He
13
14
15
10
17
10
Li
Be
B
C
- Z
N
O
.
F
farine
Ne
neon
11
12
13
14
15
16
17
18
Na
Mg
AI
Si
P
S
CI
Ar
3
4
5
6
-
9
10
12
32
33
35
36
K
Ca
-
Sc
-
22
Ti
24
Cr
Mn
Fe
-
Co
Ni
Ga
Ge
As
Br
Kr
Rb
nDidum
Sr
Y
Zr
Nb
-
Mo
Tc
Ru
RI
Pd
Ag
Cd
-
In
Sn
Sb
Te
53
2-
Xe
-
55
8
57-71
72
73
74
75
76
78
79
81
82
83
54
85
Cs
Ba
Hf
Ta
W
Re
Ir
Pt
Au
Hg
TI
Pb
Bi
Po
At
Rn
Fr
Ra
104
Rf
Db
Sq
Bh
Hs
Mt
Ds
Rg
Cn
Uut
Uup
LV
Uus
118
Uuo
INTERNATIONAL UNION OF
PURE AND APPLIED CHEMISTRY
For notos and updates to this table, spo www.lupac.org. This version is dated 8 January 2016.
Copyright O 2016 IURAC, the international Union of Pure and Applied Chemistry
Número atómico €
1
1,00797
> Número másico
1
> Valencia
Punto de Ebullición ºC
€
Punto de Fusión ºC
€
-252,7
-259,2
H
Símbolo de elemento
Densidad (g/ml)
0,071
1s 1
Hidrógeno
>Configuración electrónica
3
A
6
29
Cu
30
Zn
--
--
-
40
41
43
46
47
40
50
51
54
weretus
Os
-
-
104.3. 204.4
200 0
89-103
105
106
107
108
109
110
112
3
S
71
La
Ce
-
Pr
Nd
Sm
-
Eu
Gd
Tb
-
Dy
Ho
Er
-
69
Tm
-
70
Yb
Lu
89
Ac
Th
Pa
Np
Pu
Am
Cm
Bk
Cf
Es
Fm
Md
No
Lr
25
26
27
28
31
19
20
21
57
50
60
61
Pm
C 8
U
93
8
8
100
101
10
1521
-
115
114
FI
Mivitrdu
-
V
2
atomic number
Symbol
-
phongrona
Se
-1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
1
B
2
Si
3
Ge
As
4
Sb
Te
5
Po
At
6
117
7
metal
no metal
semimetalElementos representativos
Clasificación de Elementos Representativos
1
2
3
4
A
5
6
7
00
6
10
=
12
13
14
15
16
17
18
K
1
2
3
4
metales alcalinos
térreos
carbonoides
nitrogenoides
anfígenos
halógenos
gases nobles
5
metales alcalino-térreos
elementos de transición
6
7
6
elementos de transición interna
7Grupo
Configuración Electrónica de Elementos Representativos
| Nombre | Configuración | Nº electrones de valencia | |
| 1 (IA) | Metales alcalinos | ns1 | 1 |
| 2 (IIA) | Alcalino térreos | ns2 | 2 |
| 13 (IIIA) | Térreos | ns2np1 | 3 |
| 14 (IVA) | Carbonoides | ns2np2 | 4 |
| 15 (VA) | Nitrogenoides | ns2np3 | 5 |
| 16 (VIA) | Anfígenos | ns2np4 | 6 |
| 17 (VIIA) | Halógenos | ns2np5 | 7 |
| 18 (VIIIA) | Gases nobles | ns2np6 | 8 |
Configuración electrónica general de los elementos representativos según los grupos
NÚMEROS DE OXIDACIÓN DE LOS ELEMENTOS DE LA TABLA PERIÓDICA
IA
VIIIA
H
He
IIA
IIIA
IVA VA VIA VIIA
+1
Li
Be
B
C
N
O
F
Ne
+3
+2,±4
±1, ±2, ±3
+4,+5
-1,-2
-1
Na
Mg
AI
Si
P
S
CI
Ar
+1
+2
+3
+2,+4
+3,+5
±2,+4,+6
+3,+5,+7
K
Ca
Sc
Ti
V
+2,+3
+4,+5
Cr
+2,+3
+6
Mn
+2,+3
+4,+6,+7
Fe
Co
Ni
Zn
Ga
Ge
As
Se
Br
Kr
+1
+2
+3
+2,+3,+4
±3,+5
-2,+4,+6
±1
+3,+5,+7
Rb
Sr
Y
Zr
Nb
Mo
Tc
Rh
Pd
Ag
Cd
In
Sn
Sb
Te
I
Xe
+1
+2
+3
+3,+4
+2,+3
+4,+5
+2,+3
+4,+5,+6
+4,+5
+6,+7
+2,+3
+4,+5,+6
+2,+4
+1
+2
+1,+3
+2,+4
±3,+5
+2,+4,+6
+1
+3,+5,+7
Cs
Ba
La
Hf
Ta
W
Re
Ir
Pt
Au
Hg
TI
Pb
Bi
Po
At
Rn
+1
+2
+3
+3,+4
+3,+4,+5
+2,+3
+4,+5,+6
+2,+3
(+4,+6,+7)
+2,+3
+4,+5,+6
+2,+4
+1,+3
+1,+2
+1,+3
+2,+4
+3,+5
±2,+4,+6
±1,+5
Fr
+1
Ra
+2
Ac
Rf
Db
Sg
Bh
Hs
Mt
Uun
Uuu
Uub
Uut
Uuq
Uup
Uuh
Uus
Uuo
+3
+3,+4
+2,+3
+2,+3
+2,+3
Cu
+1,+2
+2
+1,+3
+2,+4
+1
+2
£1
Ru
+2,+3
+4,+5,+6
+7.+8
Os
+2,+3
+4,+5,+6
+7,+81
Carácter Metálico de los Elementos
2
3 4
5
6
9
10
11
12
13
14
15
16
17
18
1
B
2
Si
3
Ge
As
4
sb
Te
5
Po
At
6
117
7
metal
no metal
semimetal
Carácter metálico de los elementos y su variación en la tabla periódica
Electronegatividad de los Elementos
1
H
2,1
2
Inferior a 1,0
13
14
15
16
17
Li
1,0
Be
1,5
B
2,0
C
2,5
N
3,0
0
3,5
F
4,0
A1
1,5
Si
1,8
P
2,1
S
2,5
CI
3,0
K
0,8
Ca
1,0
Sc
1,3
Ti
1,5
V
1,6
Cr
1,6
Mn
1,5
Fe
1,8
Co
1,8
Ni
1,8
Cu
1,9
Zn
1,6
Ga
1,6
Ge
1,8
As
2,0
Se
2,4
2,8
Rb
0,8
Sr
1,0
Y
1,2
Zr
1,4
Nb
1,6
Mo
1,8
Tc
1,9
Ru
2,2
Rh
2,2
Pd
2,2
Ag
1,9
Cd
1,7
In
1,7
Sn
1,8
Sb
1,9
Te
2,1
2,5
Cs
0,8
Ba
0,9
La*
1,1
Hf
1,3
Ta
1,5
W
2,4
Re
1,9
Os
2,2
Ir
2,2
Pt
2,2
Au
2,4
Hg
1,9
TI
1,8
Pb
1,8
Bi
1,9
Po
2,0
At
Fr
0,7
Ra
0,9
Act
1,1
*
Lantánidos: 1,1-1,3
+ Actínidos: 1,3-1,5
9
10
11
12
3
4
5
6
7
8
2,0-2,4
1,0-1,4
2,5-2,9
1,5-1,9
3,0-4,0
Mg
Na
0,9
1,2
Br
I
2,2
Electronegatividad de los elementos y su variación en la tabla periódica
Compuestos Iónicos
Repasando ....... compuestos iónicos, son compuesto que contiene iones con carga
positiva y iones con carga negativa.
Mucha de la actividad química implica la transferencia de electrones entre sustancias, entonces Se
forman iones cuando uno o más electrones se transfieren de un átomo neutro a otro.
Na
Na+ + e-
NaCl
CI + e-
CI-
11e
10e
Pierde un
electrón
11p
11p
Ion Na+
CI
Átomo de Na
neutro
Na+
17e
18e
17p
17p
Gana un
electrón
Átomo de CI
neutro
lon CI
Sodio elemental reacciona con cloro elemental,
un electrón se transfiere de un átomo neutro
de sodio a un átomo neutro de cloro.
Nos queda un ion Na y un ion Cl, las partículas con cargas opuestas se atraen, los iones Na y Cl se
enlazan para formar el compuesto cloruro de sodio (NaCl),
El cloruro de sodio es un ejemplo de compuesto iónico: un compuesto que contiene iones con carga
positiva y iones con carga negativa.
En general, los cationes son iones metálicos; los aniones son iones no metálicos.
1
Compuestos Moleculares
Repasando ..... compuestos moleculares, son compuestos con uniones
covalentes
Los compuestos formados en su totalidad por no metales son sustancias moleculares
Una molécula es un conjunto de dos o más átomos estrechamente unidos, que al tener ambos elevada
afinidad electrónica, tienden a compartir sus electrones en la formación de uniones, de manera de
completar su octeto generalmente (enlaces covalentes)
+1
·
2e
.
+1
H
0
+
O
H
H
H:H
H - H
PREDICCIÓN DE LAS CARGAS IÓNICAS
Recordemos ...... Muchos átomos ganan o pierden electrones con el fin de quedar con el
mismo número de electrones que el gas noble más cercano a ellos en la tabla periódica.
Los gases nobles son quimicamente muy poco reactivos y difícilmente forman compuestos, dado que
sus arreglos electrónicos son muy estables.
Los elementos cercanos pueden alcanzar estos mismos arreglos estables perdiendo o
ganando electrones.
Ejemplo:
Elátomo de sodio pierde un electrón (catión) pasa a tener el mismo número de
electrones que el átomo neutro de neón (número atómico 10).
El cloro gana un electrón queda con 18, lo mismo que el argón (número atómico 18).
La tabla periódica es muy útil para
recordar las cargas de los iones, sobre
todo las de los elementos que están en
los extremos izquierdo y derecho de la
tabla, y algunos elementos de
transición
1A
7A 8A
H+
H
2A
3A
4A
5A
6A
Li+
N3-
02-
F
Na+
Mg2+
Metales de transición
AI3
p3-
s2-
CI-
K+
Ca2+
Cr3
Mn2+
Fe2+
Fo3+
Co2+
Ni2+
Cu+
Cu2+
Zn2
Se2-
Br-
N
O
Rb+
Sr2+
Ag+
Ca2+
Sn2+
Te2-
L
Cs+
Ba2+
P+2+
Au+
Au3+
Ph2+
Bi3+
S
+
G
A
S
E
S
B
PROPIEDADES QUIMICAS
Metales
- Los metales se oxidan (pierden electrones) cuando participan en reacciones
química, por su baja EI. - Muchos metales se oxidan con diversas sustancias comunes, incluidos el O2, el H2 y
los ácidos, forman compuestos iónicos - de los óxidos metálicos son básicos. Los que se disuelven en agua reaccionan para
formar hidróxidos metálicos
No Metales
- Debido a sus afinidades electrónicas, los no metales, al reaccionar con metales,
tienden a ganar electrones (se reducen), forman compuestos iónicos - Los óxidos, halogenuros e hidruros de los no metales son sustancias moleculares,
forman enlaces covalentes - La mayor parte de los óxidos no metálicos son ácidos; los que se disuelven en agua
reaccionan para formar ácidos - los ácidos, y casi todos los óxidos no metálicos se disuelven en disoluciones básicas
para formar sales
Dra. Xenia Hernández
Metales, No metales y metaloides
Metales
alcalinos
Metales
No metales
Gases
nobles
8A
(1)
Metales
alcalinotérreos
Halógenos
3A
(13)
4A
(14)
5A
(15)
6A
(16)
7A
(17)
2
He
5
B
6
C
7
N
8
O
9
F
10
Ne
3
11
Na
12
Mg
3B
5B
6B
(6)
7B
(7)
(8)
(9)
(10)
(11)
(12)
4
19
K
20
Ca
21
Sc
22
23
24
Cr
25
Mn
26
Fe
27
Co
28
Ni
29
Cu
30
Zn
31
Ga
32
Ge
33
As
34
Se
35
Br
36
Kr
5
37
Rb
38
Sr
39
Y
40
Zr
41
Nb
42
Mo
43
E
44
Ru
45
Rh
46
Pd
47
Ag
48
Cd
49
In
50
Sn
51
Sb
52
Te
53
I
54
Xe
.
6
55
Cs
56
Ba
57
La
72
Hf
73
Ta
74
W
75
Re
76
Os
77
Ir
78
Pt
79
Au
80
Hg
81
TI
82
Pb
83
Bi
84
Po
85
At
86
Rn
7
87
Fr
88
Ra
89
Ac
104
Rf
105
Db
106
Sg
107
Bh
108
Hs
109
Mt
110
Ds
111
Rg
112
Cn
113
(Uut)
114
FI
115
(Uup)
116
Lv
117
(Uus)
118
(Uuo)
58
Ce
59
Pr
60
Nd
61
Pm
62
Sm
63
Eu
64
Gd
65
Tb
66
Dy
67
Ho
68
Er
69
Tm
70
Yb
71
Lu
t
90
Th
91
Pa
92
U
93
Np
94
Pu
95
Am
96
Cm
97
Bk
98
Cf
99
Es
100
Fm
101
Md
102
No
103
Lr
Existen otros sistemas para numerar los grupos de la tabla periódica. Aqui utilizaremos el sistema en el que se clasifican como A y B
los grupos. Un sistema alternativo es numerar a los grupos de 1 a 18, que aparece entre paréntesis, el cual es el recomendado por la IUPAC.
1B
2B
13
Al
14
Si
15
P
16
S
17
18
CI
Ar
(3)
4B
(4)
(5)
Ti
V
(2)
2
3
Li
4
Be
Metales de transición
8B
1A
Metaloides
(18)
1
1
H
2A
+
COMPUESTOS QUÍMICOS
ORGÁNICOS (se estudiarán más adelante)
INORGÁNICOS
Agrupados en funciones químicas
ÓXIDOS
HIDRÓXIDOS
ÁCIDOS
SALES
COMPUESTOS INORGÁNICOS -diagrama I
METALES
NO METALES
BINARIOS
Hidrogeno
HIDRUROS
metálicos
=
=
HIDRUROS no metálicos
(en agus):
ÁCIDOS HIDRÁCIDOS
BINARIOS
Oxigene
BINARIOS
=
ÓXIDOS BÁSICOS
u oxidos metalicos
ÓXIDOS ÁCIDOS
.
BINARIOS
Agua
TERNARIOS
L
HIDRÓXIDOS
OXÁCIDOS
(acidos)
TERNARIOS
+
SALES NEUTRAS
SALES ACIDAS
SALES BASICAS
SALES DOBLES
TERNARIOS
CUATERNARIOS
CUATERNARIOS
CUATERNARIOS
+
SALES BASICAS
COMPUESTOS INORGÁNICOS-diagrama II
SALES BINARIAS
METAL
NO METAL
OXÍGENO +
+ HIDRÓGENO
OXÍGENO
+
+ HIDRÓGENO
OXIDOS BÁSICOS
HIDRUROS METÁLICOS
OXIDOS ACIDOS
HIDRUROS NO METÁLICOS
H20
+
H20 +
H20
H2O
HIDROXIDOS
OXOÁCIDOS
HIDRÁCIDOS
OXOSALES
SALES BINARIAS
COMPUESTOS INORGÁNICOS-diagrama III
Clasificación de Compuestos Inorgánicos
Compuestos Inorgánicos
Binarios
Ternarios
Cuaternarios
Con oxigeno
Hidróxidos
Sales acidas
óxidos
Oxoácidos
Sales básicas
-peróxidos-
Sales neutras
-superóxidos
Con hidrogeno
Sales Binarias
Hidruros metálicos
Hidruros no metálicos
REGLAS Y CONCEPTOS GENERALES
Los compuestos (binarios y ternarios) en su nomenclatura están compuestos por dos
nombres: el genérico y el específico.
El nombre genérico es el que indica a qué grupo de compuestos pertenece la molécula o su
función química,
por ejemplo ....
si es un óxido metálico/básico, un óxido no metálico/ácido, un peróxido, un hidruro,
un hidrácido, un oxácido, una sal haloidea, etc.
El nombre específico es el que diferencia a las moléculas dentro de un mismo grupo de
compuestos ....
óxido ferroso y óxido férrico, estos dos compuestos pertenecen al grupo de los óxidos y
por eso su nombre genérico es óxido y a la vez los nombres específicos ferroso y férrico
hacen referencia a dos compuestos diferentes FeO y Fe2O3, respectivamente.