Metabolismo: Cadena de Transporte E- y Fosforilación Oxidativa, Usc, Presentación
Diapositivas de Usc Universidade de Santiago de Compostela sobre Bloque Ii: Metabolismo Tema 7. Cadena de Transporte E- y Fosforilación Oxidativa. El Pdf, una presentación de Biología de nivel universitario, detalla el gradiente electroquímico de protones y su uso en la síntesis de ATP, incluyendo mecanismos de transporte mitocondrial.
Ver más47 páginas
Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Bioquímica: Grado en Enfermería
Departamento de Bioquímica y Biología Molecular
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular BLOQUE II: METABOLISMO Tema 7. Cadena de transporte e- y fosforilación oxidativa Juan Jose Nieto Fontarigo
Contenidos del Tema 7
Cadena de transporte electrónico
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular Contenidos Tema 7.1. Cadena de transporte electrónico
- Fuente de electrones para la cadena respiratoria
- Lanzaderas mitocondriales
- Flujo electrónico mitocondrial
- Transportadores electrónicos
- Gradiente electroquímico de protones
Fosforilación oxidativa
Tema 7.2. Fosforilación oxidativa
- Teoría quimiosmótica
- ATP Sintasa
- Estequiometría y rendimiento
- Regulación de la fosforilación oxidativa
- Acoplamiento de la fosforilación y cadena de transporte electrónico
- Formación de especies reactivas (ROS)
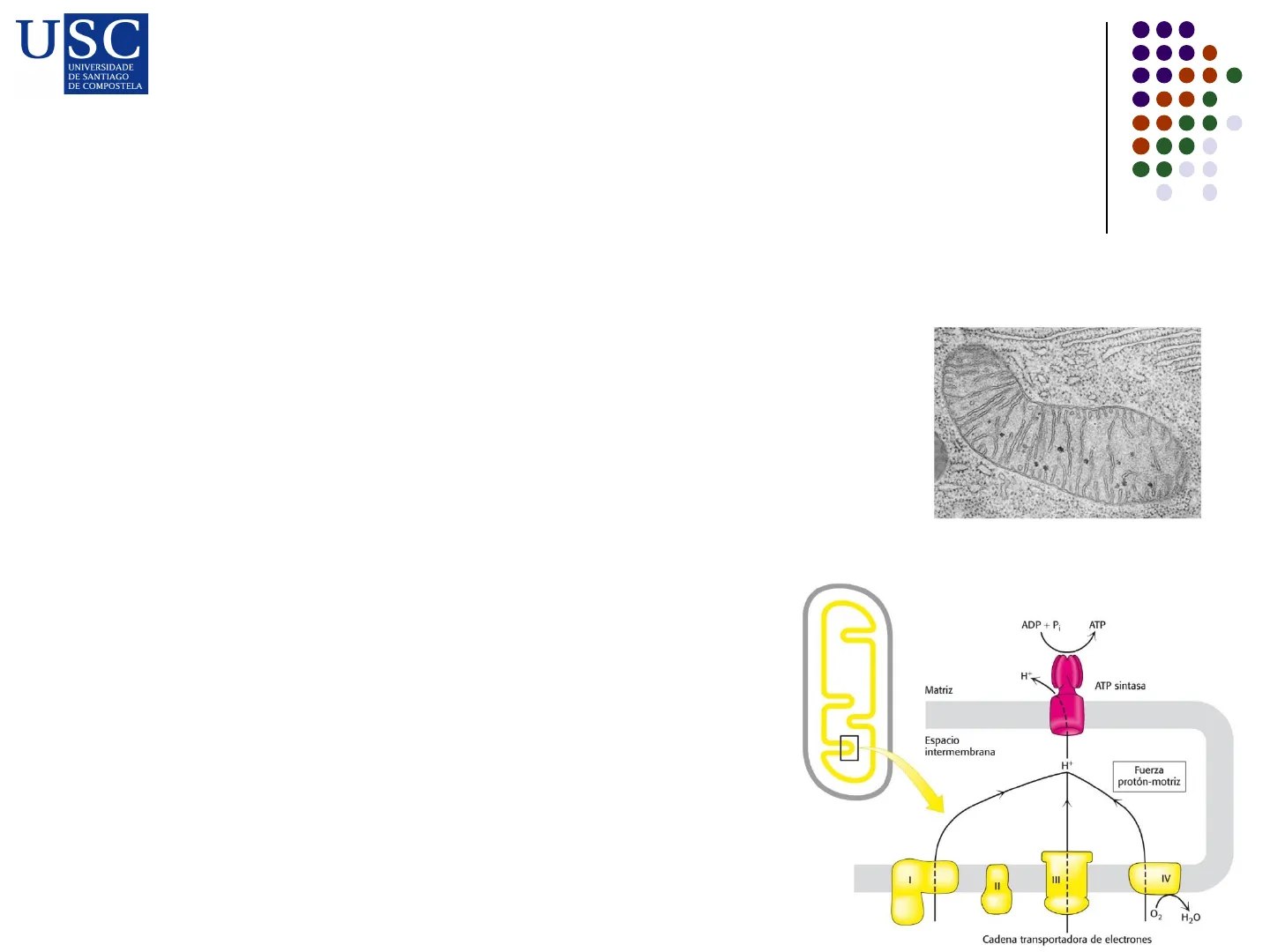
ADP + Pi ATP H Matriz ATP sintasa Espacio intermembrana H Fuerza protón-motriz O2 H20 IV Cadena transportadora de electrones
Tema 7.1. Cadena de transporte electrónico
Contenidos del Tema 7.1
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular Tema 7.1. Cadena de transporte electrónico Contenidos
- Fuente de electrones para la cadena respiratoria
- Lanzaderas mitocondriales
- Flujo electrónico mitocondrial
- Transportadores electrónicos
- Gradiente electroquímico de protones
Juan Jose Nieto Fontarigo
Fuentes de electrones para la cadena respiratoria
Glucólisis, oxidación de piruvato y ciclo de Krebs
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular Tema 7.1. Cadena de transporte electrónico 1. Fuentes de electrones para la cadena respiratoria Resultado de la glucólisis + oxidación de piruvato + ciclo de Krebs Glucosa + 10 NAD+ + 2 FAD + 4 ADP + 4 Pi 6 CO2 + 10 NADH + 10 H+ + 2 FADH, + 4 ATP
- El catabolismo oxidativo genera electrones que quedan almacenados en forma de NADH y FADH2
- Reacciones que generan NADH:
- Glucolisis: GAPDH
- Oxidación de Piruvato: Piruvato deshidrogenasa
- Ciclo de Krebs: Isocitrato, a-Cetoglutarato y Malato Deshidrogenasas
- 6-oxidación: b-Hidroxiacil-CoA Deshidrogenasa
- Otras
O H C NH2 +2 0-CH2 0. H H o=P-O~ H N H OH OH NH 2 -O- N o=P-O- N -O CH2 H H H H NAD+ (oxidized) N Nº OH OH
Reacciones que generan FADH2
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular Tema 7.1. Cadena de transporte electrónico 1. Fuentes de electrones para la cadena respiratoria Resultado de la glucólisis + oxidación de piruvato + ciclo de Krebs Glucosa + 10 NAD+ + 2 FAD + 4 ADP + 4 Pi 6 CO2 + 10 NADH + 10 H+ + 2 FADH2 + 4 ATP
- El catabolismo oxidativo genera electrones que quedan almacenados en forma de NADH y FADH 2
- Reacciones que generan FADH2:
- Ciclo de Krebs: Succinato Deshidrogenasa
- 6-oxidación: Acil-CoA Deshidrogenasa
- Otras
O H3C N NH H3C N N O CH2 Riboflavina CHOH I CHOH 1 CHOH - CH2 O 1 0-P=0 NH2 "0-P=0 N N 1 0 N Nº Adenina CH2 O エ ー H/ H H OH OH
Re-oxidación de transportadores electrónicos
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular Tema 7.1. Cadena de transporte electrónico 1. Fuentes de electrones para la cadena respiratoria
- La re-oxidación de transportadores electrónicos reducidos (NADH, NADPH y FADH2, FMNH2) genera la mayor parte de la energía necesaria para la síntesis de ATP.
- En condiciones aerobias, esto ocurre en la cadena de transporte electrónico o cadena respiratoria: proceso de transferencia escalonada de electrones desde los transportadores reducidos hasta el O2.
- La cadena de transporte electrónico se lleva a cabo en la membrana mitocondrial interna (a) ATP synthase (FOF1) Outer membrane Freely permeable to small molecules and ions Cristae Inner membrane Impermeable to most small molecules and ions, including H+ Contains: · Respiratory electron carriers (Complexes I-IV) · ADP-ATP translocase · ATP synthase (F.F1) · Other membrane transporters Matrix Contains: · Pyruvate dehydrogenase complex · Citric acid cycle enzymes · Fatty acid B-oxidation enzymes · Amino acid oxidation enzymes Ribosomes · DNA, ribosomes · Many other enzymes Porin channels · ATP, ADP, Pi, Mg2+, Ca2+, K+ · Many soluble metabolic intermediates
Lanzaderas mitocondriales
Transporte de NADH al interior de la mitocondria
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular Tema 7.1. Cadena de transporte electrónico 2. Lanzaderas mitocondriales
- La glucolisis genera NADH en el citoplasma. La entrada de la cadena del transporte electrónico (Complejo I) está en la matriz mitocondrial.
- La membrana mitocondrial es impermeable a NAD+ NADH Intermembrane space (P side) 2H+ 4H+ 4H+ Cyt c Q IV 102 + 2H+ H2O NADH + H+ NAD+ Succinate Fumarate Matrix (N side)
- El NADH debe enviarse al interior de la mitocondria mediante una serie de rutas
denominadas lanzaderas mitocondriales. Las más importantes son dos:
- Lanzadera del malato-aspartato
- Lanzadera del glicerol 3-fosfato
Lanzadera del Malato-Aspartato
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular Tema 7.1. Cadena de transporte electrónico 2. Lanzaderas mitocondriales Lanzadera del Malato-Aspartato
- Tiene lugar en hígado, riñón y corazón. El efecto neto es el intercambio de dos electrones entre citosol y mitocondria (Daran lugar a 2.5 ATP)
- Es un sistema reversible
- Transporta el NADH citosólico a la mitocondria cuando la relación NADH/NAD+ es mayor en el citosol que en la matriz mitocondrial. NAD+ Oxalacetato Glutamato NADH Malato DH XA AAT Malato a-Cetoglutarato Aspartato Citoplasma Matriz a-Cetoglutarato Aspartato Malato Malato DH AAT NAD+ Oxalacetato Glutamato
- Enzimas:
- Malato deshidrogenasa
- Aspartato aminotransferasa (AAT)
NADH
Lanzadera del Glicerol-3-Fosfato
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular Tema 7.1. Cadena de transporte electrónico 2. Lanzaderas mitocondriales Lanzadera del Glicerol-3-Fosfato
- Tiene lugar en cerebro y músculo. El efecto neto es el transferencia de dos electrones reductores desde un NADH citosólico a un FAD mitocondrial.
- Cede los e- al complejo Ill y no al | > solo se genera 1.5 ATP por cada par de -
- La DHAP de la glucolisis se reduce a glicerol 3-fosfato (Glicerol-3-fosfato DH citosólica)
- La Glicerol-3-fosfato DH mitocondrial está anclada en la membrana interna de la mitocondria y vuelve a formar dihidroxiacetona fosfato (Reduce FAD). Los electrones del NADH entran en el transporte electrónico a través de ubiquinona (Q) Intermembrane space (p side) Glycolysis NAD+ NADH + H+ cytosolic glycerol 3-phosphate dehydrogenase CH2OH C=0 Glycerol 3- phosphate Dihydroxyacetone phosphate 1 CH2-0-P CH2OH 1 CHOH I mitochondrial glycerol 3-phosphate dehydrogenase CH2-0-P FAD FADH2 QH2 Complex III Matrix (N side)
Flujo electrónico mitocondrial
Procesos ligados de transporte y fosforilación
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular Tema 7.1. Cadena de transporte electrónico 3. Flujo electrónico mitocondrial La cadena de transporte electrónico y fosforilación oxidativa son procesos ligados donde:
- Los e- fluyen de dadores electrónicos hasta el O2 mediante transportadores electrónicos en la membrana interna mitocondrial en una serie de reacciones redox ligadas: Reductor (donador e-) + oxidante (aceptor e-) Reductor oxidado + oxidante reducido AH2 (donador e") + B (aceptor e" ) > A + BH2 1 Reduced substrate (fuel) donates e -. 2 Electron carriers pump H+ out as electrons flow to O2. H+ Electron carriers (respiratory chain) H+ Inner H+ H+ H+ H+ H+ mitochondrial + membrane + H+ - + + - - + - Reduced e- donor O2 (e- acceptor) 1 4+ Membrana mitocondrial interna H+ H+ H+ I H+ G II H+ F Espacio intermembranoso Q H+ H+ III H+ cit C 4H+ + O2 H+ IV H+ H+ 4e- 2H2O H+ ADP + Pi H+ H+ V H+ H+ H+ - H+ H+ + H+ UCP H+ Figura 8.5. Baynes & Dominiczak: BIOQUÍMICA MÉDICA. 5ª Ed. @ Elsevier, 2019. ATP Dirección del flujo de electrones Matriz H+ H + +
Acoplamiento del flujo de electrones al transporte de H+
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular Tema 7.1. Cadena de transporte electrónico 3. Flujo electrónico mitocondrial La cadena de transporte electrónico y fosforilación oxidativa son procesos ligados donde:
- El fujo de e- está acoplado al transporte de H+ hacia el espacio intermembrana, generando un gradiente de concentración → La energía derivada del flujo de e- se conserva en forma de potencial electroquímico. Membrana mitocondrial interna H+ H+ H+ I H+ G II H+ F Espacio intermembranoso Q H+ H+ III H+ cit C 4H+ + H+ H+ IV H+ H+ 4e- 2H2O H+ ADP + Pi H+ H+ H+ V H+ ATP UCP H+ H+ Dirección del flujo de electrones Intermembrane space (P side) 4H+ 4H+ Cyt c Q IV 102 + 2H+ H2O NADH + H+ NAD+ Succinate Fumarate Matrix (N side) Nelson & Cox: Lehninger Principios de Bioquimica. @ Ed Omega, 2019 Figura 8.5. Baynes & Dominiczak: BIOQUÍMICA MÉDICA. 5ª Ed. @ Elsevier, 2019. Matriz 2H+ O2
Síntesis de ATP por potencial electroquímico
USC UNIVERSIDADE DE SANTIAGO DE COMPOSTELA Bioquímica Grado en Enfermería. Facultad de Enfermería Departamento de Bioquímica y Biología Molecular Tema 7.1. Cadena de transporte electrónico 3. Flujo electrónico mitocondrial La cadena de transporte electrónico y fosforilación oxidativa son procesos ligados donde:
- El flujo de H+ a favor de gradiente a través de un canal específico proporciona energía libre para la síntesis de ATP (Fosforilación oxidativa). 1 Reduced substrate (fuel) donates e -. 2 Electron carriers pump H+ out as electrons flow to O2. H+ Electron carriers (respiratory chain) H+ Inner H+ H+ H+ H+ H+ + + H+ + + - e - H+ H+ O2 + Reduced e- donor (e- acceptor) H+ 3 - - 1 - ATP synthase + ADP + P. H+ 1 + - ATP - - H+ + + H+ + + + H+ H+ H+ H+ H+ H+ H+ H+ H+ 4 ATP synthase uses electrochemical potential to synthesize ATP. Intermembrane space ++ ++ ATP4- ATP4- ADP3- ADP3- + + H+ H+ + + H2PO4 Phosphate translocase (symporter) H2PO4 H+ H+ + + + + Sistemas de transporte mitocondrial 2.5 moles de ATP de cada mol de NADH Nelson & Cox: Lehninger Principios de Bioquimica. @ Ed Omega, 2019 Matrix Adenine nucleotide translocase (antiporter) H+ mitochondrial membrane + - H + + + Energy of e- flow is stored as electrochemical potential. + H+ - + >H+ H+ H+ H+ H+ ATP synthase