Estructura cristalina de los materiales y sus defectos
Diapositivas sobre la estructura cristalina de los materiales y sus defectos. El Pdf explora las imperfecciones en sólidos cristalinos, como defectos de punto, línea y superficie, con un enfoque en las maclas, útil para estudiantes universitarios de Física.
Ver más48 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Estructura cristalina de los materiales y sus defectos
- Estructuras cristalinas de los metales
Imperfecciones en sólidos cristalinos
- Defectos de punto
- Defectos de línea
- Defectos de superficie
- Fenómenos de deslizamiento
tema 2
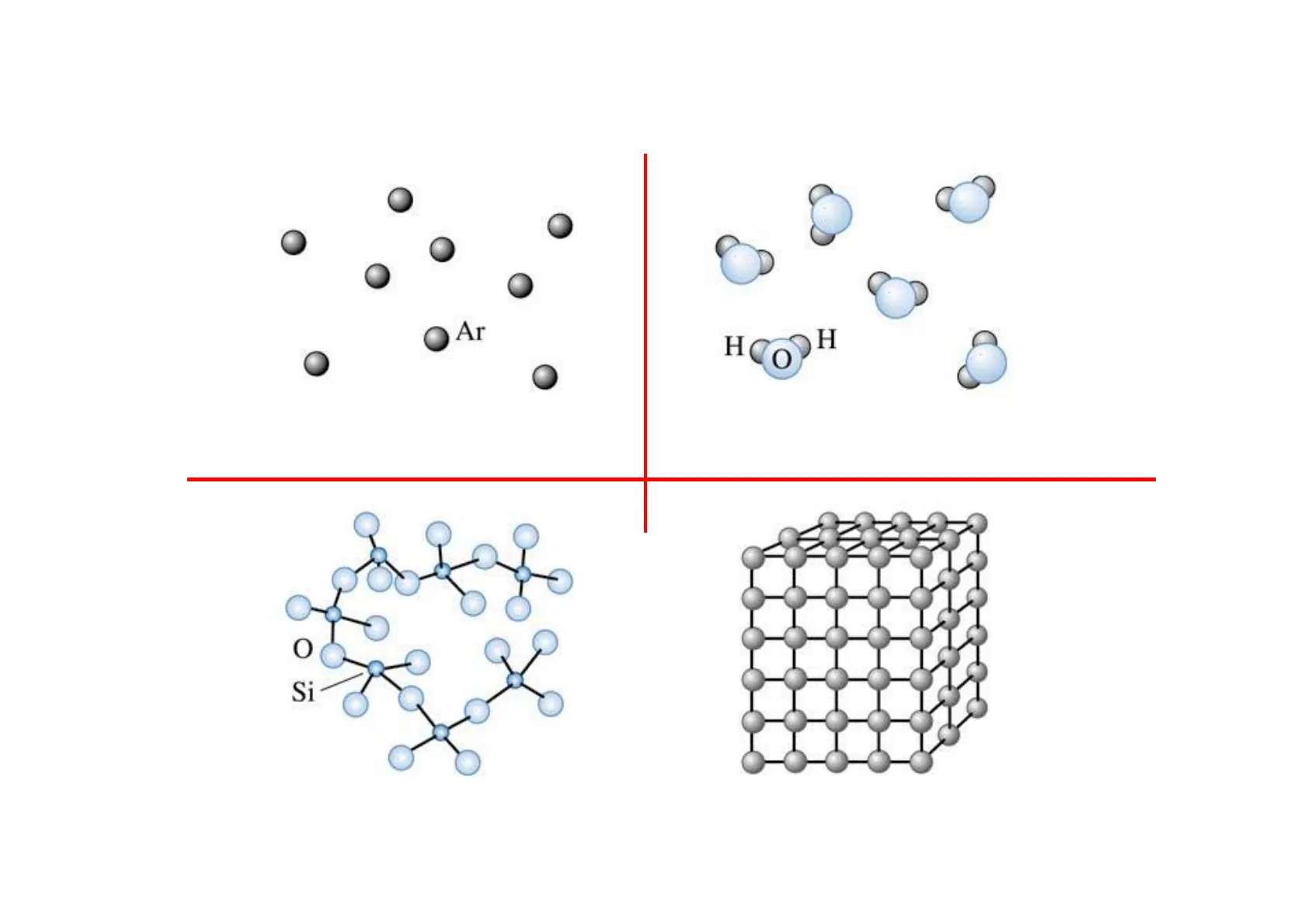
Estados de agregación de la materia
Ordenamiento de Corto y Largo alcance
Ar
Gases (Desorden)
H
H
O
Líquidos (Orden de corto alcance)
0
Si
tema 2
Vidrio (Orden de corto alcance)
Metal, Cerámico (Orden de largo alcance)
Sólidos
Estados de agregación de la materia
Ordenamiento de Corto y Largo alcance
Conjunto de los estados de equilibrio que pueden ser adoptados por un cuerpo variando sus propiedades de forma continua.
Si las propiedades físicas se modifican discontinuamente > cambia el estado de agregación.
Estados de agregación: gaseoso, líquido y sólido.
- Gaseoso carece de estabilidad de volumen y de estabilidad de forma.
- Líquido tiene estabilidad de volumen pero no estabilidad de forma.
- Sólido presenta estabilidad de forma y estabilidad de volumen.
Muchas sustancias líquidas, al enfriarse > modificación gradualmente de sus propiedades > parecen sólidos sin la existencia de un cambio de estado.
Ejemplo: alquitrán al enfriar aumenta progresivamente su viscosidad, crece su resistencia al cambio de forma y a temperatura suficientemente baja, posee aparentemente estabilidad de forma y parece un sólido > líquido subenfriado.
tema 2
Cristales
- Cuerpos en que los átomos, iones o moléculas adoptan posiciones de equilibrio fijas y ordenadas regularmente en el espacio.
- Si se considera la línea determinada por los centros de dos moléculas o iones consecutivos, se encuentran a lo largo de ella otras moléculas o iones idénticos, separados por iguales intervalos.
- Los puntos que definen las posiciones de esas partículas materiales constituyen así una red tridimensional característica de la estructura cristalina del cuerpo de que se trate.
- Las estructuras cristalinas de los sólidos conocidos constituyen un conjunto extremadamente numeroso, pero su estudio se sistematiza si las referimos a las redes espaciales posibles.
- El concepto de red espacial es puramente geométrico.
- Se llama red espacial a una distribución tridimensional de puntos, ordenados de tal forma que cada punto de la red tiene alrededores idénticos.
Cristales y redes de Bravais
- La geometría de la red espacial debe permitir que se llene todo el espacio de átomos sin dejar huecos, característica que hace que sólo existan 14 tipos de redes posibles (redes de Bravais)
- Cada red está caracterizada por una celda unidad, que, a su vez viene definida por una serie de parámetros de red (llamados también fundamentales).
Aristas: (a / b / c ) Ángulos: (a / B / Y)
- La celda unidad es la subdivisión de la red cristalina que sigue conservando las características generales de toda la red.
Celda unidad
Puntos de la red
tema 2
Triclínica
Monoclínica simple
Monoclínica de bases centradas
Rómbica simple
Rombica de bases centradas
Rombica de caras y bases centradas
Rómbica centrada
Romboédrica
Hexagonal
Tetragonal simple
Tetragonal centrada
Cúbica simple
Cúbica de caras centradas
Cubica centrada
Cristales y sistemas cristalinos
Los vértices de las celdas unidad se llaman nudos.
> Las redes de Bravais pueden tener puntos no solo en los nudos sino también en otras posiciones.
>
Puntos en el centro de las bases -> red centrada en las bases.
> Punto en el centro del prisma > red centrada en el cuerpo.
> Punto en el centro de cada cara la red > red centrada en las caras.
> Las 14 redes espaciales pueden agruparse en 7 sistemas cristalinos caracterizados por las relaciones entre las aristas y los ángulos que estas forman entre sí en la celda unidad.
Las aristas de la celda unidad se designan por a, b, c y los ángulos que forman por a, B, y (parámetros de red o constantes reticulares).
| Nombre | Relaciones |
|---|---|
| TRICLÍNICO | a + b + c; a + B + y ± 90° |
| MONOCLÍNICO | a + b # c; a = B= 90° ± y |
| ORTORRÓMBICO | a + b + c; a = B = y = 90° O RÓMBICO |
| TETRAGONAL | a = b # c; a = B = y = 90° |
| HEXAGONAL | a = b # c; a = B = 90° y = 120° |
| ROMBOÉDRICO | a = b = c; a = B = Y # 90° |
| CUBICO | a = b = c; a = B = y = 90° |
tema 2
Planos y direcciones cristalinas. Índices de Miller
- La estructura cristalina de los materiales está relacionada tanto con las propiedades mecánicas como con la microestructura de los mismos, y se define mediante los Planos cristalográficos y direcciones cristalográficas.
- Plano cristalográfico: definido por tres puntos cualesquiera de la red, no alineados.
- Otra terna cualquiera de puntos con igual disposición relativa determinará otro plano paralelo al anterior y sobre el cual, los puntos de la red que contenga estarán dispuestos de igual forma, se tratara de un plano equivalente.
- La cualidad definitoria de un plano cristalográfico es su orientación con respecto al sistema de referencia.
- Dos puntos cualesquiera de la red determinan una dirección cristalográfica que tendrá, el mismo significado que otra paralela definida por dos puntos homólogos. Siendo la cualidad característica de las direcciones cristalográficas su orientación.
- Para identificar los diferentes planos y direcciones en un cristal se usan los índices de Miller, para planos (hkl), para direcciones [uvw].
- Los planos que son cristalográficamente equivalentes se representan: {hkl}.
- Las direcciones equivalentes se representan: < uvw>.
- En el sistema hexagonal se utilizan cuatro índices. Una serie de planos se representa por (hkil). Entre los tres primeros índices existe siempre la relación i = - (h + k).
Planos compactos
b
a
C
C
a
b
Direcciones compactas en un plano octaédrico en la red ccc
Plano de máximo empaquetamiento de átomos considerados como esferas rígidas
tema 2
Planos compactos y apilamiento
apilamiento a b
apilamiento a a
tema 2
apilamiento a b c
apilamiento a b a
Redes comunes de metales
ESTRUCTURA CUBICA CENTRADA EN EL CUERPO (CC)
ESTRUCTURA HEXAGONAL COMPACTA (HC)
ESTRUCTURA CUBICA CENTRADA EN LAS CARAS (CCC)
empaquetamiento a b c
empaquetamiento a b a
tema 2
Red cúbica centrada en el cuerpo (CC)
Fe (a), Cr (a), V, Mo, W, Li, Na y K
Número de átomos por celda unidad
N- Ni + Ne + Na
Ni= Número de átomos en el interior de la celda
Nc = Número de átomos en cada cara de la celda
Nv = Número de átomos en cada vertice de la celda
Número de átomos por celdilla unidad para la red cc
N= 1+ == 2 átomos 8
8
Índice de coordinación: 8
Planos y direcciones compactas
4 Direcciones compactas: diagonales del cubo <111>
Planos compactos: no hay
ESTRUCTURA CUBICA CENTRADA EN EL CUERPO (CC)
Ejes de simetría
<111>
<110>
<100>
3 ejes cuaternarios 4 ejes ternarios 6 ejes binarios
Ejes de simetría en la red cc
tema 2
Red cúbica centrada en el cuerpo (CC): Relación a-r
D = 4r
d2 = 2a2 => d=av2
D2 = a2 + (a 2)2= 3a2
(4r)2 = 3a2
av3 r= 4
r
D
2r
r
a
d
Cálculo de radio atómico en la red cúbica centrada en el cuerpo
Índice de empaquetamiento (factor de empaquetamiento)-(FEA)
i= n Va V c
n = Número de átomos de la celdilla.
Va = Volumen el átomo.
Vc = Volumen de la celdilla unidad.
n=2
Va= 4 -πr' .3 = 3
4 3 - T av3 4 3
4 3 3 a3 312 43
3/2 = πα331/2 42
Vc=a3
Sustituyendo:
2 Tt a3 312 42 a3
21/2 3 i= = 8 =
i = 0,68
68% del volumen del cubo.
tema 2
Red cúbica centrada en el cuerpo (CC): Densidad lineal y planar
Densidad lineal
nº de átomos en una dirección 2 átomos longitud de la dirección (f. de a) av3 nm
Densidad planar
En el plano (100): nº de átomos en un plano 1 átomos área del plano (f. de a) a2 nm 2
z
[111]
y
x
Densidad lineal en la dirección [111] de la celda cc
Z
(1,1,1)
V
(1,1,0)
(100)
Densidad planar (100) en la red cúbica centrada en el cuerpo
En el plano (110): nº de átomos en un plano 2 átomos área del plano (f.de a) a22 nm2
(0,1,0)
y
(1,0,0)
d
x
(110)
Densidad planar (110) en la red cúbica centrada en el cuerpo
z
(0,1,1)
D
= (12,1/2 1/2)
a
tema 2
Red cúbica centrada en el cuerpo (CC): Ejemplo de cálculo de densidad
= =
Ejemplo de cálculo de densidad
Cálculo de la densidad del Cr (cc) conocido el parámetro de red obtenido por Difracción de Rayos-X.
p= n M a VN C A
NA = 6,02214076 x 1023 mol-1/g
a = 0,289 nm
n = 2 átomos celda
M a = 52,01 g/at- at - g
Vc= a3 = 23,88 x 10-24 cm 3 celda
Sustituyendo en la densidad sale p = 7,20 g/cm3 (densidad teórica)
La densidad del Cr (cc) es 7,19 g/cm3 a 20°℃ (experimental)
tema 2
Red cúbica centrada en las caras (CCC)
Fe (y), Al, Co (B), Ni(B), Cu, Ag, Pt, Au, Pb y Ca
A
A
A
4
A
A
A
B
B
B
B
B
B
C
C
A
B
B
8
B
A
A
A
A
B
B
B
18
A
A
A
A
A
A
A
A
ESTRUCTURA CUBICA CENTRADA EN LAS CARAS (CCC)
Número de átomos por celda unidad
=N,+Nc + Nv=0+6 + 8 = 4 ato
Índice de coordinación: 12
Planos y direcciones compactas
6 Direcciones compactas: diagonales de caras <110>
4 Planos compactos: planos diagonales {111}
tema 2
Ejes de simetría
<111>
<{110}
<100>
3 ejes cuaternarios 4 ejes ternarios 6 ejes binarios
Ejes de simetría en la red ccc
Red cúbica centrada en las caras (CCC): Relación a-r
A
A
C
C
C
B
B
A
Relación a-r
d = 4r
d2 = 2a2
(4r)2 = 2 a2 => 4r=av2
av2 r= 4
r
d
a
2r
r
Cálculo de radio atómico en la red cúbica centrada en las caras
Índice de empaquetamiento
i= n Va V . C
n= 4
Va= 4 3 P= +7 (2) 3 =
4 = 3 3 43 )3/2 π α' 2502 3.42
a
Vc=a3
i= 4 IT a3 23/2 3.42 a3 3 = π 202 12 =
π 2 6
i = 0,74
74% del volumen del cubo
tema 2
Red cúbica centrada en las caras (CCC): Densidad lineal y planar
Densidad lineal
En la diagonal de la cara del cubo [110]:
y
[110]
x
nº de átomos en una dirección 2 átomos longitud de la dirección (f. de a) = av2 nm
Densidad planar
En el plano (100): nº de átomos en un plano 2 átomos área del plano (f. de a) a2 nm2
d
a
a
Densidad planar (100) en la red cúbica centrada en las caras
r
d
a
2r
r
d/2
h
d
Densidad planar en el plano compacto octaédrico (111) en la red cúbica centrada en las caras
En el plano octaédrico (111):
Número de átomos = { + 3 - 2
Area del plano = d. h
d . h
d2 = h2 + (2 ) 2
h2 = d2 - de = 3d= = 3 a 2 2
tema 2 h = a V3 2
nº de átomos en un plano 2 área del plano (f. de a) = av2 .a V3 = 2 4 átomos a23 nm2
Red cúbica centrada en las caras (CCC): Ejemplo de cálculo de densidad
z
Ejemplo de cálculo de densidad
Cálculo de la densidad del Cu (ccc) conocido el parámetro de red obtenido por Difracción de Rayos-X.
p= n M a = 0,36 1 nm n = 4 at celda A a VN c
NA= 6,02214076 x 1023 mol-1/g
M a = 63,50 g /at - g
V c = a 3 = 47,05 x 10 -24 cm 3 celda
Sustituyendo en la densidad sale p = 8,98 g/cm3 (densidad teórica)
La densidad del Cu (ccc) es 8,96 g/cm3 a 20°℃ (experimental).
tema 2