Aminoácidos y Proteínas: Clasificación, Estructura y Propiedades
Diapositivas de Universidad Andres Bello sobre Aminoácidos y Proteínas (parte 1). El Pdf detalla la clasificación, estructura y propiedades de aminoácidos y proteínas, incluyendo conceptos como aminoácidos esenciales y el enlace peptídico, útil para estudiantes universitarios de Biología.
Ver más49 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
AMINOACIDOS Y PROTEINAS (PARTE 1)
Semana 2
Clase teórica donde se revisarán los siguientes conceptos:
- Los aminoácidos: clasificación, estructura, propiedades.
- Aminoácidos esenciales.
- Curva de titulación de los aminoácidos.
- El enlace peptídico.
- Estructura de proteínas: estructura secundaria, terciaria y cuaternaria.
- Clasificación de las proteínas.
- Proteínas conjugadas.Estructura de los aminoácidos
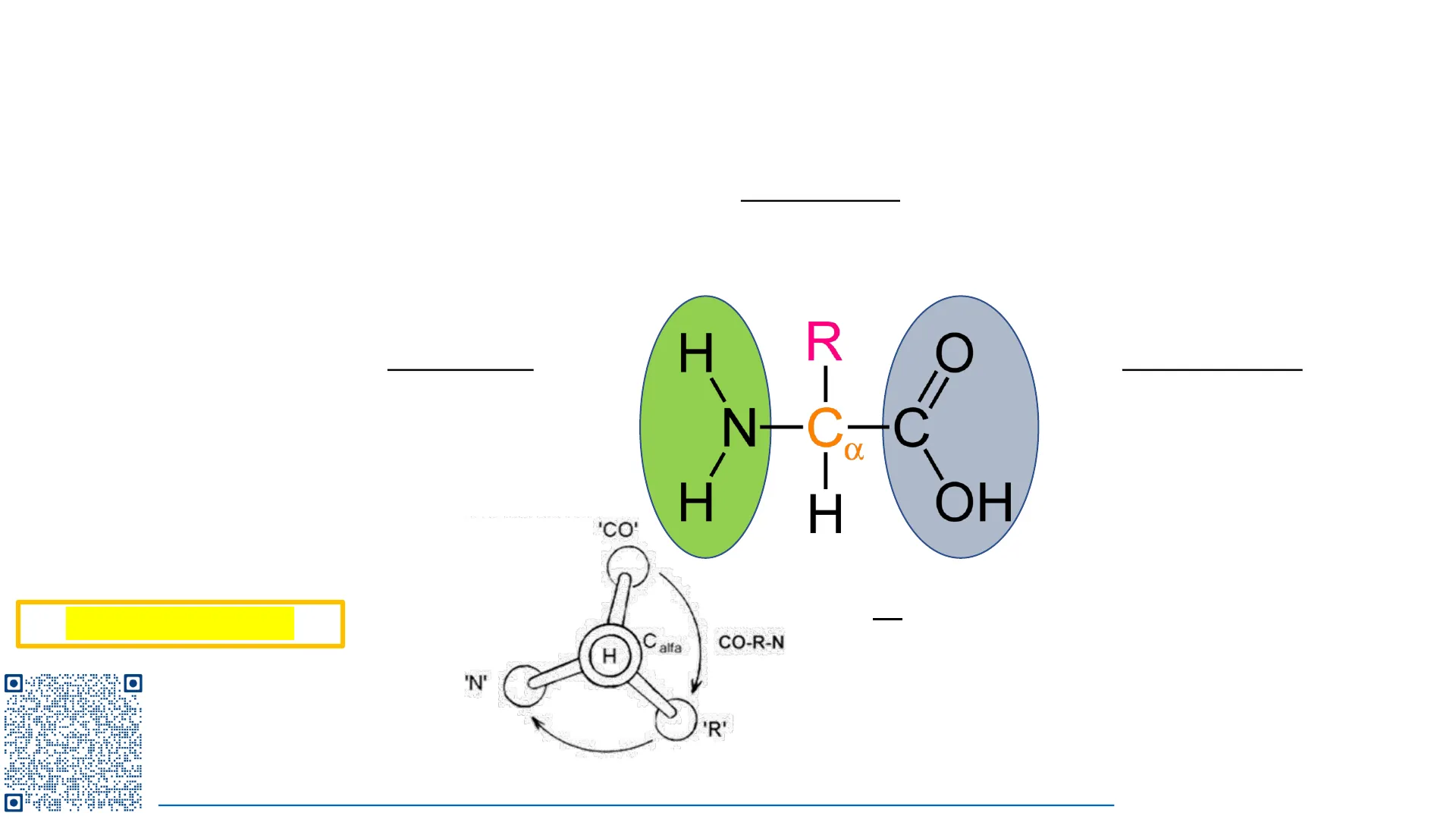
Estructura de los aminoácidos
Cadena lateral: · Otorga identidad (tamaño, carga, polaridad, reactividad) Grupo amino: H R C I · Ácido · Ionizable N -- C- a C / I H H OH 'CO' Ca: C alfa CO-R-N · Soporta a la cadena lateral 'N' 'R' Grupo Carboxilo: · Básico · Ionizable Jove: "Aminoácidos" H · Presenta quiralidad · L-a-aminoácidos https://app.jove.com/es/embed/player?id=11470&access=d1cd401b05&language=es&t=1&s=1&fpv=1
Aminoácidos esenciales
Aminoácidos esenciales en el adulto
En el adulto: Val Leu 1 Ile NH2 OH NH2 Triptófano Treonina Valina Lisina Leucina O -5 OH OH OH OH NH Isoleucina
Aminoácidos esenciales en el niño
En el niño (además): His Arg OH O 1 - OH OH OH NH2 NH, NH Met Phe Trp Thr Lys NH, HIN- NH2 Metionina Histidina Fenilanina O 0 O .N NH2
Estereoquimica de Aminoácidos
· El carbono-a constituye un centro quiral y genera un ordenamiento tetraédricos de los orbitales de enlace alrededor del carbono a · Para los aminoácidos es posible tener dos configuraciones diferentes, que son los enantiómeros que se caracterizan en ser imágenes especulares no superponibles · Isómeros Ópticos D, L COO + C H H3N CH3 L-Alanine COO- + H C NH3 CH3 D-Alanine · Los enantiómeros se pueden distinguir porque rotan de manera diferente el plano de la luz polarizada. · Todos los aminoácidos que forman parte de las proteínas son enantiómeros L. Algunos D-aminoácidos se encuentran en péptidos sintetizados fuera de los ribosomas 4
Propiedades espectroscópicas de los aminoácidos
Wavelength selector 10 Bandwidth (X1-X2) Light source Slit Sample tube or cuvette 40,000 20,000 10,000 5,000 Molar absorptivity, & Trp 2,000 1,000 Tyr 500 200 100 Phe 50 20 10 200 220 240 260 280 300 320 Wavelength (nm) - Todos los aminoácidos absorben a longitudes de onda que se encuentran en el IR. - Solo la Phe, Tyr y Trp absorben en la región del UV sobre los 250 nm, esta absorción en el UV es la base para la determinación de la concentración de una proteína. - Light- detecting photocell or phototube Meter
Modificaciones químicas de los aminoácidos
Hidroxilación
Hidroxilación OH O H2M OH NH2 5- hidroxi-lisina OH HO -NH 4- hidroxi-prolina
Glicosilación
Glicosilación ASN THR/SER
Metilación
Metilación N-metil-arginina COOH N-acetil-lisina N-metil-lisina COOH COOI HIN-C-H HIN-C-H HẠN-C-F CH2 CH2 CH2 CH CH CH2 CH CH2 CH2 NH CH2 CH2 C NH-FC-CH3 H2N N CH, 0
Puentes disulfuro
Puentes disulfuro 0 O H2N-CHC-OH CH2 H2N-CHC-OH CH2 SH S SH S CH2 H2N-CHC-OH CH2 H2N-CHC-OH Ö NH-CH3
Fosforilación
Fosforilación 00 ATP Quinasa ADP P Fosfatasa Proteína fosforilada Modificaciones de aminoácidos Proteína desfosforilada P. -0=
Aminoácidos presentes en ciertas proteínas
25-Hydroxylysine 4-Hydroxyproline y-Carboxyglutamic acid Pyroglutamic acid COOH 1 HN-C-H / 1 -C CH2 11 O C Ho CH HOOC COOH Aminoácidos presentes en ciertas proteínas. (c) COOH - CH3 NHỜ HO CH2 1 1 CH2-NH3 (CH2) 3 NHỜ CH2 N 1 H NHỊ CH2 CH2 1 y-Aminobutyric acid (GABA) HO-C-H NH N Histamine OH OH Epinephrine + 1 1 H3N-C-H HỌC CH2 C 0- - H OH CH2 1 CH2 1 CHOH 1 CH2 COOH 1 + H3N-C-H HN-C-H 1 1 - 1 Serotonin Un aminoácido (GABA) y tres derivados; todos neurotransmisores Lehninger: Principles of Biochemistry ( OMEGA 2009) CH2 1 NHẸ COOH 1 COOH
Estructura de los aminoácidos
Clasificación de los aminoácidos estandares
Clasificación de los aminoácidos estandares: Se realiza en base a las características de su CADENA LATERAL · Aminoácidos estandares: los 20 a- aminoácidos que componen las proteínas · Son codificados a través del código genético · Contienen un grupo funcional COOH y un grupo funcional amina NH2 . Se diferencian por la cadena lateral No polares polares Aromáticos Con carga positiva (básicos) Con carga negativa (ácidos ) Glicina Serina fenilalanina lisina Aspartato Alanina Treonina Tirosina arginina glutamato valina cisteína Triptófano histidina Leucina asparagina metionina glutamina isoleucina Prolina
Clasificación de los aminoácidos
Aminoácidos apolares o alifáticos
Aminoácidos apolares o alifáticos Grupos R apolares, alifáticos COO- COO COO COO- H -0 H3N-C-H + H2Ń CH 2 H CH3 H2Č- - CH2 CH CH3 CH3 Glicina Alanina Prolina Valina COO- COO- COO- H3N-C-H H3N-C-H H3N-C-H CH2 CH H-C-CH3 CH2 T CH2 CH2 CH3 CH3 CH3 S CH3 Leucina Isoleucina Metionina · Cadenas laterales alifáticas · A mayor tamaño, mayor hidrofobicidad · Participan en interacciones hidrofóbicas · Se posicionan hacia el interior de las proteínas Prolina: · Cadena lateral unida al Ca y al grupo amino · Aminoácido más rígido - H3N-C-H
Aminoácidos aromáticos
Clasificación de los aminoácidos Aminoácidos aromáticos COO COO- COO- Grupos R no polares, aromáticos - + + H3N-C-H H3N-C-H H3N-C-H - I - CH2 CH2 CH2 NH OH Fenilalanina Tirosina Triptofano 1 . 10 000 Triptófano Absortividad molar, M-1 cm-1 Tirosina 1000 100 Fenilalanina 10 200 250 300 Longitud de onda, nm · Poseen anillos aromáticos en su estructura · Los anillos aromáticos absorben luz ultravioleta (max. 280 nm) · Son hidrofóbicos · Pero Tyr y Trp pueden forman enlaces puentes de H - 1 +
Aminoácidos polares sin carga
Clasificación de los aminoácidos Aminoácidos polares sin carga · Poseen grupos funcionales en sus cadenas laterales, pero estos no se ionizan · Cadenas laterales débilmente polares · Son hidrofílicos · Se localizan en la superficie de las proteínas (en contacto con el medio acuoso · Forman enlaces puente de H entre ellos y con el agua Cisteína: · Grupo funcional sulfhidrilo (SH-) altamente reactivo . En condiciones oxidantes el grupo SH- reacciona con otro y forma un enlace covalente S-S (Puente disulfuro) Polar, uncharged R groups COO COO 1 HIN C H HIN-C-H HIN-C-H CH_OH H-C-OH CH. CH, SH Serine Threonine Cysteine COO COO HIN-C-H HẸN-C-H CH, CH2 CH 1 HIN 0 HẠN 0 Asparagine Glutamine ......
Aminoácidos polares con carga positiva (básicos)
Clasificación de los aminoácidos Aminoácidos polares con carga positiva; básicos Positively charged R groups COO COO COO 1 I + I + H3N-C-H H3N-C-H H3N-C-H CH2 I CH2 1 CH2 I CH2 I CH CH2 I CH2 C-N H NH 1 + +NH3 C=NH2 NH2 Lysine Arginine Histidine · Poseen grupos funcionales básicos en sus cadenas laterales · Pueden ionizarse y presentar carga positiva · Hidrofílicos · Se localizan en la superficie de las proteínas Histidina: · Puede intercambiar protones a pH fisiológico · Se localiza comúnmente en los sitios activos de enzimas CH2 I CH2 C-NH
Aminoácidos polares con carga negativa (ácidos)
Clasificación de los aminoácidos Aminoácidos polares con carga negativa; ácidos Negatively charged R groups COO- COO- + H3N-C-H + H3N-C-H CH2 COO- CH2 I CH2 COO- Aspartate Glutamate · Poseen grupos funcionales ácidos en sus cadenas laterales · Presentan carga negativa a PH fisiológico · Hidrofílicos · Se localizan en la superficie de las proteínas · Interacciones puentes salinos y puentes de H
Comportamiento ácido-básico de los Aminoácidos
Garrett & Grisham: Biochemistry, 2/e Figure 4.6 (ionización de los grupos alfa-amino y alfa-carboxilo) pH 1 Net charge +1 R + o N o pH 7 Net charge 0 R + N O pH 13 Net charge -1 R - O COOH H+ COO- H+ COO- 1 1 1 1 H3N-C-H HON-C-H 1 R R R Cationic form Zwitterion (neutral) Anionic form pKa = 2 pKa = 9,5 Saunders College Publishing 14 N H3N-C-H 1
Propiedades ácido-base de los Aminoácidos
· El grupo amino, el grupo carboxilo y los grupos R ionizables de los aa, permiten que actúen como ácidos débiles o bases débiles. Debido a su comportamiento anfótero, los aminoácidos tienden a neutralizar las variaciones de pH del medio, ya que pueden comportarse como un ácido o una base, liberando o retirando protones del medio. Son buffer o tampones, controlan pequeños cambios de pH. H 1 R-C-COOH - +NH3 H 1L R-C-COO-+ H+ 1 En este caso actúa como dador de H+ - +NH3 H · Como pueden presentar diferentes cargas dependiendo del pH de la solución en la que se encuentra, cuando el aminoácido tiene carga neta 0, se encuentre en forma del ion bipolar o zwitterion, R-C-C=0 H3N+ 0- Zwitterionic form
Propiedades y convenciones de los aminoácidos comunes
TABLE 3-1 Properties and Conventions Associated with the Common Amino Acids Found in Proteins pK_ values Amino acid Abbreviation/ symbol M. pK1 (-COOH) PK2 (-NH;) pKR (R group) pl Hydropathy index* Occurrence in proteins (%)+ Nonpolar, aliphatic R groups Glycine Gly G 75 2.34 9.60 5.97 -0.4 7.2 Alanine Ala A 89 2.34 9.69 6.01 1.8 7.8 Proline Pro P 115 1.99 10.96 6.48 1.6 5.2 Valine Val V 117 2.32 9.62 5.97 4.2 6.6 Leucine Leu L 131 2.36 9.60 5.98 3.8 9.1 Isoleucine lle 1 131 2.36 9.68 6.02 4.5 5.3 Methionine Met M 149 2.28 9.21 5.74 1.9 2.3 Aromatic R groups Phenylalanine Phe F 165 1.83 9.13 5.48 2.8 3.9 Tyrosine Tyr Y 181 2.20 9.11 10.07 5.66 -1.3 3.2 Tryptophan Trp W 204 2.38 9.39 5.89 -0.9 1.4 Polar, uncharged R groups Serine Ser S 105 2.21 9.15 5.68 -0.8 6.8 Threonine Thr T 119 2.11 9.62 5.87 -0.7 5.9 Cysteine Cys C 121 1.96 10.28 8.18 5.07 2.5 1.9 Asparagine Asn N 132 2.02 8.80 5.41 -3.5 4.3 Glutamine Gin Q 146 2.17 9.13 5.65 -3.5 4.2 Positively charged R groups Lysine Lys K 146 2.18 8.95 10.53 9.74 -3.9 5.9 Histidine His H 155 1.82 9.17 6.00 7.59 -3.2 2.3 Arginine Arg R 174 2.17 9.04 12.48 10.76 -4.5 5.1 Negatively charged R groups Aspartate Asp D 133 1.88 9.60 3.65 2.77 -3.5 5.3 Glutamate Glu E 147 2.19 9.67 4.25 3.22 -3.5 6.3 DAD ZAINO ELLO Además de los dos grupos ionizables (COOH y NH3+), 7 aminoácidos tienen un tercer grupo ionizable en su grupo R pKa1: valor del pKa del grupo carboxilo pKa2: valor de pKa grupo amino pKr: valor de pka del grupo R ionizable
Estado de protonación de los aminoácidos según el pH
· Los aminoácidos a pH= 7 su grupo a-carboxilo se encuentra como base conjugada (COO-) y el grupo a- amino se encuentra como acido conjugado (NH3+) · Los aminoácidos se pueden comportar como acido a base, cambian su estado de protonación a medida que cambia el pH de la solución R R H+ R H +H3N COOH H+ H+ - Zwitterionic form Both groups deprotonated Concentration Both groups protonated I 0 4 6 8 10 12 14 pH pKa COOH pKa NH3+ ¿Qué estructura del aa predomina según el pH? Cuál es el pH cuando: [A ] = [HA] usando pH = pKa + log [A ] [HA] log [A-] = log 1 = 0 [HA] pH = pKa H+ H H 1 +H3N COO- H2N COO-