Tema 4: Disoluciones y Diluciones, una Presentación de Linkia Fp
Diapositivas de Linkia Fp sobre Tema 4: Disoluciones y Diluciones. El Pdf, para Bachillerato en Química, explora la materia, los átomos, las mezclas heterogéneas y homogéneas, y los componentes de las disoluciones, como el solvente y el soluto.
Ver más62 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Linkia FP
Disoluciones y Diluciones
La Materia y sus Componentes
La materia
- Ocupa espacio y tiene masa
- La unidad fundamental de la materia es el átomo
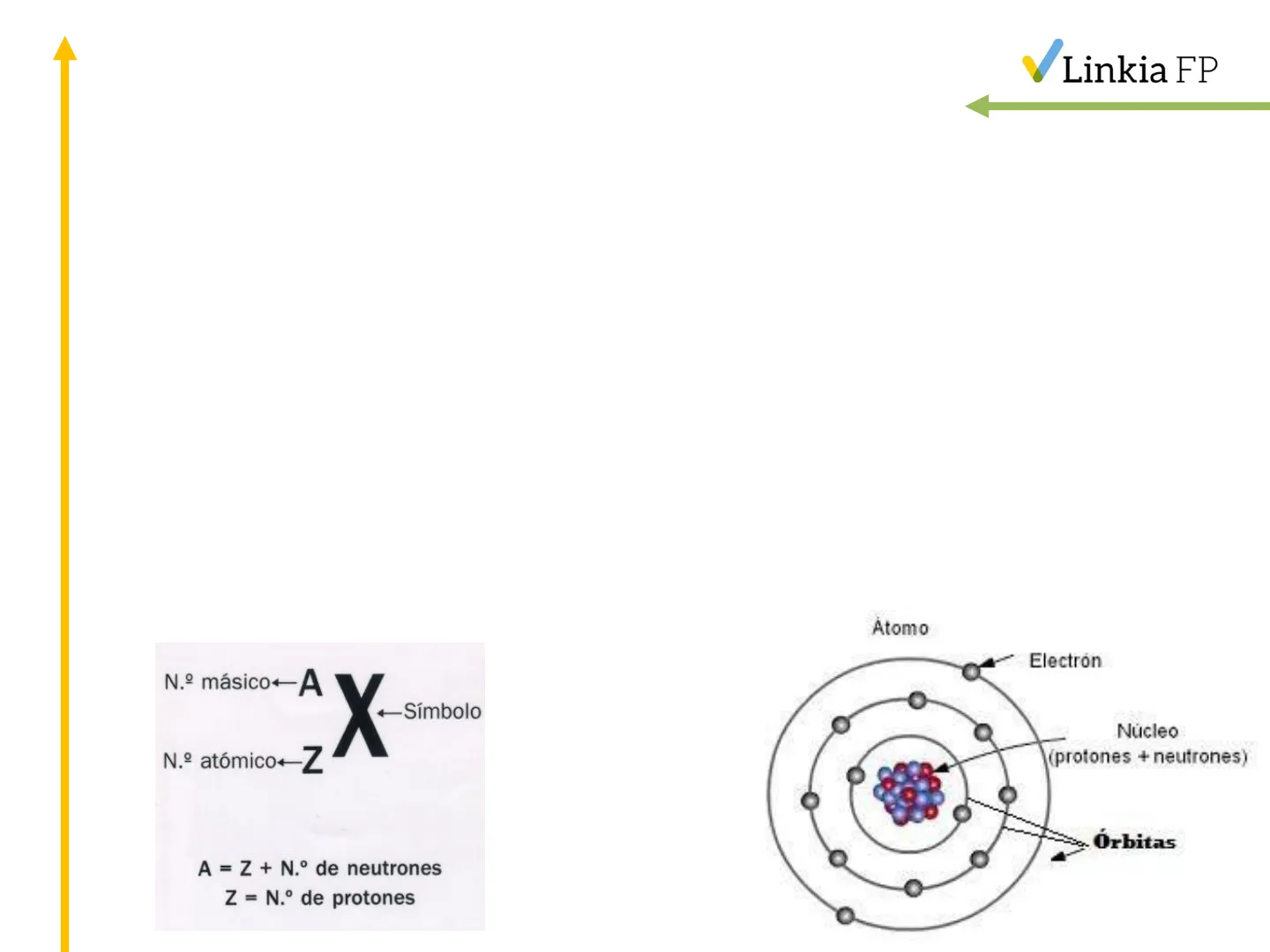
- El átomo está formado por:
- Neutrones: forman parte del núcleo sin carga
- Protones: forman parte del núcleo de carga positiva
- Electrones: giran en orbitales y dan carga negativa
Se utiliza la letra Z para llamar al número de protones. El número A es lo que constituye el número de masa del átomo. N.º másico+-A N.º atómico+-Z X +Símbolo Atomo Electrón Núcleo (protones + neutrones) Órbitas A = Z + N.º de neutrones Z = N.º de protonesLa materia
Linkia FP
- Los átomos combinados forman moléculas
- Molécula diatómica, dos átomos O2
- Molécula triatómica, tres átomos H2O
- Molécula tetratómica, cuatro átomos P4
- Redes cristalinas, los átomos de un tipo se encuentran rodeados por los de otro Na Na Na CI CI Na CI CI Na Na CI Na Na CI CI Na
Diferentes Formas de la Materia
Linkia FP
- La materia puede presentarse como sustancias puras o mezclas
- Tendrán diferentes propiedades dependiendo de su composición Sistemas materiales Sustancias puras (1 solo componente) Mezclas (dos o más componentes) Simples Compuestos dos o mas tipos de átomos Homogéneas no se distinguen componentes Heterogéneas se distinguen componentes
El Concepto de Mol
Linkia FP Diferentes formas de la materia · Al entrar en contacto dos sustancias estas reaccionan y origina otra sustancia diferente (reacción química)
- Mol: es la manera de medir la cantidad de materia. Un mol equivale a 6,022x 1023 unidades de cualquier materia EL CONCEPTO DE MOL 23 1 mol = 6,02 x 10 UNIDADES Generalmente se usa para ÁTOMOS, MOLÉCULAS, ELECTRONES 23 1 mol átomos C = 6,02 x 10 átomos C 1 mol moléculas H2O = 6,02 x 10 moléculas H2O 0 1 mol e = 6,02 x 10"e"
Clasificación de Sustancias Puras
Linkia FP Sustancias puras
- Están formadas por un solo tipo de moléculas
- Se pueden clasificar en:
- Sustancias simples o elementos (P4, O2, O3)
- Formadas por un solo tipo de átomo
- No pueden descomponerse en sustancias más simples
- Pueden encontrarse los átomos aislados o formando moléculas
- Compuestos puros (NH3, H2O)
- Formados por un solo tipo de molécula pero esta está formada por mas un de un tipo de átomo
- Podrían a su vez descomponerse en otros elementos más sencillos
Mezclas o Sistemas
Linkia FP Mezclas o sistemas
- Formados por varios componentes puros que no se combinan entre sí quimicamente
- Cada componente mantiene sus propiedades las cuales se suman
- No tienen composición química definida y podemos separa sus componentes mediante métodos sencillos
- Según el número de fases pueden ser:
- Homogéneas (una sola fase)
- Heterogéneas (dos o más fases)
Mezclas Heterogéneas
Linkia FP Mezclas heterogéneas En estas mezclas hay al menos dos fases:
- La fase dispersa o interna: también llamada soluto, componente que esta en menor proporción
- La fase dispersante o externa: también llamada disolvente componente que está en mayor proporción Agua y aceite
Clasificación de Sistemas Heterogéneos
Mezclas heterogéneas Linkia FP Clasificación de los sistemas heterogéneos Según el estado de agregación de cada fase:
| FASE EXTERNA (DISOLVENTE) | FASE INTERNA (SOLUTO) | EJEMPLO |
|---|---|---|
| Gas | Aire | Gas |
| Líquido | Niebla | Sólido |
| Humo | Gas | Oxígeno en agua |
| Líquido | Líquido | Alcohol en agua |
| Sólido | Agua con arcilla | Gas |
| Burbujas de aire en una piedra | Sólido | Líquido |
| Intrusión de agua en las rocas | Sólido | Aleaciones |
Clasificación de Sistemas Heterogéneos por Tamaño de Partículas
Linkia FP Mezclas heterogéneas Clasificación de los sistemas heterogéneos Según el tamaño de las partículas:
- Dispersiones macroscópicas o groseras: las partículas del soluto son mas grandes de 50um y sus fases tienden a separarse de manera espontánea.
- Dispersiones finas: las partículas del soluto tienen un tamaño entre 0,1 y 50um y solo pueden verse al microscopio
- Dispersiones coloidales o coloides: las partículas de la fase interna tiene entre 0,001 y 0,1um. Tienen aspecto de sistema homogéneo y no pueden observarse con un microscopio óptico.
Mezclas Homogéneas o Disoluciones
Mezclas homogéneas o disoluciones Linkia FP
- Son sistemas muy estables
- Sus componentes no pueden separarse mediante procesos sencillos
- Si pueden separarse mediante procesos que alteren el estado de agregación de alguna de las fases como la destilación
Componentes de las Disoluciones
Linkia FP Mezclas homogéneas o disoluciones Componentes de las disoluciones:
- Disolvente: componente con el mismo estado de agregación que la disolución resultante. Si ambos tienen el mismo estado será el que esté en mayor proporción
- Soluto: componente con distinto estado de agregación que la disolución resultante. Si ambos componentes tienen el mismo estado será el que esté en menor proporción. Las más usadas en laboratorio son las (soluto/disolvente) líquido/líquido y sólido/líquido.
Solubilidad en Disoluciones
Mezclas homogéneas o disoluciones Linkia FP Solubilidad
- Es una magnitud que indica la capacidad que tiene un disolvente para disolver una sustancia.
- Informa de si es posible o no hacer una disolución.
- Para expresar la solubilidad en términos cuantitativos se usa el coeficiente de solubilidad.
- Se define como la máxima cantidad de soluto que puede disolverse en 100g o 100 ml de un determinado disolvente a una temperatura determinada.
Factores que Afectan la Solubilidad
Mezclas homogéneas o disoluciones Linkia FP Solubilidad
- La solubilidad depende de varios factores, características del soluto, del solvente, la presión, la temperatura.
| FACTOR | CÓMO AFECTA A LA SOLUBILIDAD |
|---|---|
| Temperatura | A mayor temperatura mayor solubilidad |
| Presión | A mayor presión mayor solubilidad |
| Presencia de otras partículas | A más presencia menor solubilidad |
Solubilidad y Temperatura
Mezclas homogéneas o disoluciones Linkia FP Solubilidad y temperatura La temperatura es el principal factor que afecta a la solubilidad. Al aumentar la temperatura las moléculas de la disolución se mueven más y esto favorece la dispersión. 100 90 NaNO3 Solubility (g of salt in 100 g H2O) 80 70 CaCl2 60 Pb(NO3)2 KNO3 50 KCI 40 NaCl 30 KCIO3 20 10 Ce2(SO4)3 0 0 10 20 30 40 50 60 70 80 90 100 Temperature (℃) Los coeficientes de solubilidad a diferentes temperaturas en una tabla obtendremos las curvas de solubilidad K2Cr2O7
Tipos de Disolución según Concentraciones
Mezclas homogéneas o disoluciones Linkia FP Tipos de disolución según las concentraciones
- Diluidas: son aquellas en las que la concentración de soluto es mucho menor que el coeficiente de solubilidad
- Concentradas: son aquellas en las que la concentración de soluto está próxima al coeficiente de solubilidad Diluido Concentrado
Clasificación de Disoluciones por Saturación
Mezclas homogéneas o disoluciones Linkia FP Tipos de disolución según las concentraciones
- Disolución no saturada: la concentración de soluto es menor al coeficiente de solubilidad por lo que admite más soluto.
- Disolución saturada: contienen la cantidad máxima de soluto que admite, tienen la concentración de soluto correspondiente al coeficiente de solubilidad.
- Disolución sobresaturada: la cantidad de soluto es superior a la que corresponde al coeficiente de solubilidad a esa temperatura.
Propiedades de las Disoluciones
Mezclas homogéneas o disoluciones Linkia FP Propiedades de las disoluciones
- Propiedades físicas de una disolución que no dependen de la naturaleza del soluto si no del número de partículas de soluto que hay presentes en la disolución.
- No dependen de las características del disolvente.
- Son iguales para cualquier disolución.
- La variación en estas propiedades permite calcular la concentración de una disolución.
Ecuaciones de Congelación y Ebullición
Mezclas homogéneas o disoluciones Linkia FP Ecuaciones T° congelación y punto de ebullición · El descenso en el punto de congelación y el aumento en el punto de ebullición están relacionados con la concentración de una disolución mediante: Tc = Kc x molalidad Descenso en el punto de congelación ATe = Ke x molalidad Aumento en el punto de ebullición Kc y Ke son constantes dadas y son características de cada disolvente. Molalidad: es la concentración de una disolución. Se mide en mol/Kg.
Cálculo de Temperatura de Ebullición
Linkia FP Mezclas homogéneas o disoluciones Ecuaciones Tº congelación y punto de ebullición Si la constante de ebullición del agua es de 0,52 ℃ Kg/mol y el agua hierve a 100 ℃ calcula a qué temperatura hervirá una disolución de 25g de sal (NaCl) en 100 ml de agua. Dato: Masa molecular de la sal 58,5 g/mol y 1 Kg = 1000 ml ATe = Ke x molalidad sustituimos los datos ATe = 0,52 x molalidad Molalidad NaCl= moles NaCl/Kg disolvente= moles NaCl / 0,1Kg agua Moles de NaCl= si un mol pesa 58,5g en 25g ... x=25/58,5= 0,43 moles NaCl y este dato lo sustituyo en la molalidad Molalidad NaCl= 0,43 moles de NaCL/ 0,1Kg agua = 4,3 mol/Kg Sustituyo en la primera ecuación: ATe = 0,52℃ Kg/molx 4,3 mol/Kg = 2,24 ℃ La temperatura de ebullición de la disolución será de 102,24 ℃ Ya que la cantidad añadida de sal ha subido la temperatura de ebulición del agua 2,24 ℃
Presión Osmótica
Mezclas homogéneas o disoluciones Linkia FP Presión osmótica La relación entre la presión osmótica y la concentración de soluto viene dada por la siguiente ecuación: TXV = nxRxT Tt es la presión osmótica V es el volumen en litros n es el número de moles de soluto R es la constante universal de los gases = 0,082 atm L/mol K
Tipos de Disoluciones por Presión Osmótica
Mezclas homogéneas o disoluciones Linkia FP Presión osmótica Según la presión osmótica tenemos tres tipos de disoluciones:
- Disolución isotónica: tiene una presión osmótica igual a la de referencia. No hay paso de disolvente.
- Disolución hipotónica: tiene una presión osmótica inferior a la de referencia. Hay paso de disolvente a la disolución de referencia
- Disolución hipertónica: tiene una presión osmótica superior a la de la disolución de referencia. Hay paso de disolvente desde la disolución de referencia.
Cálculo de Presión Osmótica
Mezclas homogéneas o disoluciones Linkia FP Presión osmótica ¿Qué presión osmótica ejercerá una disolución de 1,8g de glucosa en 100 ml de agua a 27 °℃? Datos: Masa molecular de la glucosa 180 g/mol TTXV = nxRxT despejamos la presión osmótica TT = nxRxT V Volumen: 100mL = 0,01 L Buscamos n: 1,8 g de C6H12O6 / 180g en un mol = 0,01 mol de C6H12O6 Temperatura en Kelvin= Temperatura en Celsius +273 = 27 + 273 = 300 K Sustituimos en la fórmula principal: T = 0,0 1mol glucosax0,082x300K = 2,46 atm 0,1 L La presión osmótica será de 2,46 atm = 249259,5 Pa
Reacciones Químicas
Mezclas homogéneas o disoluciones Linkia FP Reacciones químicas · Es la transformación de una sustancia inicial (reactivo) en otras sustancias llamadas productos. · Las moléculas que forman los reactivos deben romper los enlaces de los átomos que las forman y crear enlaces nuevos en la nueva molécula. · Se representan mediante ecuaciones químicas los reactivos se colocan a la izquierda y los productos a la derecha. · Entre producto y reactivo se coloca una flecha
- reacción irreversible
- reacción reversible