Silicatos: Cuarzo, feldespatos y zeolitas en Ciencias, Universidad
Documento de Universidad sobre Silicatos: Cuarzo, feldespatos, zeolitas. El Pdf explora los silicatos, minerales abundantes en la corteza terrestre, con un enfoque en cuarzo, feldespatos y zeolitas, describiendo su estructura, clasificación y propiedades, así como sus usos industriales en la producción de vidrio y cerámica.
Ver más9 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Generalidades y clasificación de los silicatos
Los silicatos son los minerales más abundantes en la corteza terrestre. Son la clase de más importancia geológica por ser muchos de ellos Minerales petrogenéticos, es decir, los minerales que constituyen parte fundamental de algunos tipos de rocas.
Todos los silicatos están compuestos por silicio y oxígeno, y pueden estar acompañados de otros elementos entre los que destacan aluminio, hierro, magnesio, calcio, sodio y potasio. Su unidad estructural básica es un tetraedro SiO44- donde el Si4+ ocupa el centro del tetraedro y los O2- los vértices.
El enlace Si-O puede clasificarse como un 50% iónico - 50% covalente. Es decir, aunque el enlace es debido en parte a la atracción de unidades iónicas de cargas contrarias, implica también el reparto de electrones y la interpenetración de las nubes electrónicas de los iones, orientados según la disposición de los orbitales híbridos sp3 del Si.
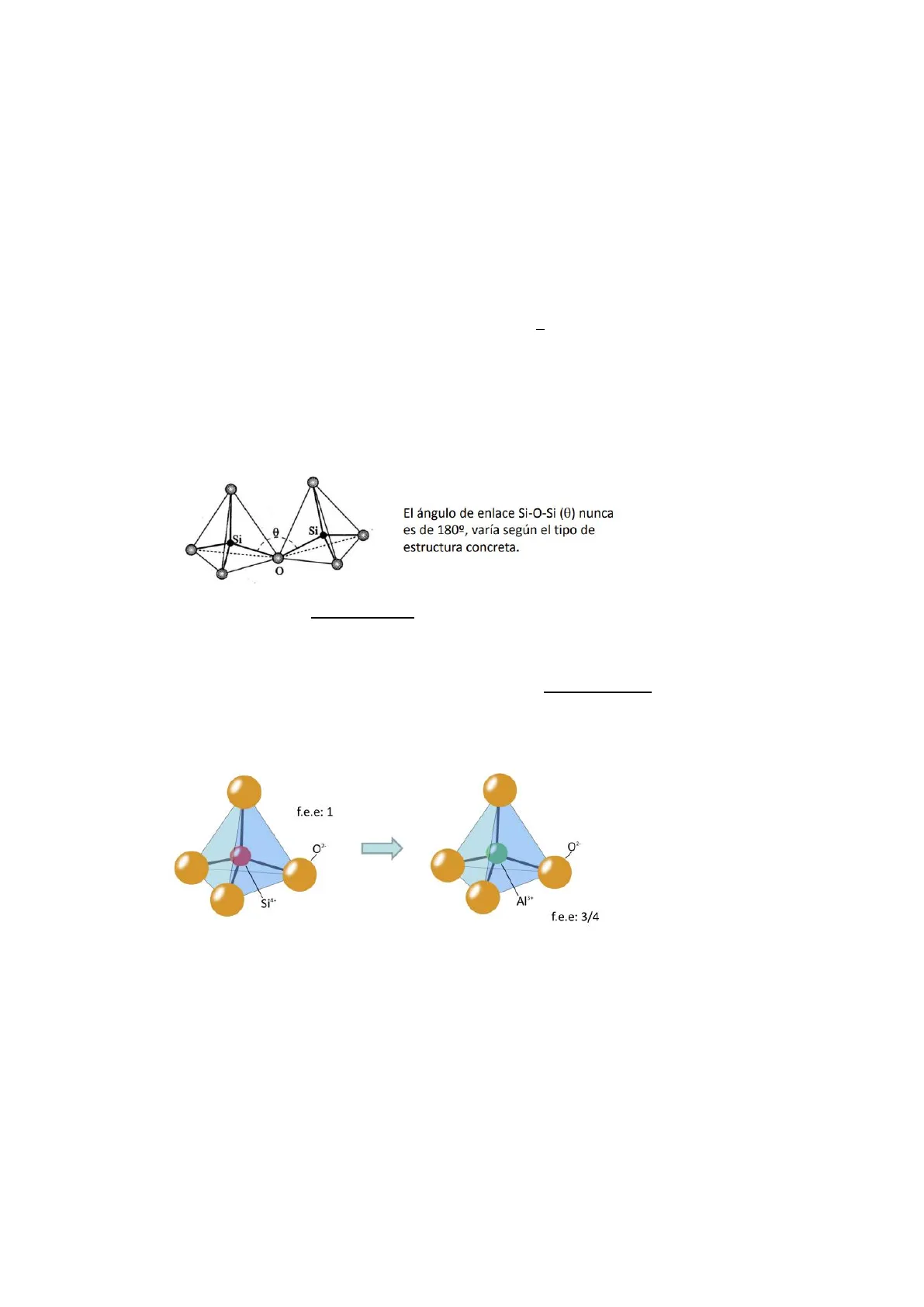
Si e Si O El ángulo de enlace Si-O-Si (0) nunca es de 180º, varía según el tipo de estructura concreta.
El grupo [SiO4]4- es mesodesmico. Es decir: f.e.e = Z+/NC = Z-/2, siendo Z+ la carga del catión, NC el número de coordinación y Z- la carga del anión: f.e.e. = 4+/4 = 1 = 2-/2. Por lo tanto, la f.e.e es igual a la mitad de la carga del anión, lo que implica que el oxígeno de un vértice puede enlazarse con otro Si y producir la polimerización.
En la estructura de muchos silicatos algunos átomos de Si4+ pueden ser sustituidos por átomos de Al3+. En lugar de grupos [SiO4] 4- tenemos grupos [AlO4] 5- .
f.e.e: 1 0 0 Si4+ A13+ f.e.e: 3/4
Si hay sustitución de parte del Si4+ por Al3+ en los tetraedros, la carga negativa adicional que se genera en la unidad tetraédrica se compensa con la entrada en la estructura de otros iones como alcalinos, alcalinotérreos, aluminio, hierro o magnesio. Esta sustitución de Al por Si da origen a numerosos minerales que se denominan, en conjunto, aluminosilicatos.
Clasificación de los silicatos
La unión entre tetraedros, polimerización, se hace compartiendo los oxígenos de los vértices. Un tetraedro puede compartir: ninguno, uno, dos, tres o sus cuatro oxígenos. Los minerales de la clase silicatos se clasifican en las subclases:
SUBCLASE DESCRIPCION
nesosilicatos Tetraedros aislados
sorosilicatos Tetraedros unidos en parejas
ciclosilicatos Tetraedros unidos formando anillos
inosilicatos Tetraedros unidos formando cadenas
filosilicatos Tetraedros unidos formando láminas
tectosilicatos Tetraedros unidos formando armazones tridimensionales
Nesosilicatos: Silicatos con tetraedros aislados
Los tetraedros no comparten vértices. Están unidos entre sí por medio de cationes con los que se unen por enlaces iónicos. No hay sustitución de Si por Al en los tetraedros.
UNIDAD ESTRUCTURAL Fórmula [SiO4]4- Relación Si:O 1:4 Nº de vértices compartidos 0 Haward pointing tetrahedips partiwend pointing tetrahedron Islion
Sus estructuras, de cada mineral en concreto, dependen del tamaño y carga de los cationes intersticiales.
- Olivinos. Hay olivinos magnesicos y ferrosos. Forsterita (Mg2SiO4) y Fayalita (FezSiO4) son isomorfos y presentan solución sólida completa. En ocasiones se utilizan como gemas.
- Granates. Hay diferentes variedades. El Almandino (Fe3Al2Si3O12) es uno de los más abundantes. Tienen utilidad como abrasivos.
Sillimanita-Andalucita-Cianita (Al2SiO5). Son polimorfos. Se utilizan como refractarios en la industria cerámica.
Sorosilicatos: Tetraedros formando parejas
Los grupos tetraédricos dobles comparten un oxígeno en el vértice común. No hay sustitución de Si por Al en los tetraedros.
UNIDAD ESTRUCTURAL Fórmula [Si2O2]6- Ca Relación Si:O 2:7 Al Nº de vértices compartidos 1 Si 0 H
Las parejas de tetraedros se unen entre si mediante cationes intersticiales.
- Epidota Ca2(Fe,Al)Al20(OH)(SiO4)(Si2O7). La estructura de la epidota tiene grupos de 2 tetraedros [(Si2O7)] y también tetraedros aislados.
Ningún mineral del grupo sorosilicatos tiene interés industrial.
Ciclosilicatos: Tetraedros unidos formando anillos
Existen varias posibles combinaciones cíclicas cerradas de 3, 4 o 6 tetraedros. Sin sustitución de Si por Al en los tetraedros o con muy escasa sustitución.
UNIDAD ESTRUCTURAL Fórmula [SiO3]2- Relación Si:O 1:3 Nº de vértices compartidos 2 pří
Los anillos se apilan en la dirección del eje c, uniéndose mediante otros cationes y formando "columnas". Las columnas, a su vez, se unen entre si mediante otros cationes. Cristales con hábitos columnares.
- Turmalina (anillo de 6T). Se utiliza como gema y en la industria electrónica por ser piezoeléctrica (simetría 3m). (Na, Ca)(Al,Fe,Li)(AI,Mg,Mn)6(BO3)3(Si6O18) . (OH,F)
- Berilo (anillo de 6T). Se utiliza como fuente de Be para metalurgia y como gema (esmeralda). (Be3Al2Si6O18)
Inosilicatos: Tetraedros enlazados formando cadenas
Con o sin sustitución de Si por Al. Existen inosilicatos en los que se reconocen cadenas sencillas e inosilicatos formados por cadenas dobles.
UNIDAD ESTRUCTURAL UNIDAD ESTRUCTURAL Fórmula [SiO3]2- Fórmula [Si2011]6- Relación Si:O 1:3 Relación Si:O 4:11 Nº de vértices compartidos 2 Nº de vértices compartidos 2y 3
Las cadenas se unen entre si mediante otros cationes.
- En las cadenas sencillas, dos de los cuatro oxigenos de cada T de SiO4 son compartidos con los tetraedros vecinos, por lo que la relación Si:O es 1:3.
→ Inosilicatos de cadena simple: (Ca,Na)(Mg,Fe,Al,Ti)(Si,Al)2O6
- Piroxenos (p.e. Augita): Excepto la espodumena LiAlSi2O6, ningún mineral del grupo tiene un interés industrial destacable.
→ Inosilicatos de cadena doble: Ca2(Mg,Fe)5SigO22(OH)2
- Anfíboles (p.e. Actinolita). Solo los anfíboles fibrosos tienen interés industrial por su uso en la fabricación de amianto.
Filosilicatos: Tetraedros de SiO4 unidos formando capas
UNIDAD ESTRUCTURAL Fórmula [Si2O5]2- Relación Si:O 2:5 Nº de vértices compartidos 3
En las capas tetraédricas, tres de los cuatro oxígenos de cada T están compartidos con T vecinos, resultando una relación Si:O = 2:5. Todos los vértices no compartidos apuntan en la misma dirección.
- En las cadenas dobles, la mitad de los T comparten 2 oxígenos y la otra mitad comparten 3 oxígenos. La relación Si:O es 4:11.
Las capas se unen mediante cationes en coordinación octaédrica. Hábitos laminares y una familia de exfoliación bien desarrollada perpendicular al eje c. Pueden, o no, presentar sustitución de Si por Al en las capas T.
- Las láminas de mica moscovita KAI2(Si3AI)O10(OH)2 se utilizan en la industria electrónica como aislante electrico.
- El talco Mg3Si4O10(OH)2 es un mineral que se usa en la industria del papel.
Tectosilicatos: Tetraedros unidos formando una red tridimensional continua
UNIDAD ESTRUCTURAL Fórmula [SiO2]º Relación Si:O 1:2 Nº de vértices compartidos 4
Todos los T comparten sus 4 vértices.
- Si no hay sustitución de Si por Al, la estructura tiene composición SiO2. Ejemplo: cuarzo.
- Si hay sustitución de Si por Al, el exceso de carga negativa se neutraliza por la entrada de otros cationes en la estructura. Ejemplos: feldespatos y zeolitas.
Cuarzo
Características del cuarzo
Fórmula: SiO2. Clasificación: tectosilicato. Sistema trigonal (32) en su forma de baja temperatura (cuarzo a). Coloraciones variadas. Transparente a translucido. Dureza alta (7 en la escala de Mohs), que se deriva de su estructura. Piezoeléctrico.
El interés industrial del cuarzo se basa tanto en sus propiedades físicas (que dependen de su estructura) como en su composición química.
El cuarzo es un mineral muy común y abundante en la naturaleza, debido a que aparece en casi todos los tipos de rocas:
- Rocas sedimentarias: abundante en areniscas y lutitas, frecuente en otras rocas.
- Rocas ígneas de composición ácida: granitos y riolitas.
- Rocas metamórficas en SIO2: cuarcitas, pizarras y gneises.
Además, puede presentar diferentes variedades macrocristalinas:
Cristal de roca.** Cuarzo ahumado. * Cuarzo amatista. En agregados masivos en filones o vetas. Material granular detrítico: Arenas siliceas.
Usos industriales del cuarzo
Las variedades macrocristalinas de cuarzo, como el cristal de roca, se pueden tallar para aprovechar sus propiedades piezoeléctricas, aunque para este uso es más frecuente el uso de cristales de cuarzo sintéticos.
La piezoelectricidad es una propiedad que presentan los monocristales de algunos minerales con ejes polares (sin centro de simetría), como el cuarzo o la turmalina y supone que al aplicar presión al cristal se genera una carga eléctrica. O, a la inversa, al aplicar una corriente eléctrica entre sus caras, se genera una oscilación (vibración) del cristal. Esta propiedad tiene múltiples aplicaciones tecnológicas: encendedores, relojes de cuarzo y transductores (sensores de presión, micrófonos, altavoces, atomizadores de fluidos ... ).
Arenas silíceas
Las arenas siliceas están formadas principalmente por granos de cuarzo. Tienen más del 95% de SiO2, el resto son impurezas (óxidos de hierro y/o titanio u otros minerales). Se pueden purificar consiguiendo que el contenido en sílice sea ~99.99% (flotación, separación magnética, lavados ácidos ... ).
Para algunos usos deben ser muy puras y con granulometría fina y homogénea (>90% entre 125-500 µ).
Usos industriales de las arenas silíceas
- Son la materia prima imprescindible para la fabricación del vidrio común.
- Se usan en la industria cerámica como componentes de los vidriados.
- Se utilizan como abrasivo.
Mezcladas con cemento constituyen el mortero de construcción.
- Se utilizan como relleno de filtros de agua.
- Son componentes de arenas para elaborar moldes para fundición.
- Materia prima para la fabricación de cuarzo sintético.
→ Producción de vidrio común (calizo o sodocálcido):
- Mezcla de arenas siliceas con minerales que aporten carbonato de sodio y carbonato de calcio (calcita): 65% SiO2 + 25% Na2CO3 + 10% CaCO3
- Fusión a ~1500℃ con liberación de CO2. La mezcla fundida se compone de: 75% SiO2 + 18% Na2O + 7% CaO
- Conformado del producto a unos 800-1000ºC.
- Enfriamiento.
- ADITIVOS: Durante la fabricación del vidrio se pueden añadir a la mezcla una gran variedad de compuestos para obtener un vidrio con las características deseadas, entre otros:
- Feldespatos alcalinos: actúan como fundentes y estabilizan el vidrio al aportar Al2O3.
- Compuestos de boro, para incrementar la resistencia al ataque químico y la resistencia al choque térmico (vidrio de borosilicato, p.e. Pyrex).