Silicatos Filisilicatos: estructura, clasificación y propiedades
Documento de Universidad sobre Silicatos Filisilicatos: estructura, clasificación y propiedades. El Pdf describe la estructura, clasificación y propiedades de los filosilicatos, incluyendo illita, esmectitas y minerales arcillosos fibrosos, útil para estudiantes de Ciencias.
Ver más8 páginas
Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Generalidades y clasificación de filosilicatos
La subclase filosilicatos comprende un número importante de minerales. Aparecen en todo tipo de rocas: ígneas, sedimentarias y metamórficas. Los filosilicatos son componentes mayoritarios de suelos y rocas sedimentarias. En su estructura se identifican capas continuas de tetraedros.
- Hábito hojoso.
- Exfoliación en (001).
Son aluminosilicatos hidratados.
Estructura de los filosilicatos
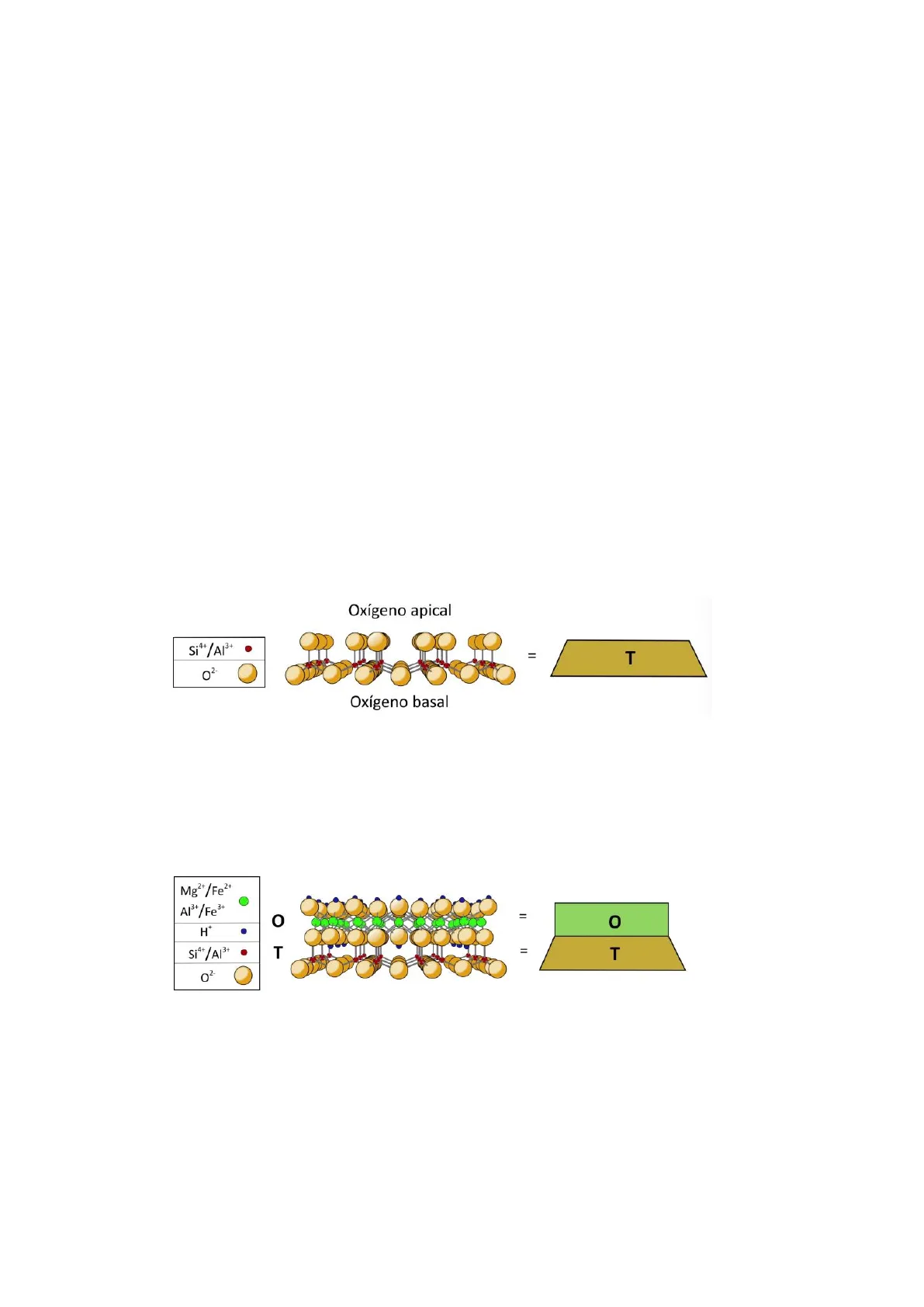
En las capas de tetraedros o capas tetraedricas los cationes T (Si4+ o Al3+) se coordinan con 4 oxígenos:
- Tres de ellos son compartidos con otros tetraedros, están en el mismo plano. Se les llama oxígenos basales.
- El cuarto átomo de oxígeno no está compartido con los otros tetraedros. Se les llama oxígenos apicales.
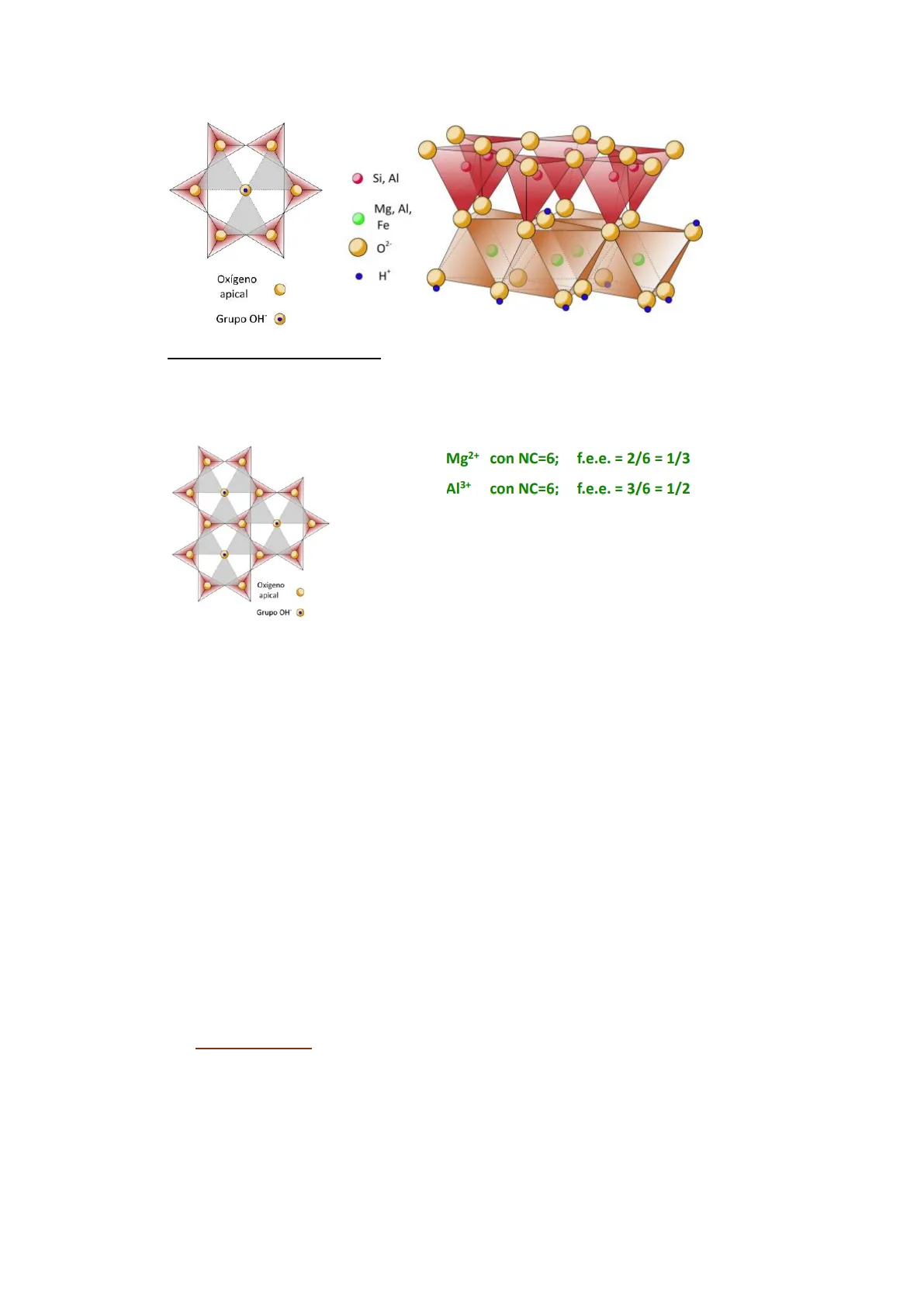
Oxígeno apical Si4+/AI34 T ญ่ O Oxígeno basal Las capas tetraedricas se unen entre si mediante cationes en coordinación octaédrica formando capas de octaedros o capas octaédricas. Las posiciones octaédricas (O) esta ocupadas por Mg2+ (y/o Fe2+) o por Al3+ (y/o Fe3+). La unión entre una capa tetraedrica y una capa octaédrica tiene lugar mediante los oxígenos apicales. Los oxígenos apicales son compartidos por la capa T y por una capa O. Mg2+/Fe2+ Al3+/Fe3+ O = O H+ . Si4+/A13+ . T T Los oxígenos de los vértices de los octaedros que no están compartidos por una capa tetraédrica están unidos a H formando grupos OH. Por ejemplo, hay un grupo OH en el centro del cerco hexagonal formado por seis oxígenos apicales. En la figura los triángulos sombreados en gris representan la posición de los octaedros. Los octaedros comparten vértices entre sí y "se apoyan" sobre una cara.Si, Al Mg, Al, Fe H Oxígeno apical Grupo OH
Tipos de Capas Octaédricas
Cada oxígeno apical forma parte de tres octaedros. Las posiciones octaédricas pueden estar ocupadas por cationes divalentes o trivalentes. Oxígeno apical Grupo OH" Mg2+ con NC=6; f.e.e. = 2/6 = 1/3 Al3+ con NC=6; f.e.e. = 3/6 = 1/2 Segunda regla de Pauling: En una estructura iónica estable, la fuerza electrostática (f.e.) del total de enlaces que llegan a un anión procedentes de los cationes vecinos es igual a la carga del anión (Z-).
- Si el cation que hay en el centro del octaedro es divalente (Mg2+, Fe2+), de cada tres posiciones octaedricas, estan ocupadas las tres: capa trioctaedrica.
- Si el cation que hay en el centro del octaedro es trivalente (Al3+, Fe3+), de cada tres posiciones octaédricas, están ocupadas solo dos: capa dioctaédrica.
Clasificación de los filosilicatos
La clasificación de los filosilicatos se basa en los siguientes tres criterios:
- apilamiento de las capas T y O
- tipo de capa O
- Dioctaédrica
- Trioctaédrica
- existencia o no de déficit de carga (existencia o no de cationes interlaminares).
Se distinguen tres grandes grupos: Filosilicatos 1:1, Filosilicatos 2:1, Filosilicatos 2:1:1.
Filosilicatos 1:1
- Su estructura se basa en el apilamiento de una capa T y una O.
- La secuencia se repite a lo largo del eje cristalográfico c.
- La distancia entre dos láminas T sucesivas es de 7Å, este parámetro se denomina espaciado basal.
- Sin sustitución de Si por Al en la capa T.
- No hay déficit de carga: no hay cationes en posiciones interlaminares.Lámina tetraedrica (T) Lámina 7Ä octaedrica (O) T O S
- Ejemplos:
- Dioctaédrico: Caolinita: Al2Si2O5(OH)4
- Trioctaédrico: Serpentina: Mg3Si2O5(OH)4
Filosilicatos 2:1
- Su estructura se basa en el apilamiento de una capa T, una O y otra capa T.
- La secuencia se repite a lo largo del eje cristalográfico c.
- La distancia entre dos láminas T sucesivas con la misma orientación (espaciado basal) es de 9-15Å. Lámina tetraedrica (T) Lámina 9-15 Å octaedrica (O) Lámina tetraedrica (T) Interlámina T O linares T
- Se diferencian tres subgrupos:
- Subgrupo 1:
- Sin sustitución de Si por Al en la capa T.
- No hay deficit de carga: no hay cationes en posiciones interlaminares.
- Espaciado basal = 9A.
- Ejemplos:
- Dioctaédrico: Pirofilita: Al2Si4O10(OH)2
- Trioctaédrico: Talco: Mg3Si4O10(OH)2
- Subgrupo 2:
- Con sustitución parcial de Si por Al en la capa T.
- Hay déficit de carga y entran cationes en la interlámina.
- Espaciado basal = 10A (micas)
- Ejemplos:
- Dioctaédrico: Moscovita: KAl2Si3AlO10(OH)2
- Trioctaédrico: Biotita: K(Mg, Fe2+)3Si3AIO10(OH)2
- Subgrupo 3:
- Con sustitución parcial y variable de Si por Al en la capa T.
- Hay deficit de carga y entran cationes y moléculas de agua en la interlámina.
- Espaciado basal = 15A (esmectitas y vermiculitas).
- Ejemplos:
- Dioctaédrico: Montmorillonita:(Ca,Na)0.35Al2(Si,Al)4O10(OH)2 nH2O
- Trioctaédrico: Vermiculita: (Ca,Mg)0.35Mg3(Si,Al)4O10(OH)2 nH2O
- Subgrupo 1:
Filosilicatos 2:1:1
- Su estructura se basa en el apilamiento de una capa T, una O, otra T y otra O.
- La secuencia se repite a lo largo del eje cristalográfico c.
- El espaciado basal es de 14A.
- Con múltiples posibilidades de sustituciones cationicas tanto en las capas tetraédricas como en las octaédricas.
- Hay variedades ricas en aluminio y otras magnésicas.
- Este grupo lo constituyen las cloritas.
- Las hay dioctaédricas, trioctaédricas y di-tri octaédricas. Lámina tetraedrica (T) Lámina octaedrica (O) Lámina 14 Å tetraedrica (T) Lámina octaedrica (O) T 0 T
Minerales de la arcilla de interés industrial
Hay algunos filosilicatos a los que en la bibliografía se les suele denominar MINERALES DE LA ARCILLA. Hay que distinguir los siguientes términos o conceptos:
- Arcilla: Material natural de tamaño de grano fino (<2u), que presenta propiedades de plasticidad, es decir la capacidad de ser moldeado al mezclarse con una cantidad apropiada de agua, y de mantener la forma adquirida al ser secado o cocido. Arcilla = Minerales de la arcilla + minerales asociados + fases asociadas.
- Minerales de la arcilla: minerales de tamaño inferior a <2u responsables de las
propiedades de la arcilla, es decir, plasticidad en húmedo y endurecimiento tras el secado.
Son filosilicatos.
- Illita [Kx(AI, Mg, Fe)2(Si, Al)4O10(OH)2]: filosilicato de tamaño inferior a 2u.
- Minerales asociados: el resto de los minerales de los que se compone una arcilla (ej. cuarzo, calcita, dolomita, feldespatos, óxidos de hierro, etc.).
- Fases asociadas: fases no minerales que forman una arcilla (ej. materia orgánica, sílice coloidal, geles de hierro, etc.)
Caolinita
La caolinita [Al2Si2O5(OH)4] es un filosilicato 1:1 dioctaédrico (Al3+ en la capa O).Las rocas que son muy ricas en caolinita, se denominan caolín.
Propiedades de la caolinita
- Tamaños de cristal muy pequeños (<2u).
- Morfologías platiformes y hexagonales.
- Es un mineral muy blando.
- Es blanco, si no está mezclado con impurezas.
- Presenta brillo mate-terroso. Si, Al Al o2 . H*
- Comportamiento plástico al mezclarlo con agua en cantidades apropiadas.
Yacimientos de caolinita
La caolinita se forma fundamentalmente siguiendo la siguiente reacción química: 2KAISi308 + 2H2CO3 + 9H2O -- > 2 K+ + 2HCO3" + Al2Si205(OH)4 + 4H2SO4 Feldespato potásico + ácido carbónico + agua = iones K + iones bicarbonato + caolinita + ácido ortosilícico. Esta reacción se denomina hidrólisis del feldespato potásico y se desarrolla fundamentalmente en el ambiente externo, durante la meteorización química (frecuente en perfiles edáficos sobre rocas ricas en feldespatos). La reacción progresa más rápidamente si hay disponibilidad de agua, si el medio es ácido y si la temperatura es alta. Estas condiciones se dan en climas tropicales húmedos. También se puede producir una reacción similar en ambientes hidrotermales.
Usos industriales de la caolinita
- Industria papelera: se usa caolín muy puro, como carga y cobertura.
- Industria cerámica: se usan arcillas ricas en caolinita (mezclada con cuarzo, feldespatos, carbonatos, etc.) en las pastas de cerámica para sanitarios, pavimentos, revestimientos, gres y en los vidriados
- Otros usos:
- Fabricación de pinturas, latex y plásticos como carga.
- Fabricación de cosméticos y productos farmacéuticos.
Illita
La illita [Kx(Al, Mg, Fe)2(Si, Al)4O10(OH)2] es un filosilicato 2:1 dioctaédrico, con Al en la capa octaédrica y K en la interlamina. Presenta morfología laminar. Es muy frecuente en rocas sedimentarias y suelos. Es el filosilicato más abundante en las arcillas rojas que se utilizan para fabricar cerámica estructural.STRUCTURE OF ILLITE/MICA . O OH OK · Al, Mg, Fe · Si, Al MODIFIED FROM GRIM (1962)
Esmectitas
Las esmectitas son un grupo de filosilicatos 2:1, tienen moleculas de H2O y cationes en posiciones interlaminares, lo que condiciona una amplia variedad de composiciones; ej. La Montmorillonita [(Ca, Na)0.35Al2(Si,Al)4O10(OH)2nH2O]. En general, los cationes interlaminares son Ca, K, Na y/o Mg. STRUCTURE OF MONTMORILLONITE . 0 · OH · Si, Al · Al, Fe, Mg EXCHANGEABLE CATIONS n H2O MODIFIED FROM GRIM (1962) Las rocas con contenidos muy altos en esmectita, independientemente de su composición, se denominan "bentonitas".
Propiedades de las esmectitas
- Tamaño de partícula pequeño (<2u) y hábitos laminares.
- Alta capacidad de intercambio catiónico (CIC): los cationes de la interlámina pueden ser intercambiados por otros. La CIC de una bentonita puede variar en función del pH y Eh del medio.
- Alta capacidad de hidratación e hinchamiento: varían en función de la naturaleza del cation interlaminar y produce un incremento en el espaciado basal.
- Alta plasticidad: el agua forma una envuelta sobre las partículas laminares produciendo un efecto lubricante que facilita el deslizamiento de unas partículas sobre otras cuando se ejerce un esfuerzo sobre ellas.
- Alta tixotropía: es la propiedad de algunos fluidos pseudoplásticos que muestran un cambio en su viscosidad dependiente del grado de agitación: al aumentar la agitación disminuye la viscosidad.
Yacimientos de bentonitas
Las bentonitas se forman por:
- Desvitrificación y cristalización de vidrio volcánico (en perfiles de alteración sobre rocas volcánicas).
- En lagos alcalinos (pH alto) por cristalización a partir del agua.
- Meteorización química de aluminosilicatos en suelos.
Usos industriales de las esmectitas
Componente principal de la mayoría de los lodos de perforación (tixotropía).
- Aglomerante en la fabricación de piensos peletizados. Absorbente en cama de animales domésticos.
- Absorbente y aislante en la retención de aguas o lixiviados de vertederos de residuos tóxicos y radioactivos.
- Aglomerante en la fabricación de moldes de metalurgia. Filtro de impurezas en el procesado de aceites y vinos. Soporte de reacciones y catálisis en procesos químicos y/o farmacéuticos. Excipiente en la composición de fármacos
Minerales de la arcilla fibrosos
Las llamadas "arcillas fibrosas" son paligorskita y sepiolita. La sepiolita contiene fundamentalmente Si y Mg, y la paligorskita Si, Mg y Al. Sepiolita: Mg4Si6O15(OH)2 . 6H2O Paligorskita: (Mg,Al)2Si4O10(OH) . 4H2O Proyección SEPIOLITA (100) OH2 H2O(ZEOL) 0 O OH O Mg · Si Modificado de Bailey (1980) Sepiolita inversión cada 6 tetraedros. PALIGORSKITA Proyección (001) H2O DOH2 OH O · Mg, Al · Si Modificado de Bailey (1980) Paligorskita inversión cada 4 tetraedros Son filosilicatos 2:1 pero presentan inversiones periódicas en la polaridad de los tetraedros, lo que genera capas octaédricas discontinuas y canales internos.
Propiedades de las arcillas fibrosas
- Pequeño tamaño de partícula, partículas con hábito fibroso.