Características generales de los elementos de transición y sus compuestos
Documento de Universidad sobre Características generales de los elementos de transición y sus compuestos. El Pdf explora la teoría de bandas, el radio metálico y la conductividad eléctrica de los metales de transición, útil para estudiantes de Química.
Ver más19 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Características generales de los elementos de transición y sus compuestos
1
TEMA 1
- Características
generales de los
elementos de transición
y sus compuestos.
Elementos de transición
1
1
1
1
1
1
1
1
1
1
1
1
1
1Elementos de transición
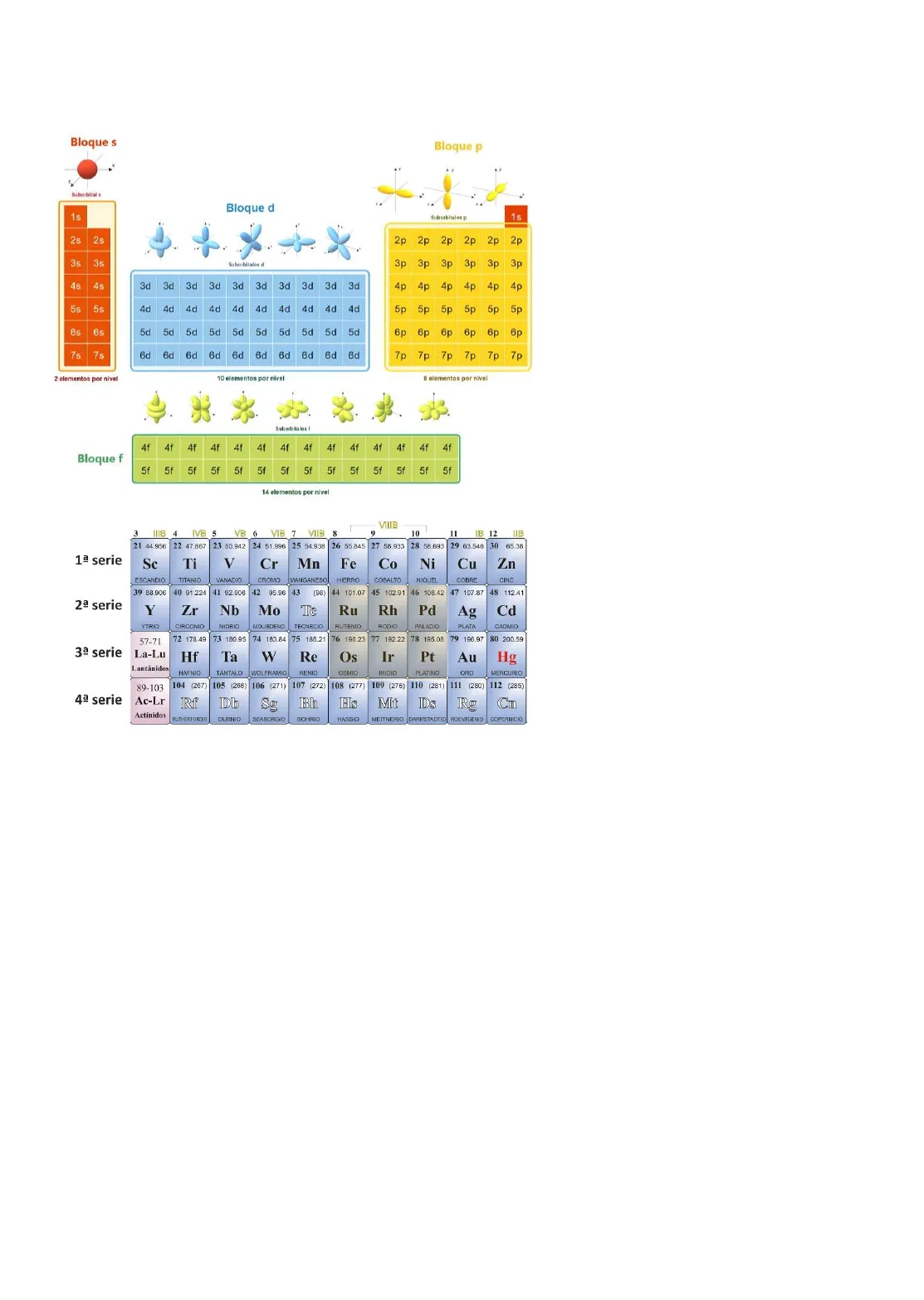
Bloque s
Bloque p
Suborbital #
Bloque d
Suborbitales p
1s
2s
2s
2p
2p
2p
2p
2p
2p
3p
3p
3p
3p
3p
3p
4s
3d
3d
3d
3d
3d
3d
3d
3d
3d
3d
4p
4p
4p
4p
4p
4p
5s
4d
4d
4d
4c
4d
4d
4d
4d
5p
5p
5p
5p
5p
5p
5d
5d
5d
5d
5d
5d
5d
5d
5d
5d
6p
6p
6p
6p
6p
6
7s
6d
6d
6c
6d
6d
6d
6d
6d
6d
6d
7p
7p
7p
7p
7p
7p
2 elementos por nivel
10 elementos por nivel
6 elementos por nivel
4f
4f
4f
4f
4f
4f
4f
4f
4f
4f
4f
4f
4f
4f
5f
5f
5f
5f
5f
5f
5f
5f
5f
5f
5f
5f
5f
5f
14 elementos por nivel
VIIIB
3
IIIB
4
IVB 5
VB 6
VIB 7 VIIB 8
10
11
IB 12
HIE
21 44.956
22 47.867
23 50.942
24 51.996
25 54.938
26 55.845
27 58.933
28 58.693
29 63.546
30 65.38
1ª serie
Sc
Ti
V
Cr
Mn
Fe
Co
Ni
Cu
Zn
ESCANDIO
TITANIO
VANADIO
CROMO
MANGANESO
HIERRO
COBALTO
NIQUEL
COBRE
CINC
39 88.906
40 91.224
41 92.906
42 95.96
43
(98)
44 101.07
45 102.91
46 106.42
47 107.87
48 112.41
2ª serie
Y
Zr
Nb
Mo
Te
Ru
Rh
Pd
Ag
Cd
YTRIO
CIRCONIO
NIOBIC
MOLIBDENO
TECNECIO
RUTENIO
RODIO
PALADIO
PLATA
CADMIO
57-71
72 178.49
73 180.95
74 183.84
75 186.21
76 190.23 77 192.22
78 195.08
79 196.97
80 200.59
3ª serie
La-Lu
Lantánidos
Hf
Ta
W
Re
Os
Ir
Pt
Au
Hg
HAFNIO
TÁNTALO
WOLFRAMIO
RENIO
OSMIO
IRIDIO
PLATINO
ORO
MERCURIO
89-103
104 (267)
105 (268)
106 (271)
107 (272)
108 (277)
109 (276)
110 (281)
111 (280)
112 (285)
4ª serie
Ac-Lr
Actinidos
Rf
Db
Sg
Bh
Hs
Mt
Ds
Rg
Cn
RUTHERFORDIO
DUBNIO
SEABORGIO
BOHRIO
HASSIO
MEITNERIO
DARMSTADTIO| ROENTGENIO
COPERNICIO
Los elementos de transición son
aquellos que en alguno de sus estados
de oxidación tienen orbitales d o f
parcialmente ocupados.
Consideraremos de transición a todos
los elementos del bloque d (excepto
Zn, Cd y Hg) y los del bloque f
(lantánidos y actínidos), que son los
de transición interna.
El bloque d lo componen los
elementos situados entre los bloques
s y p. En su estado fundamental se
llenan progresivamente los niveles nd
(n = 3, 4, 5, 6).
El bloque f lo componen los
elementos situados después del
lantano y del actinio. En su estado
fundamental se ocupan
progresivamente los niveles 4f o 5f.
- Los elementos escandio, titanio, vanadio, cromo, manganeso, hierro, cobalto, niquel y cobre (Sc, Ti,
V, Cr, Mn, Fe, Co, Ni y Cu) constituyen la primera serie de transición (3d). - Los elementos itrio, circonio, niobio, molibdeno, tecnecio, rutenio, rodio, paladio y plata (Y, Zr, Nb,
Mo, Tc, Ru, Rh, Pg y Ag) constituyen la segunda serie de transición (4d). - Los elementos lantano, hafnio, tántalo, wolframio, renio, osmio, iridio, platino y oro (La, Hf, Ta, W,
Re, Os, Ir, Pt y Au) constituyen la tercera serie de transición (5d).
Configuraciones electrónicas
Las configuraciones electrónicas de los elementos de transición son en general de los tipos:
[GN] (n-1)dns2, [GN] (n-1)d ** Ins", [GN] (n-1)d1º nsº
(n = 4, 5, 6, 7; x =1-9)
Las configuraciones electrónicas de los elementos de transición interna son en general:
[GN] (n-2)f*(n-1)d'ns2 (x=0-14; y=0, 1,2)
3s
3s
Suborbitales d
4s
5s
4d
4d
6s
6s
7s
Suborbitales !
Bloque f
1sLos elementos de la primera serie de transición tienen configuración electrónica [Ar] 4s2-x 3dª ** con
x = 0-1 y a = 1-9. El número total de electrones de valencia (a + 2) es el número del grupo.
En general, la configuración de la segunda serie de transición es [Kr] 5s2-x 4da ** y la tercera serie de
transición incorpora los orbitales f con una configuración [Xe] 6s2-x 4f14 5da ** (excepto el La que no
tiene los 4f14).
Configuraciones electrónicas de los elementos de transición en el estado fundamental
21
Sc
[Ar]3d14s2
22
Ti
[Ar]3d24s2
23
V
[Ar]3d34s2
24
Cr
[Ar]3d54s1
25
Mn
[Ar]3d54s2
26
Fe
[Ar]3d®4s2
27
Co
[Ar]3d74s2
28
Ni
[Ar]3d®4s2
29
Cu
[Ar]3d1º4s1
39
Y
[Kr]4d15s2
40
Zr
[Kr]4d25s2
41
Nb
[Kr]4dª5s'
42
Mo
[Kr]4d55s1n
43
Tc
[Kr]4d55s2
44
Ru
[Kr]4d75s1
45
Rh
[Kr]4d85s1
46
Pd
[Kr]4d10
47
Ag
Kr]4d1º5s1
72
Hf
[Xe]4f14
5d26s2
73
Ta
[X]4f14
5d36s2
74
W
[X]4f14
5dª6s2
75
Re
[Xe]4f14
5d56s2
76
Os
[X]4f14
5do6s2
77
Ir
[Xe]4f14
5d76s2
78
Pt
[Xe]4f14
5d96s1
79
Au
[Xe]4f14
5d1º6s1
* Los elementos
señalados son los
que tienen una
configuración
electrónica
diferente a la
esperada.
Configuraciones electrónicas de los elementos de transición interna en el estado fundamental
57
La
[Xe]
5d16s2
58
Ce
[Xe]4f1
5d16s2
59
Pr
[Xe]
4f6s2
60
Nd
[Xe]
4f 6s2
61
Pm
[Xe]
4f-6s2
62
Sm
[Xe]
4f66s2
63
Eu
[Xe]
4f6s2
64
Gd
[Xe]4f7
5d16s2
65
Tb
[Xe]
4f1º6s2
66
Dy
[Xe]
4f116s2
67
Ho
[Xe]
4f126s2
68
Er
[Xe]
4f136s2
69
Tm
[Xe]
4f146s2
70
Yb
[Xe]
4f-6s2
71
Lu
[X]4ª
5d1652
89
Ac
[Rn]
6d17s2
90
Th
[Rn]
6d27s2
91
Pa
[Rn]5f2
6d17s2
92
U
[Rn]5f3
6d17s2
93
Np
[Rn]5fª
6d17s2
94
Pu
[Rn]
5f67s2
95
Am
[Rn]
5f 7s2
96
Cm
[Rn]5fª
6d17s2
97
Bk
[Rn]
5fª7s2
98
Cf
[Rn]
5f1º7s2
99
Es
[Rn]
5f117s2
100
Fm
[Rn]
5f127s2
101
Md
[Rn]
5f137s2
102
No
[Rn]
5f147s2
103
Lr
[Rn]5f14
6d17s2
Factores que determinan la configuración
Carga nuclear efectiva: Zeff
La carga nuclear efectiva es la carga positiva neta experimentada por un electrón en un átomo
polielectrónico. Se usa el término "efectiva" porque el efecto de apantallamiento de los electrones más
cercanos al núcleo evita que los electrones en orbitales superiores experimenten la carga nuclear
completa debido a las repulsiones interelectrónicas.
Generalmente el orden energético de los orbitales es s < p <d <f, los orbitales s son los más
penetrantes ya que tienen una probabilidad no nula de estar en el núcleo. Pero al entrar el primer
electrón al orbital 3d en el Sc, la energía relativa entre este y el 4s se invierte y el 3d pasa a estar en un
nivel más bajo de energía y ser más interno. A pesar de esto los siguientes electrones llenan el orbital 4s,
ahora más alto en energía que el 3d, porque hay menos repulsiones interelectrónicas en este orbital.
En la primera serie de transición, la energía y el tamaño de los orbitales d disminuye al desplazarnos
hacia la derecha y aumenta la separación entre los orbitales 3d y 4s.
La separación entre los orbitales 4d y 5s es menor que entre 3d y 4s y aún menor entre 5d y 6s.
Zeff
Apantallamiento
?(r) 2
00
4d
4f
4Tr2Rn.(r)2
Función de distribución radial
4
3p
- Z ≥ 21 (Sc: Z=21)
3s
3
2p
n
2s
2
4
Energy
Energy -+
3
2
1
1s
0
1
1
25
50
75
100
Atomic number, Z
Distance r from the nucleus/atomic units
Efectos relativistas
Como consecuencia del llenado de los orbitales f aumenta el tamaño, la
masa y la carga del núcleo. Los electrones, especialmente en los orbitales más
internos, se ven muy afectados por esta gran diferencia de masa y carga respecto
al núcleo, aumentando su velocidad hasta cifras cercanas a la velocidad de la
luz. Esto provoca un cambio en la masa del electrón (masa relativista) y afecta
al tamaño y forma de los orbitales atómicos, tanto internos como externos.
mo
m =-
1,2
1-
2
mo = "masa en
reposo"
Los orbitales s y p se ven especialmente afectados al ser más internos y sufren efectos relativistas
directos, haciendo que se contraigan.
Los orbitales d y f son más externos y sufren efectos relativistas indirectos, haciendo que se expandan y
sean más difusos.
En la tercera serie de transición predomina la configuración [Xe] 5d* 6s2 por el aumento de la
diferencia de energía entre los orbitales 6s y 5d debido a los efectos relativistas.
Repulsiones interelectrónicas
Las repulsiones interelectrónicas son más altas en el orbital 3d que en el 4s, por eso se llena el orbital
s a pesar de encontrarse más alto en energía y en la primera serie de transición predomina la
configuración [Ar] 3d* 4s2.
Las repulsiones interelectrónicas en los orbitales d disminuyen al bajar en un mismo grupo debido a
que los orbitales son cada vez más difusos al ser capas más externas y con mayor distorsión por efectos
relativistas (3d-3d > 4d-4d > 5d-5d). Por eso en la segunda serie de transición predomina la configuración
[Kr] 4dx+15s1.
Energía de cambio o canje
Las configuraciones con d5, d1º, f7 of14 son especialmente estables por el semillenado o llenado
completo del orbital.
3d
3p
35
4p
4s
3d_Z < 21
K
AP
3d
Q ca
5
SC
Tia
T
0
10
20
Consecuencias de la configuración electrónica
Consecuencias:
- Muchos estados de oxidación: muchos electrones de valencia.
- Compuestos de valencia mixta: hay pequeñas diferencias de energía entre algunos estados de
oxidación (ej. Fe3O4 = Fe" Fez"" O4).
- Compuestos coloreados: AE(HOMO-LUMO) es pequeña y hay transiciones de absorción.
- Compuestos paramagnéticos: comportamiento magnético complejo y variado.
- Índices de coordinación altos: valencias muy elevadas.
Estructura de los metales de transición en estado sólido
En el estado elemental todos son sólidos no moleculares y presentan varias formas polimórficas.
Las estructuras que toman los elementos de transición son: red cúbica centrada en el cuerpo (ccc),
empaquetamiento cúbico compacto (ecc) y empaquetamiento hexagonal compacto (ehc).
I.C. = 8
Capa c
Capa b
Vista de arriba
Capa a
Número de coordinación = 12
EMPAQUETAMIENTO HEXAGONAL COMPACTO
Capa a
Capa b
Capa a
Vista de arriba
Número de coordinación = 12
A presiones elevadas ocurren transiciones a fases cristalinas en las que los átomos metálicos presentan
índices de coordinación (I.C.) más altos y estructuras más compactas que aquellas que son estables a
presión y temperatura ambiente.
En general, al elevar la temperatura,
Estructura de los metales de transición a 298K y 1atm:
3
4
5
6
7
8
9
10
manteniendo presión atmosférica o
Cu
.
bajas presiones, se producen transiciones
Sc
Ti
V
Cr
.
Fe
Co
Ni
11
.
.
.
a fases cristalinas menos compactas.
2180
1768
397
1811
418
428
T/K
Liquid
2000
ecc
1400
800 -
ehc
CCC
200
1
10
102
103
104
105
P/bar
Zr
Nb
Mo
Tc
·
Ru
.
Rh
.
Pd
Ag
.
1799
423
2128
2750
2896
658
2430
2607
651
2237
556
1828
377
137
1235
285
144
La
Hf
.
Ta
W
Re
Os
.
Ir
Pt
Au
.
1193
423
2506
3290
3695
850
3459
774
3306
2719
669
787
188
159
147
141
137
135
136
2041
566
139
1337
368
144
1814
378
164
1941
470
147
2183
514
135
129
Mn
see text
1519
283
137
126
125
1728
430
125
1358
338
128
609
721
677
182
160
147
140
135
134
134
Y
.
.
.
619
782
Cúbica centrada en el cuerpo
EMPAQUETAMIENTO CÚBICO COMPACTO
Capa a
Teoría de bandas
La teoría de bandas considera que los orbitales atómicos de valencia de los n átomos que estarán
formando el enlace metálico se combinan entre sí para dar n orbitales moleculares. Cuando n es un
número muy elevado, los orbitales moleculares formados se encuentran muy próximos en energía y dan
lugar a una banda.
Los orbitales moleculares más bajos en energía que el orbital atómico original son orbitales enlazantes y
los que tienen más energía son orbitales antienlazantes.
Los electrones de los átomos van ocupando los orbitales moleculares en orden de menos a más energía,
pero al estar los niveles tan próximos en energía los electrones pueden moverse libremente por toda la
banda. La banda de energía formada por los orbitales atómicos de valencia es la banda de valencia y la
formada por los primeros orbitales atómicos vacíos es la banda de conducción.
En los metales la banda de valencia está semillena o llena, pero solapada con la banda de conducción,
por lo que los metales son buenos conductores eléctricos.
Node
Bandwidth-
Empty
E
1
1
2
3
4
5
30
Bonding MOs
Energía
E
np
Banda s-p
ns
Banda d
(n-1)d-
Orbitales atómicos
Densidad de estados N(E)
El número de niveles con un determinado valor de energía se conoce como la densidad de estados N(E).
La densidad de estados no es uniforme a lo largo de toda la banda porque los niveles de energía se
empaquetan más a unos determinados valores de energía que a otros debido a la forma de las
combinaciones lineales que originan los orbitales moleculares que constituyen la banda. Hay más
combinaciones posibles degeneradas en energía que dan lugar a los orbitales moleculares de la parte
central de la banda.
La banda d se estrecha al avanzar hacia la derecha en un mismo
periodo porque la ocupación de la banda es mayor y las repulsiones
interelectrónicas son más fuertes, hay menor solapamiento.
Al representar la diferencia de energía total (calculada a partir de la
densidad de estados para los diferentes tipos de estructuras de los
metales de transición) frente al número de electrones de valencia
(N = s+d) se aprecia una gran diferencia de energía entre ccc y ecc.
Para N = 5 o 6 la estructura más estable es la ccc, mientras que para
N > 7 las estructuras compactas son más estables. El ehc es más
estable para N = 7 u 8 y el ecc para N > 8.
Total AU (kcal/mole)
6-
4 -
2 -
7 8
ehc-ecc
0
5 6
9 10 11
-2
-4
ccc-ecc
Number of valence electrons N
Number of atomic orbitals >
Antibonding MOs
Energy band
Filled