El laboratorio en la evaluación de proteínas y su metabolismo
Diapositivas sobre la evaluación de proteínas y su metabolismo. El Pdf, un recurso de Biología para Universidad, explora la estructura de los aminoácidos, el origen y la clasificación de las proteínas, así como sus funciones en el organismo y la electroforesis de proteínas plasmáticas.
Ver más20 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Proteínas y su metabolismo
Unidad 6: Proteína
- Asociación de varios aminoácidos puestos en una cadena lineal.
- Contienen carbono, oxígeno, nitrógeno e hidrógeno.
- Los aminoácidos se unen entre sí por enlaces peptídicos, uniendo el extremo amino de uno con el extremo carboxilo de otro aminoácido.
¿Qué es un aminoácido?
Un aminoácido es una molécula orgánica con un grupo amino (-NH2) y un grupo carboxilo (- COOH). Los aminoácidos más frecuentes y de mayor interés son aquellos que forman parte de las proteínas.
Se tiene una infinidad de tipos de proteínas, de acuerdo a lo que se vaya uniendo a este radical, dando lugar a la lipoproteínas, las proteínas carboxiladas, las proteínas unidas a hidratos de carbonos, a las proteínas transportadoras de metales, etc
amino acids peptide protein grupo amino H O H N -- C-C-O-H C C+N R carbono alfa CH2 1 CH2 1 Grupo amino -NH2 Grupo ácido -COOH CH2 CH2 Cadena o radical Diferente para NH2 cada aminoácido
Origen de las proteínas
El hombre puede sintetizar algunos de los aminoácidos (aas) que necesita para formar sus proteínas a partir de compuestos nitrogenados más simples o transformando sus aminoácidos entre sí.
Existe sin embargo un grupo de aminoácidos para la síntesis de proteínas y que los animales superiores no pueden formar, a estos aminoácidos se les llama esenciales y deben ser proporcionados por los alimentos, en forma de proteínas vegetales o animales
Aminoácidos Esenciales
- Ramificados: Valina (Val), Leucina (Leu), Isoleucina (Ile)
- Básicos: Lisina (Lys), Arginina (Arg), Histidina (His)
- Aromáticos: Fenilalanina (Phe) y Triptófano (Trp)
- Otros: Metionina (Met) y Treonina (Thr)
Mnemotecnia para aminoácidos esenciales
Fer Hizo un Lío Tremendo y Valentina Le Metió un Triptófano Lisina Triptófano Isoleucina Metionina Histidina Valina Leucina Fenilalanina Treonina
Aminoácidos No Esenciales
Glicina (Gly), Alanina (Ala), Prolina (Pro), Serina (Ser), Ácido glutámico (Glu), Cisteína (Cys), Tirosina (Tyr), Asparagina (Asn), Glutamina (Gln) y Ácido Aspártico (Asp)
En general, las proteínas animales contienen aminoácidos esenciales en mayor cantidad y en las proporciones en que el hombre los necesita, y por eso son de mayor valor nutritivo.
Clases de proteínas plasmáticas
- Las proteínas son complejas sustancias orgánicas nitrogenadas y tienen un papel fundamental en la estructura y funcion de las células tanto animales como vegetales.
- Cada especie tiene proteínas características, lo que le confiere su carácter específico, tanto genético como inmunológico.
- La palabra proteína viene del griego "proteos" que quiere decir el primero, ya que forma parte básica de la estructura corporal.
Estructura de los aminoácidos
grupo carboxilo H H H/ HO - H Arginina e Histidina solo son esenciales en periodos de crecimiento celular, la infancia, la lactancia y la enfermedad
- Este término fue sugerido por Mulder, químico Holandés, en el siglo XIX para designar el componente universal de todos los tejidos vegetales y animales. "Sin proteínas no hay vida posible en nuestro planeta".
- A través de ellas se producen los principales fenómenos de la vida.
- El principal papel de las proteínas de la dieta es servir como fuente principal de aminoácidos, los cuales son utilizados para la síntesis de proteínas nuevas en nuestro organismo.
Clasificación de las proteínas
Por su origen
1. Proteínas de origen animal:
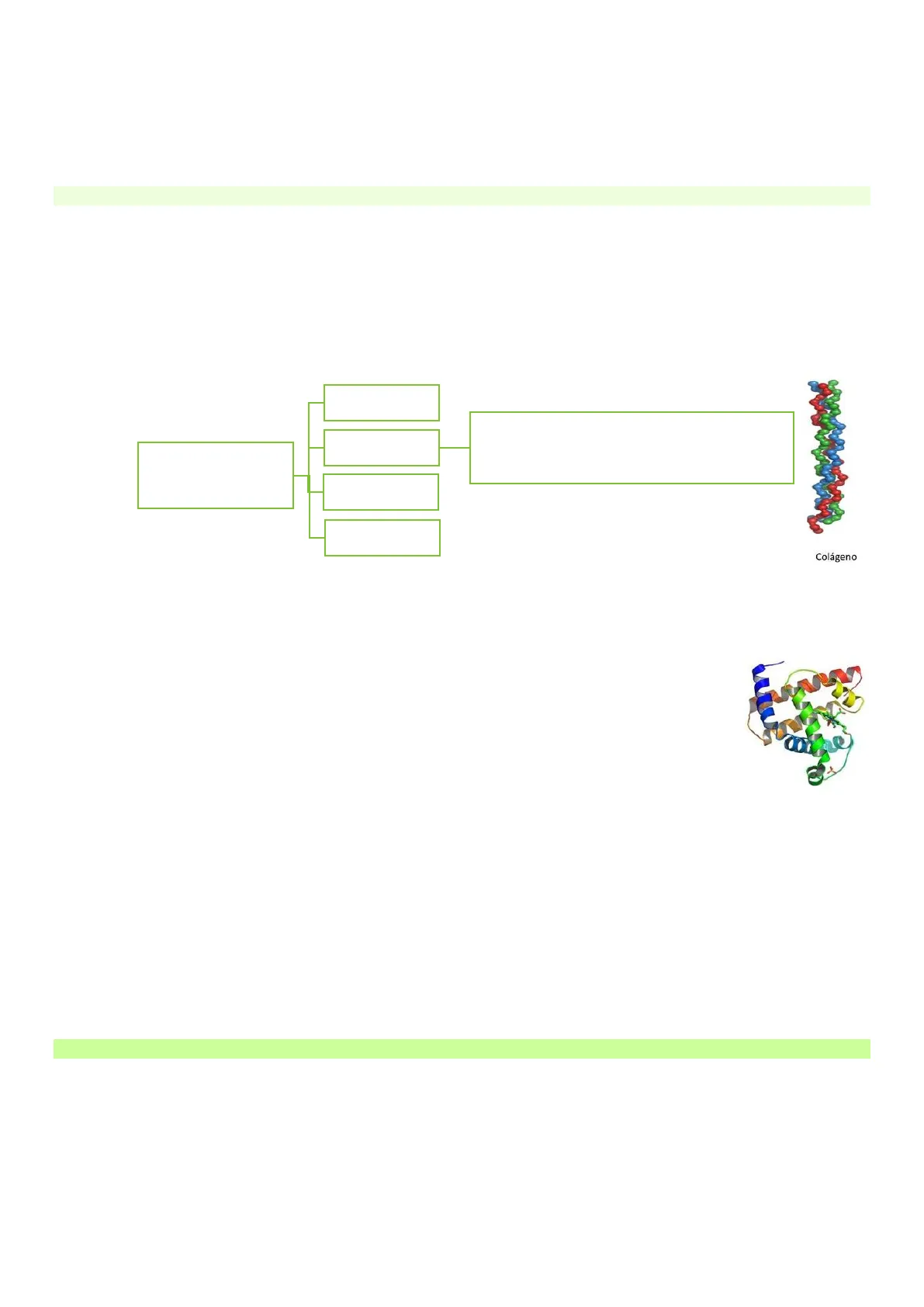
a. Escleroproteínas o proteínas fibrosas:
como la elastina del músculo y colágeno del tejido conjuntivo. Estas proteínas son insolubles debido a su estructura molecular, y desempeñan funciones de protección y soporte de tejidos
Las proteínas fibrosas tienen cadenas polipeptídicas dispuestas en grandes hebras u hojas Constan mayoritariamente de un único tipo de estructura secundaria Forman parte de las estructuras que dan soporte, forma y protección externa a los vertebrados Son claros ejemplos de estructura y función Queratinas Colágeno Triple hélice de golágeno. Modificación postraduccional de los aa del colágeno. Fibras del colágeno Estructura y función Elastina Fibroinas Colágeno
b. Esferoproteínas o proteínas globulares:
son constituyentes de líquidos orgánicos, como la caseína de la leche, la albúmina de la clara del huevo y las globulinas del plasma sanguíneo. Este tipo de proteínas en general, son solubles en agua, se digieren fácilmente y contienen una buena proporción de aminoácidos esenciales.
Las proteínas globulares tienen cadenas polipeptídicas plegadas en forma globular o esférica Tiene varios tipos de estructura secundaria La mayoría son enzimas y proteínas reguladoras Ejm: Mioglobina y Hemoglobina
- Estructura y función. Grupo Hemo
- Curva unión O2 a la Mb
- Mioglobina
c. Protaminas e Histonas:
son polipéptidos de pesos moleculares no muy elevados. Se encuentran en los huevos de pescados
2. Proteínas de origen vegetal:
a. Glutelinas y Prolaminas:
Las contienen los vegetales, especialmente los cereales, por ej. Glutenina en el trigo, ordeina en la cebada, gliadina en el trigo y centeno, etc.
El compuesto denominado gluten es una mezcla de gliadina más glutenina.
Una vez metabolizadas dentro del organismo, se convierten en proteínas plasmáticas.
Por su estructura
1. Simples u holoproteínas:
son las compuestas solo por aminoácidos. Por ejemplo albúmina.
2. Complejas o heteroproteínas:
son las que se encuentran unidas a un grupo no proteico llamado grupo prostético. Por ej. lipoproteínas y nucleoproteínas.
Funciones de las proteínas en el organismo
- Son parte estructural de las células. lo que realmente importa en esta cátedra
- Participan en la movilidad celular.
. Muchas hormonas son de naturaleza proteica.
- La mayoría de las enzimas son proteínas.
- Son indispensables para la acción que realizan las vitaminas.
- Forman parte de los receptores hormonales.
- Algunas son segundos mensajeros para la acción hormonal.
. Forman complejos con glúcidos y lípidos, como las Glucoproteínas y Lipoproteínas.
. Participan en la defensa inmunológica. Ej .: inmunoglobulinas y sistema de complemento.
- Participan en la contracción muscular.
- Proteínas asociadas a sistemas buffer.
- Proteínas transportadoras. Ej .: albúmina, hemoglobina y transferrina.
- Proteínas de coagulación.
- Proteínas reguladoras. Ejm: citoquinas
- Proteínas de sostén. Ejm : colágeno
Metabolismo de las proteínas plasmáticas
- El hígado es el órgano más importante para regular la síntesis de proteínas mediante ciclos de sustratos y reacción catalizada por activación simultánea de varias enzimas, las cuales producen proteínas de manera rápida a concentraciones elevadas, aún en forma intermitente, dependiendo de las necesidades
- El valor biológico (proporción del nitrógeno retenido dividido nitrógeno absorbido) de las proteínas depende de la cantidad de aminoácidos esenciales que contengan, se le asigna a la albúmina del huevo el valor de 1
- El valor biológico hace referencia a la proporción de aminoácidos esenciales de los alimentos y su facilidad de asimilación por nuestro organismo.
. Expresa la fracción de nitrógeno absorbido y retenido por el organismo y representa la capacidad máxima de utilización de una proteína.
Tabla de Valor Biológico de Proteínas
Tipo de proteína Valor Biológico Tipo de proteína Caseína Valor Biológico 77 Suero de leche 104-120 Huevo entero 100 Soja 74-90 Clara de huevo 88 Gluten entero 64 Pescados 80-85 Arroz 59 Aislado de guisante 80-85 Legumbres 50 Carnes 78-80 Cereales <50
- En un varón de peso corporal promedio, 16% corresponde a proteínas, siendo la mitad intracelular, el resto extracelular y el 2,6% es nitrógeno.
- La proteína tiene un estado dinámico constantemente hay catabolismo y resíntesis. El objetivo de este recambio es tener un máximo de utilidad en proteínas con escasa cantidad de aminoácidos
ANAVIP: El Huevo
ALIMENTO COMPLETO VALIOSOS NUTRIENTES: ES RICO EN PROTEÍNAS: Contiene hierro, calcio, fósforo, zinc, magnesio y vitaminas del complejo B. Dos huevos aportan 13 gramos de proteínas de alta calidad. CUIDA TUS OJOS: El huevo tiene alto contenido de vitamina A que ayuda a prevenir las cataratas. MEJORA LA MEMORIA: AYUDA A CONTROLAR EL PESO: La colina es un nutriente abundante en el huevo y ayuda en el desarrollo cerebral. Las proteínas del huevo dan saciedad, lo que ayuda en el control del peso. GRASAS: Está demostrado que el colesterol del huevo no es perjudicial para la salud. Las grasas del huevo ayudan a la absorción de vitaminas A, D, E y K. EL HUEVO
Metabolismo de las proteínas
Es el resultado de tres procesos:
- Ritmo de síntesis. La velocidad en la que se producen las proteínas
- Volumen del líquido donde se distribuyen.
- Ritmo de la degradación
Síntesis de la proteína
Replicación ARNm Síntesis de la proteína ADN - Ribosoma Transcripción (Síntesis de ARNm) Proteína ADN ARNm Proteína
1. Síntesis
El proceso de síntesis de las proteínas
La síntesis principalmente se produce en el hígado. También se producen en los Tejidos periféricos como las inmunoglobulinas en los linfocitos B, o las Apolipoproteína en las células de la mucosa intestinal.
El mecanismo de la síntesis es común para todas ellas y el control de la síntesis se ejerce en la transcripción o la traducción.
2. Volumen donde se distribuyen
El equilibrio de líquidos entre los compartimentos intravascular y extravascular del organismo, hacen que se mantenga la presión coloidosmótica del plasma (la presión osmótica del plasma es la suma de 2 presiones: la oncótica y la hidrostática que es la presión del agua).
Como se sabe las proteínas no pasan de un lugar a otro, pero sí el agua, entonces, por la presión osmótica se puede tener por ejm un edema cuando hay poca proteína, por lo que el agua escapa a los demás espacios y no permanece en donde debería estar, esto causa que el paciente esté edematizado, en donde tiene una hinchazón, que si se presiona con el dedo, queda marcado, por lo tanto, estos son los síntomas de un edema cuando se tiene un mayor volumen de líquido (en comparación con lo normal)
3. Catabolismo
Es la destrucción es éstas proteínas. El catabolismo tiene lugar en muchas distintas células:
- Endoteliales.
- Fagocitos mononucleares.
- Fibroblastos cutáneos.
- Pérdidas por filtración glomerular
- Pérdidas a través de la pared intestinal
Proteínas plasmáticas
- La sangre es un tejido que circula dentro de un sistema virtualmente cerrado, el de los vasos sanguíneos.
- La sangre compuesta por elementos sólidos; eritrocitos, leucocitos y plaquetas, suspendidos en un medio líquido; el plasma.
- El plasma consiste en agua, electrolitos, metabolitos, nutrientes, proteínas y hormonas. Entonces las proteínas plasmáticas son las que están suspendidas en el plasma
- Una vez que la sangre se ha coagulado, la fase líquida remanente se denomina suero, este carece de factores de la coagulación, que normalmente están presentes en el plasma, pero que ha sido consumido durante el proceso de coagulación.
Es por eso que cuando se quiere obtener plasma, se utilizan anticoagulantes, que de acuerdo a los análisis a realizar son diferentes, por ejm, para un estudio de celularidad sanguínea se utiliza EDTA, sin embargo, para un estudio de los factores de la coagulación, se prefiere el citrato, si se necesita examinar la química del paciente, se necesita de suero, por lo tanto no se utiliza anticoagulantes para la muestra, con esto se produce la coagulación para obtener suero.
Análisis de las proteínas plasmáticas
El estudio de las proteínas se utiliza para el seguimiento de las enfermedades y no para diagnóstico o muy rara vez. Por eso es importante tener el valor normal del paciente y ver qué pasa cuando entra en estado de enfermedad. En la actualidad se han aislado y caracterizado alrededor de 100 proteínas, sin embargo las funciones de una gran parte de ella permanecen aún desconocida.
Proteínas plasmáticas de acuerdo con sus funciones
. Proteínas con función de transporte y asociados a sistemas buffer.
- Proteínas reactantes de fase aguda (se llaman así porque en situaciones de stress, procesos inflamatorios o traumatismos aumentan su concentración para compensar esos estados).
- Proteínas sintetizadas por el sistema inmuno competente.
- Un gran número de las proteínas conocidas tiene micro heterogeneidad, esto es debido en general a la cantidad variable de ácido siálico y en menor proporción a la sustitución de aminoácidos en la cadena polipeptídica. Actualmente se conocen las variables genéticas o polimorfismo genético de muchas proteínas. Estas se deben a las mutaciones en las cadenas polipeptídicas de las proteínas. Por ejemplo el polimorfismo de la PROTEINAS PLASMATICAS