Leucocoria, neuroftalmologia e disturbi della motilità pupillare
Documento di Università su leucocoria, neuroftalmologia e disturbi della motilità pupillare. Il Pdf esplora diverse patologie oculari, tra cui la leucocoria, il retinoblastoma e le neuropatie ottiche ischemiche, descrivendo cause, sintomi, diagnosi e trattamenti.
Mostra di più15 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Malattie dell'apparato visivo
Leucocoria: definizione e cause
Leucocoria in greco significa letteralmente "pupilla bianca". In medicina per leucocoria si intende la perdita del fisiologico colore rosso del riflesso retinico, che appunto diventa bianco. Tanto nel neonato quanto nell'adulto, la leucocoria deve destare la massima attenzione del clinico e infatti il test del riflesso rosso è uno dei primissimi test di screening cui viene sottoposto il neonato, sia alla nascita che durante i controlli periodici dal pediatra.
Le principali cause di leucocoria (congenita) sono:
- Cataratta congenita
- Fibroplasia retrolenticolare (o retinopatia del prematuro)
- Persistenza di vitreo primitivo iperplastico, una malformazione spesso associata a microftalmia
- Malattia di Coats
- Toxocariasi oculare
- Retinoblastoma
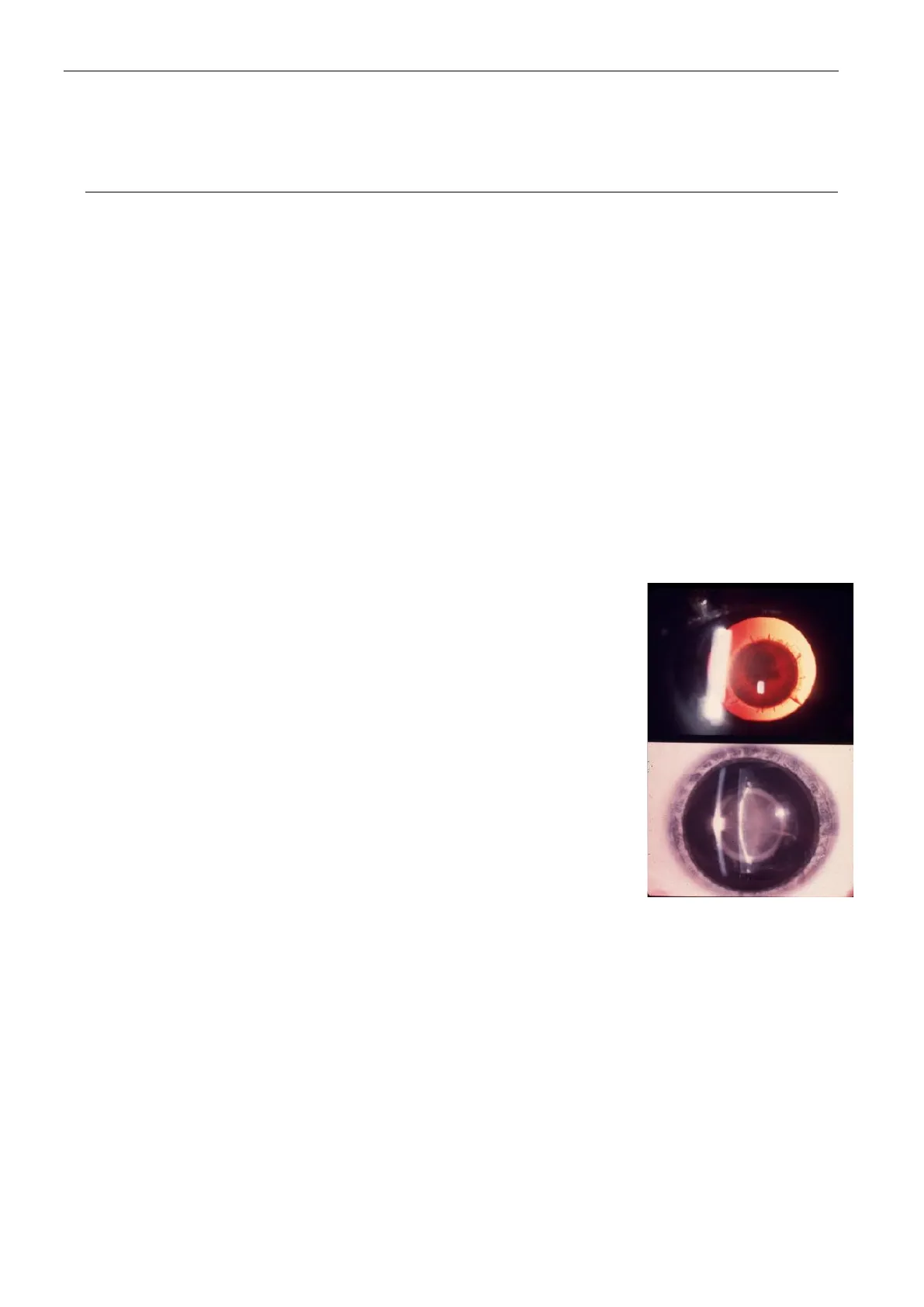
Cataratta congenita
In caso di cataratta congenita si rende necessaria una correzione chirurgica molto precoce: se non si riesce ad asportare l'opacità del cristallino entro i primi mesi di vita molto difficilmente si riuscirà a prevenire l'ambliopia. Il problema è che il cristallino è una lente convergente (o positiva) con un potere di rifrazione di circa 20 diottrie. Quindi dopo l'intervento bisogna correggere l'afachia, altrimenti l'occhio operato vedrebbe come un occhio ipermetrope di 20 diottrie. La correzione con occhiali è molto mal tollerata perché le lenti, che devono avere un elevato potere diottrico, sono spesse e pesanti, però ci si può pensare se entrambi gli occhi vengono operati di cataratta. Se invece viene operato un occhio solo (in caso di cataratta monolaterale) è molto difficile che gli occhiali possano funzionare: con occhiali così spessi la differenza di visione sui due occhi è molto "disturbante" ed è concreto il rischio di sviluppare ambliopia. La differenza di dimensioni nelle immagini formate sui piani retinici dei due occhi se la differenza di diottrie è molto forte si chiama aniseiconia.
La correzione preferibile è quella con lente a contatto: la lente non è dentro l'occhio quindi non mima perfettamente il cristallino, però riesce a compensare abbastanza bene la differenza di diottrie dopo l'intervento. Ovviamente trattandosi di bambini molto piccoli è importante che i genitori siano molto ben istruiti. Quando l'occhio è cresciuto a sufficienza (i bambini vengono seguiti tramite visite periodiche) si può valutare di impiantare un cristallino artificiale. Non è possibile impiantare una lente intraoculare subito dopo l'intervento perché le lenti artificiali hanno un potere diottrico fisso mentre il potere diottrico dell'occhio del bambino cambia continuamente in virtù dei fisiologici cambiamenti di forma del bulbo oculare in accrescimento.
A quanti anni si decide di impiantare la lente intraoculare? Non c'è un'età standard, dipende dal singolo caso. In linea di massima superata la fase critica dell'ambliopia, e cioè la scuola elementare, si può iniziare a pensare all'impianto.
Retinoblastoma
La causa peggiore di leucocoria, nonché motivo principale dello screening pediatrico con riflesso rosso, è il retinoblastoma. Il retinoblastoma è il più comune tra i tumori maligni intraoculari dell'infanzia, con un'età media alla diagnosi di 12 mesi per le forme bilaterali e di 24 mesi per le forme monolaterali. Il retinoblastoma è causato dalla perdita di entrambi gli alleli del gene oncosoppressore Rb, sito sul cromosoma 13. Il trattamento varia in base a localizzazione, estensione e mono- o bi- lateralità e può essere:
- Conservativo: chemioterapia, radioterapia, fotocoagulazione laser, crioterapia
- Radicale: enucleazione
Chiaramente ci si avvale di un trattamento conservativo in caso di bilateralità. Se il retinoblastoma è monolaterale si preferisce l'enucleazione, che abbassa significativamente il rischio di metastatizzazione.
Fibroplasia retrolenticolare
Nota anche come retinopatia del prematuro (ROP), si deve principalmente a due fattori:
- immaturità retinica: la retina non è completamente vascolarizzata neanche nel bambino nato a termine
- ossigenoterapia: fondamentale nella gestione del neonato prematuro ma favorisce neoangiogenesi accompagnata dalla produzione di tessuto fibrovascolare
A differenza della cataratta congenita e del retinoblastoma, la fibroplasia retrolenticolare è una causa di leucocoria che "non ci coglie di sorpresa" perché colpisce bambini prematuri, ricoverati in terapia intensiva neonatale, in particolare quelli di peso più basso. L'eziologia è multifattoriale ma è noto che l'ossigenoterapia aumenti il rischio. Cenni storici: la patologia, identificata nel 1941, veniva descritta come prevalente nelle nurseries più moderne in cui si praticava ossigenoterapia. L'ossigenoterapia salva la vita del neonato ma su una retina immatura, la cui vascolarizzazione è incompleta, agisce come un forte stimolo angiogenico. Anche grazie all'introduzione dell'ossigenoterapia negli anni '60 aumenta la sopravvivenza dei neonati prematuri e così aumenta l'incidenza di fibroplasia retrolenticolare. Kinsey nel 1956 dimostra che ossigenoterapia con FiO2>50% per 4 settimane aumenta di tre volte il rischio di sviluppare ROP. Oggi si stima che interessi il 2- 4% dei bambini con peso alla nascita < 1000g. L'85% dei bambini affetti da ROP sviluppa piena vascolarizzazione senza gravi complicanze. Il trattamento standard può prevenire una grave perdita visiva nel 50% dei bambini colpiti da complicanze. Complessivamente, 6-10% delle ROP subisce una grave perdita visiva. La retina è uno degli ultimi tessuti a maturare: è senza vasi fino al IV mese di gestazione, poi dai vasi ialoidei del vitreo fino al disco ottico si sviluppano nuovi vasi che crescono verso la periferia. La periferia nasale è raggiunta dai vasi all'VIII mese di gestazione mentre la periferia temporale viene vascolarizzata circa un mese dopo la nascita nei bambini nati a termine.
Tra i fattori di rischio si annoverano:
- Prematurità: < 32 settimane di età postmestruale (e cioè la somma dell'età gestazionale e dell'età anagrafica del bambino)
- Peso alla nascita < 1500g
- Ossigenoterapia: tensione arteriosa 02 > 80mmHg fra la seconda e la quarta settimana di vita
Lo studio Cryo-ROP ha studiato l'incidenza di ROP in 4009 neonati con peso alla nascita < 1251g:
- 47% neonati nel range 1000-1251g
- 78% neonati nel range 750-999g
- 90% neonati < 750g
- 60% dei nati tra la 28° e la 31° settimana
- 80% dei nati prima della 28° settimana
Esiste una stadiazione:
- Stadio I: linea di demarcazione tra retina vascolare e retina avascolare
- Stadio II: la linea di demarcazione diventa una cresta rilevata
- Stadio III: proliferazione fibrovascolare lungo la cresta
- Stadio IV: distacco di retina trazionale parziale
- IVa: coinvolgimento maculare
- IVb: senza coinvolgimento maculare
- Stadio V: distacco di retina totale
Si parla poi di plus disease se, in qualunque stadio, sono presenti dilatazione e tortuosità vascolare: ciò è segno di malattia rapidamente progressiva. Inoltre, si classifica in base alla localizzazione:
- ZONA 1: cerchio centrato sulla papilla ottica con diametro uguale a due volte la distanza tra papilla e macula
- ZONA 2: cerchio con diametro che va dall'equatore temporale a un diametro discale dall'ora serrata
- ZONA 3: semiluna ("crescente") temporale della retina
La zona in cui è presente retinopatia ha significato prognostico: centrale è peggio.
Devono essere visitati:
- I neonati di peso inferiore a 1300g
- I neonati di peso compreso tra 1300 e 1800g se supplementati di ossigeno
La prima visita deve essere eseguita tra la 5° e la 7º settimana d'età:
- Se stadio < II: controlli ogni due settimane fino a completa maturazione della retina
- Se stadio III o maggiore: controllo settimanale fino a che la vascolarizzazione della retina è matura o si raggiunge lo stadio soglia, che indica la necessità di un trattamento laser
Per stadio soglia si intende: malattia stadio III in zona 1 o 2 per cinque ore contigue od otto ore non contigue (per "ore" si intende la divisione della retina in quadranti orari). Come in tutte le retinopatie ipossiche (come la retinopatia diabetica, che somiglia molto alla ROP per patogenesi) il trattamento prevede la crioterapia o la fotocoagulazione laser della retina anteriore avascolare: l'obbiettivo è rimuovere lo stimolo neoangiogenetico sacrificando la retina ischemica
Neuroftalmologia: il papilledema
La prof.ssa specifica: "la prima cosa da chiarire è che papilledema non è sinonimo di edema della papilla"1. Infatti, il papilledema è un edema bilaterale delle papille ottiche secondario ad un aumento della pressione intracranica: l'eziopatogenesi è di competenza neurologica, non oculistica. Anatomia del nervo ottico: circa 1,2 milioni di assoni convergono nella testa del nervo ottico, che è suddiviso in quattro porzioni:
- Intraoculare: lunga 1mm, è la più anteriore e si può esplorare con l'oftalmoscopio
- Intraorbitaria: lunga 25mm, decorre nel canale orbitario
- Intracanalicolare: lunga 9mm, decorre nella piccola ala dello sfenoide
- Intracranica: lunga 16mm, termina nel chiasma ottico
Patogenesi del papilledema: si arriva al papilledema per interruzione del flusso assoplasmatico da cause meccaniche e vascolari secondarie all'incremento dell'ICP (intracranial pressure). Il trasporto assonale, in presenza di stasi pressoria, viene interrotto. Esso si divide in lento e rapido e dipende in gran parte dai microtubuli. Eziologia del papilledema: masse emisferiche (soprattutto quelle in fossa cranica posteriore, che più facilmente possono provocare idrocefalo ostruttivo), pseudotumor cerebri2, meningite, ipertensione maligna. Un disco ottico normale (vedi Figura 4) è roseo, tondeggiante, ha margini netti e ben distinguibili con una parte piana e una parte escavata. La parte rosea prima dell'escavazione si chiama rima neurale ed è composta dagli assoni delle cellule gangliari retiniche che trasportano l'informazione visiva.
L'escavazione è ampia e distesa nell'occhio miope, piccola o addirittura assente nell'occhio ipermetrope. Nelle otticopatie glaucomatose si ha iperescavazione, mentre in altre otticopatie si ha un aumento del pallore senza un incremento dell'escavazione. Sono proposte le immagini istologiche di un nervo ottico normale e di uno edematoso. Nel nervo ottico normale si vede il caratteristico avvallamento, con gli assoni che attraversano la lamina cribrosa, mentre nel nervo ottico edematoso si nota un aumento della massa tissutale (da stasi assoplasmatica) con protrusione anteriore ed allargamento dello spazio subaracnoideo.