Le reazioni chimiche: trasformazioni fisiche e chimiche
Slide sulle reazioni chimiche. Il Pdf esplora le reazioni chimiche, differenziandole dalle trasformazioni fisiche, con esempi pratici e diagrammi esplicativi. Questo Pdf di Chimica per la scuola superiore, arricchito da esempi di combustione e decomposizione, offre una chiara introduzione ai concetti fondamentali.
Mostra di più29 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
LE REAZIONI CHIMICHE
I fenomeni naturali si possono raggruppare in una delle due categorie: TRASFORMAZIONI FISICHE Le sostanze non cambiano natura e non variano le loro proprietà caratteristiche (passaggi di stato, un oggetto che si rompe .. etc) TRASFORMAZIONI CHIMICHE Le sostanze cambiano natura e variano le loro proprietà caratteristiche (la combustione, la formazione della ruggine sul ferro, l'acido che corrode etc)
Laquid
Protochimica: dalla preistoria al III d.c.
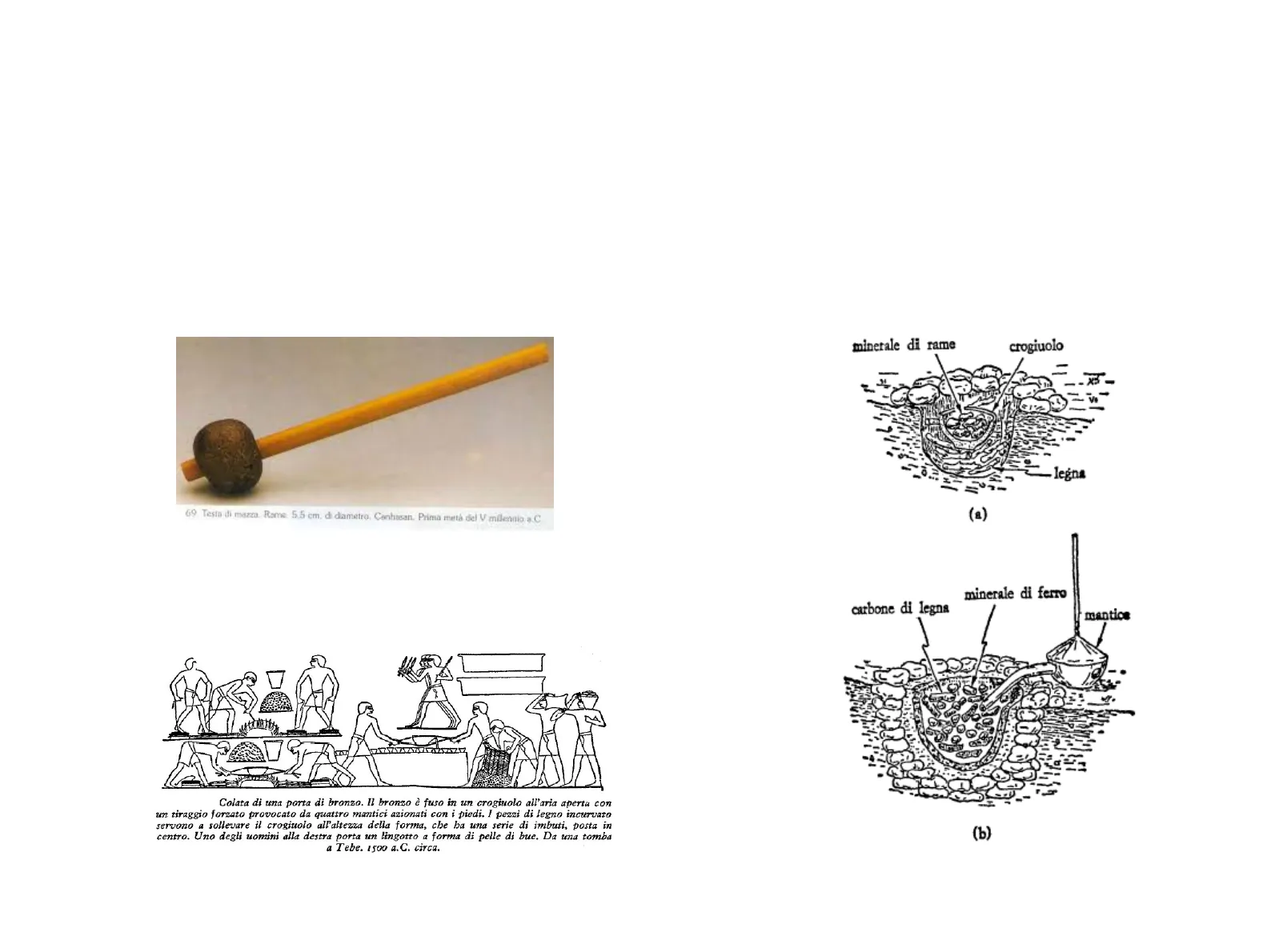
(il fuoco, i metalli, la terracotta, il vetro, i pigmenti etc) 69. Testa di mazza. Rame 5,5 cm. di diametro. Conhasan. Prima metà del V milennio a.C Colata di una porta di bronzo. Il bronzo è fuso in un crogiuolo all'aria aperta con un tiraggio forzato provocato da quattro mantici azionati con i piedi. I pezzi di legno incurvato servono a sollevare il crogiuolo all'altezza della forma, che ha una serie di imbuti, posta in centro. Uno degli uomini alla destra porta un lingotto a forma di pelle di bue. Da una tomba a Tebe. 1500 a.C. circa.
minerale di rame crogiuolo
- leģna (a)
minerale di ferro carbone di legna mantice (b) Riduzione dei minerali in metalli
Alchimia: IV-XVI secolo
Pseudoscienza il cui scopo era la trasformazione di alcuni metalli (rame, ferro, piombo etc) in argento e oro. La chimica e l'alchimia hanno scopi differenti ma hanno in comune molte tecniche, procedure e sperimentazioni.
Alchimia Egizia
Alessandro il Macedone (356 - 323 a.C) sognava l'unificazione sostanziale di due mondi differenti, quello occidentale e quello orientale, e lavorò a questo progetto fondando circa venticinque città, molte delle quali portano il suo nome, popolandole con veterani greci e creando così il mondo ellenistico, un misto di cultura greca e spiritualità orientale. Egli non riuscì pienamente nel suo progetto che però riuscì ad attuare più tardi Tolomeo I Sotere (367 -283 a.C.), In quest'ambiente, tra il I ed il IV secolo d.C., si realizzarono le condizioni ideali perché, dalla fusione di tecnologia egizia, misticismo caldeo, ebreo e persiano, e filosofia greca, nascesse e si evolvesse quella cultura ibrida sognata da Alessandro. Papiro X di Leida
Alchimia: IV-XVI secolo
L'Antico Egitto (ca. 330 aC.)
Scienza legata alla religione (Toth dio della saggezza è la fonte di ogni sapere chimico), diventa misteriosa, una scienza occulta ricca di simboli segreti. I sette metalli: oro, argento, mercurio, rame, ferro, stagno, piombo, erano in relazione con i sette astri: Sole, Luna, Mercurio, Venere, Marte, Giove, Saturno, ed entrambi connessi con le parti anatomiche e le viscere dell'uomo. Obiettivo principale degli alchimisti: trasmutazione dei metalli in oro. Con l'arrivo degli Arabi in Egitto il progresso dell'alchimia greco-egiziana rimase nelle mani degli arabi per circa 5 secoli. Si diffusero gli studi sulla trasmutazione dei metalli in oro (Giabir 760-815), solo intorno al 1000 cominciarono ad essere messi in discussione grazie agli studi del medico Avicenna.
LE REAZIONI CHIMICHE
Una reazione chimica è un processo dinamico in cui alcune specie chimiche, dette reagenti, interagiscono tra loro trasformandosi in specie chimiche diverse, dette prodotti di reazione. Una reazione chimica viene rappresentata simbolicamente mediante un'equazione di reazione, detta equazione chimica molecole (moli) H2 + 12 2 HI H I 1 + 1 H I H H I + I I Una reazione chimica implica la rottura di legami chimici tra gli atomi delle molecole dei reagenti e la formazione di nuovi legami tra gli stessi a formare molecole diverse Perché le reazioni chimiche avvengono? ?
LE REAZIONI CHIMICHE
REVERSIBILI
E' sempre possibile tornare alle condizioni iniziali, tali reazioni procedono fino al raggiungimento di una situazione di equilibrio dinamico. (A) IRREVERSIBILI Non è possibile in alcun modo tornare alle condizioni inizizioni, procedono fino al consumo totale di almeno uno dei reagenti. (B) A + B > C +D (A) CaCO3 (s) + CO2 (g) + H2O (1 ) + + Ca2+ (aq) + 2 HCO3- (aq) CO H CHO- HC HO HO 8 OH HO HOCH2 OH 15%-25% Lignin 235-32% Hemicelulose Cellulose CH OH 1 4 OH 0 HO 0 HO OH 4 OH OH OH C(s) + O2(g) + CO2(g) (B) A+ B = C +D OH 8 4
LE REAZIONI CHIMICHE
? Perché una reazione si verifica? ? Le molecole dei reagenti devono collidere affinché possano reagire tra loro e fornire i prodotti: maggiore è la frequenza degli urti e maggiore è la probabilità che le molecole possano reagire fra loro.
Teoria delle Collisioni
O 0 N O Prima della collisione Collisione Dopo la collisione Prima della collisione O O O 0 N Collisione Dopo la collisione Urto Efficace O 0 NO NO O 0 o N O o Urto Inefficace 1 2 Affinché una reazione si inneschi (cioè incominci a svolgersi) è necessario fornire una certa energia al sistema (energia di attivazione), mentre una volta che la reazione chimica è stata innescata l'energia di attivazione viene restituita all'ambiente e la reazione si svolge fornendo energia all'ambiente (esotermica) o sottraendo energia dall'ambiente (endotermica).
Reazioni esotermiche ed endotermiche: un esempio didattico qualitativo
Acqua e alcol: si percepisce un aumento di temperatura ALCOOL FFER 1000 ml ** Aceto e bicarbonato: si percepisce un raffreddamento del sistema
LE REAZIONI CHIMICHE
20 At 1 L'energia di attivazione è strettamente collegata alla velocità con cui si verifica una reazione. Energia di attivazione A differenza di Energia fra reagenti e prodotti B Maggiore è l'energia di attivazione, minore è la velocità di reazione (sx) Minore è l'energia di attivazione, maggiore è la velocità di reazione (dx) Ea.r = 203 KJ/mol Ea. f = 275 KJ/mol AH rxn = 72 KJ/mol Ea. f = 10.7 kJ/mol Ear =210.5 kJ/mol CINETICA AH rxn =- 199.8 KJ/mol
LE REAZIONI CHIMICHE
20 At CINETICA Esamina i fattori che influiscono sul tempo necessario perché una reazione giunga a completezza. La TEMPERATURA, la NATURA e la CONCETRAZIONE dei reagenti influenzano la velocità di reazione Vr generalmente aumenta all'aumentare della concentrazione dei reagenti (A) Vr generalmente aumenta all'aumentare della temperatura (B) Vr generalmente diminuisce con il procedere della reazione (C) (A) CONCENTRAZIONE (B) T (K) B 100- 80 Velocità di reazione 60 40 20 0 0 1 2 3 4 minuti (C)
LE REAZIONI CHIMICHE
20 At Alcune reazioni sono molto rapide, addirittura violente (come le esplosioni), mentre altre sono talmente lente che possono necessitare di tempi lunghissimi prima di svolgersi completamente (ad esempio anni o secoli). Esplosione Corrosione Ossidazione del Fe Combustione della carta e del legno a T.A. Velocità di Reazione
LE REAZIONI CHIMICHE
18 At Perché nel nostro corpo la combustione dello zucchero avviene a 37℃, mentre fuori da esso la temperatura deve superare i 200℃? https://www.youtube.com/watch?v=u8IXP9ouJtE ? https://www.youtube.com/watch?v=E0VUIE5zfYc Un enzima è una proteina in grado di catalizzare una reazione chimica. Il processo di catalisi indotto da un enzima (come da un qualsiasi altro catalizzatore) consiste in una accelerazione della velocità della reazione. in assenza dell'enzima in presenza dellenzima energia di attivazione in assenza dell'enzima energia di attivazione in presenza dell'enzima energia reagenti energia complessiva rilasciata durante la reazione prodotti coordinate di reazione
LE REAZIONI CHIMICHE
18 20 At L'uso di catalizzatori fa sì che processi che avverrebbero molto lentamente si compiano in tempi relativamente brevi.
Caratteristiche del Catalizzatore
Tutti i catalizzatori rispecchiano regole basilari e comuni
- Il catalizzatore compare chimicamente inalterato alla fine della reazione.
- agisce in piccole quantità.
- non altera l'equilibrio nelle reazioni reversibili.
- possiede maggiore o minore specificità nell'agire con sistemi diversi
Disattivazione del Catalizzatore
Durante il procedere della reazione, il catalizzatore può perdere progressivamente la sua efficacia, ad esempio a causa di stress termico (degradazione termica) o a causa dell'intervento di sostanze che si depositano su di esso, bloccando i centri attivi (sporcamento) o per un fenomeno chiamato avvelenamento.
LE REAZIONI CHIMICHE
Esempio: Marmitta Catalitica
1 scintilla HC+O2 CO2 + H2O + calore combustione ideale scintilla combustione reale HC + O2 + N2 CO2 + H2O ( HCpar + CO + NO +) calore 2400 °℃, 10 atm HC par CO2 CO H2O NO A N2 1 Marmitta catalitica Catalizzatore riducente Catalizzatore ossidante Struttura di ceramica a nido d'ape,rivestita di una pellicola sottile di metalli catalizzatori (palladio Pd, il rodio Rh e il platino Pt.) Pd HCpr + CO + O2 CO2 + H2O + calore Rh 2NO N2+ 02 1
Il dentifricio di elefante
Esperienza didattica sulla catalisi: la decomposizione dell'acqua ossigenata. NE JORDRAI Acqua ossigenata, Detersivo, Lievito di birra essiccato, Acqua tiepida
LE REAZIONI CHIMICHE
2 Durante lo svolgimento di una reazione chimica, alcuni o tutti i legami chimici associati alle specie reagenti si rompono, assorbendo una certa quantità energia, quindi si formano nuovi legami chimici grazie al rilascio di una certa quantità energia. A reazione avvenuta comunque una certa aliquota di energia è conservata dalle specie prodotte. E Prodotti < E Reagenti E' stata rilasciata verso l'ambiente una certa quantità di energia E Prodotti > E Reagenti E' stata assorbita dall'ambiente una certa quantità di energia TERMODINAMICA SPONTANEA NON SPONTANEA
LE REAZIONI CHIMICHE
Le reazioni chimiche avvengono quando sono soddisfatte contemporaneamente due condizioni: quella di essere intrinsecamente possibili (termodinamicamente possibili) e quella di compiersi in un tempo finito (cineticamente possibili). HH YH'H Energia libera, G E. a 0-0 I H H HH HH |AG .< 0 O Coordinata di reazione Mentre la termodinamica chimica esamina le condizioni che devono essere soddisfatte perché una certa reazione avvenga spontaneamente, la cinetica chimica esamina i fattori che influiscono sul tempo necessario perché una reazione giunga a completezza
LE REAZIONI CHIMICHE
Le reazioni che producono calore si dicono Esotermiche (1) Le reazioni che assorbono calore si dicono Endotermiche (2) Esempio: (1) La combustione è una reazione fra un combustibile (spesso contenente carbonio e/o idrogeno) e un comburente (es. ossigeno) in cui si libera un'elevata quantità di energia sotto forma di calore. C(s) + O2(g) CO (g) + calore '21 In una reazione chimica che si verifica a pressione costante, il calore scambiato dal sistema con l'ambiente esterno può essere definito dall'Entalpia. In generale l'Entalpia esprime la quantità di energia interna che un sistema termodinamico può scambiare con l'ambiente. Nelle reazioni esotermiche si ha: AH<0