L'Atomo e le Molecole: composizione, numero atomico ed elementi
Slide sull'Atomo e le Molecole. Il Pdf è una presentazione che introduce i concetti di atomo e molecola, spiegando la loro composizione e le proprietà fondamentali. Adatto per la scuola media, tratta di chimica di base, con esempi di elementi comuni.
Mostra di più30 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
L'atomo
L'atomo
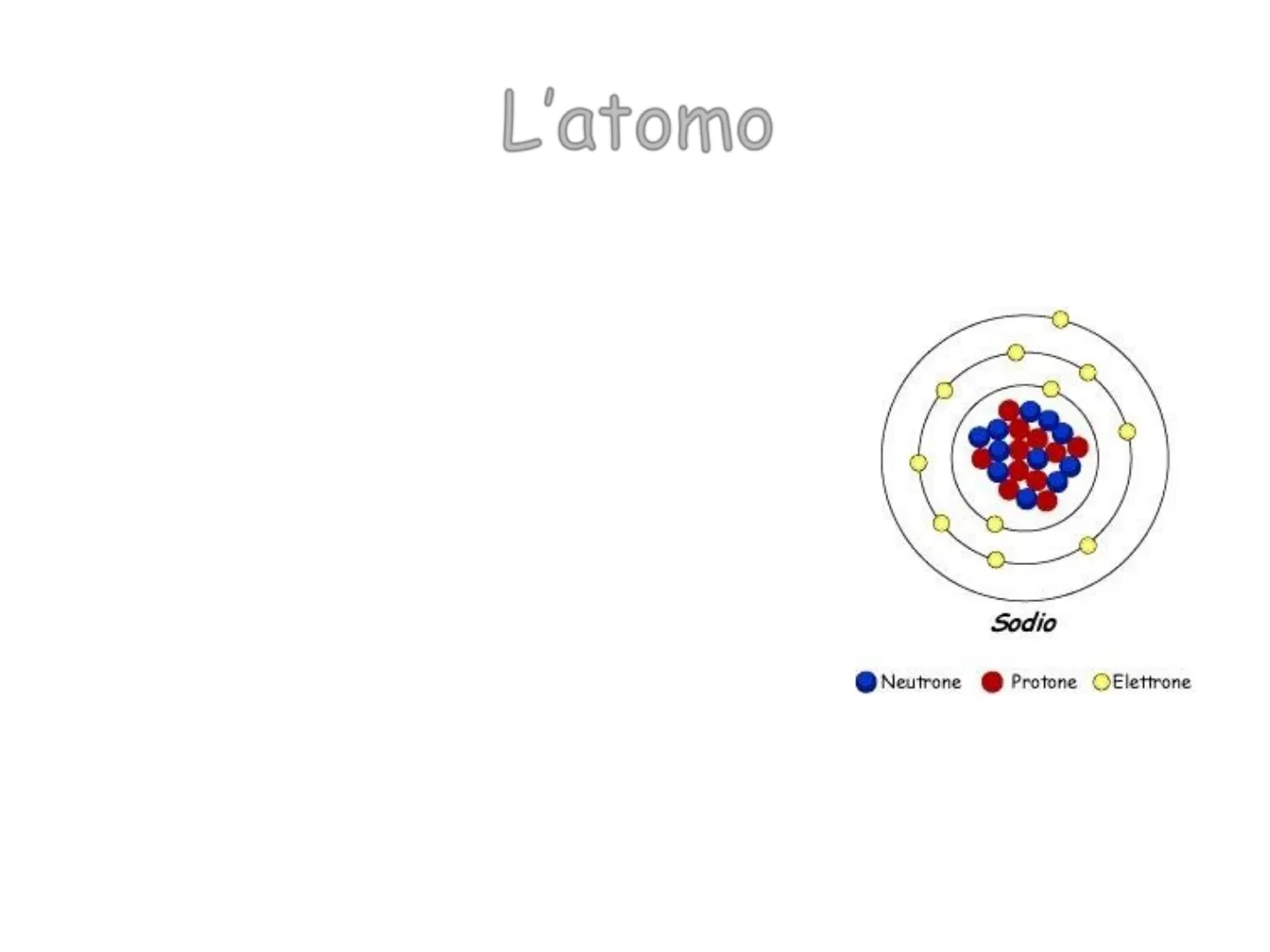
- L'atomo, la particella che come un mattone costituisce tutta la materia, non è un corpicciolo semplice. Esso è a sua volta composto da particelle elementari piccolissime: i protoni, i neutroni e gli elettroni. Sodio . Neutrone C Protone OElettrone
Protoni e Neutroni
- I protoni e i neutroni formano insieme quello che possiamo definire il cuore dell'atomo: il nucleo. +Protoni e Neutroni
- Queste due particelle hanno più o meno la stessa massa, cioè sono formate da una quantità di materia quasi uguale. Il protone, però, è diverso dal neutrone perché ha una proprietà, chiamata carica elettrica positiva, che il neutrone non possiede.
Gli elettroni
- Intorno al nucleo si muovono rapidissimamente altre particelle: gli elettroni.
Massa degli elettroni
- Essi hanno una massa così piccola che ne Servono 1836 per uguagliare la massa di un protone. Anche gli elettroni hanno una carica elettrica, ma essa è diversa da quella del protone: è una carica elettrica negativa. Nucleo Elettroni
L'atomo neutro
- In un atomo in condizioni normali il numero degli elettroni è sempre uguale a quello dei protoni: a un certo numero di cariche positive corrisponde un ugual numero di cariche negative. L'atomo, dunque, risulta neutro, né positivo né negativo. e nº H P no me e e e e
Atomo Nucleo Elettroni Numero atomico Modello Atomico Elettronico Protoni Neutroni Tavola periodica Configurazione Elettronica
Gli atomi sono tutti uguali tra loro?
- Pur essendo tutti formati dalle stesse particelle, gli atomi non sono tutti uguali tra loro: alcuni Sono più piccoli, altri più grandi. La piccolezza o la grandezza di un atomo dipende dal numero di protoni del suo nucleo.
Dimensioni degli atomi
- L'atomo più piccolo ha il nucleo composto da un solo protone; il più grande in natura possiede ben 92 protoni. + - e P
Numero atomico
- Questi atomi hanno un diverso numero atomico termine che indica quanti protoni sono presenti nel nucleo: il primo ha numero atomico 1 perché ha un solo protone e l'ultimo ha numero atomico 92 perché ha 92 protoni. Numero atomico 7 N Azoto 14,0067 [He] 2s2 2p3 Simbolo atomico Nome dell'elemento Peso atomico Configurazione elettronica
Gli atomi hanno un nome?
- Il numero atomico permette di distinguere un atomo da un altro: questo consente anche di dare un nome a ciascuno di essi. Numero atomico 7 N Azoto 14,0067 [He] 2$2 2p3 Simbolo atomico Nome dell'elemento Peso atomico Configurazione elettronica
Nomi degli atomi
- L'atomo più piccolo, quello con un solo protone, è l'idrogeno; il più grande in natura si chiama uranio e ha 92 protoni. L'atomo che possiede 7 protoni è quello dell'azoto, una sostanza presente nell'aria; l'atomo con numero atomico 8, cioè con 8 protoni, è l'ossigeno, il gas che ci permette di respirare. Litio
Elementi chimici
- Imparerai il nome di molti altri atomi: carbonio, rame, ferro, oro, argento, sodio, cloro ... Essi si definiscono elementi chimici. O 6 protoni +6 neutroni O L + I elettrone + protone neutrone Atomo di Carbonio
I simboli degli elementi chimici
- Ogni elemento chimico, per brevità, è indicato con un simbolo, che deriva dal nome dell'atomo. Ogni simbolo è formato dalla prima o dalle prime due lettere del nome dell'atomo, per non creare confusione tra atomi i cui nomi hanno la stessa iniziale. 1 H Hydrogen 1.00794 15 13.5984 24 'S Cr Chromium 51.9981 [A]3d'45 6.7665 80 Hg Mercury 200.50 7 N Nitrogen 14.0067 1822172p3 14.5341 10.4375
Esempi di simboli chimici
- Per esempio il simbolo del carbonio è C (si legge ci), quello del calcio è Ca (si legge ci-a) e quello del cloro è Cl (si legge ci- elle). Ci sono poi alcuni elementi il cui simbolo è molto diverso da quello del loro nome. 6 C Carbon 12 0107 18242p2 11 2803 20 Ca Calcium 40.078 [Arjas? 6.1132 17 p" CI Chlorine 35.453 [Na]s Jp" 12.9676
Simboli derivati dal latino
- Così il simbolo dell'oro è Au, perché è ricavato dal termine latino aurum; quello del rame è Cu, perché gli antichi romani chiamavano il rame cuprum. 79 Sự Au Gold 195.96655 [Xejat"Sd ds 9 2255 29 'Sın Cu Copper 63.546 7.7264
La Tavola degli Elementi
- La tavola periodica degli elementi è lo schema col quale vengono ordinati gli atomi sulla base del loro numero atomico. Ideata dal chimico russo Mendeleev nel 1869, inizialmente contava numerosi spazi vuoti, previsti per gli elementi che sarebbero stati scoperti in futuro, taluni nella seconda metà del 1900.
http://www.dayah.com/periodic/
Quando gli atomi si uniscono: La Molecola
- Gli atomi hanno la capacità di unirsi tra loro formando le molecole. Ma che cos'è una molecola? E' la più piccola particella di una sostanza che ne conserva tutte le proprietà. H H C H H
Esempio di molecola: l'acqua
- Un esempio di molecola è la molecola dell'acqua. Se potessimo spezzare questa particella, i suoi frammenti non sarebbero più acqua ma altre sostanze. La molecola dell'acqua è infatti costituita da tre atomi: due atomi di idrogeno (H) e uno di ossigeno (0) legati tra loro. H H O Molecola d'acqua
Molecole di ammoniaca e ossigeno
- Così accade per tutte le sostanze. La molecola dell'ammoniaca, cioè la più piccola quantità di materia che ha le caratteristiche di questa sostanza, per esempio, è formata da un atomo di azoto (N) e tre di idrogeno (H) tra loro uniti; la molecola dell'ossigeno, il gas che respiriamo, è formata da due atomi di ossigeno (0) legati tra loro. Molecola di ossigeno O2
Le Formule Chimiche
- Per indicare le molecole si usano segni convenzionali: si scrivono i simboli degli atomi che le costituiscono e in basso a destra di ogni simbolo si indica un numero, che corrisponde al numero di atomi di quell'elemento presenti nella molecola stessa.
Esempi di formule chimiche
Le Formule Chimiche
| SOSTANZA | SIMBOLO | COME SI LEGGE | SIGNIFICATO |
| ANIDRIDE CARBONICA | CO2 | ci-o-due | 1 atomo di carbonio e due atomi di ossigeno |
| GLUCOSIO | C6H12º6 | ci-sei-acca-dodici-o-sei | 6 atomi di carbonio 12 atomi di idrogeno 6 atomi di ossigeno |
| ACQUA | H20 | accadue-o | 2 atomi di idrogeno 1 atomo di ossigeno |
| CLORURO DI SODIO | NaCl | enne-a-ci-elle | 1 atomo di sodio 1 atomo di cloro |
Elementi e Composti
- Osservando gli atomi che compongono una molecola possiamo distinguere tutte le sostanze in due grandi gruppi: Gli Elementi I Composti
Elementi
- Gli elementi sono sostanze la cui molecola è costituita da atomi tutti uguali tra loro. L'ossigeno che respiriamo, per esempio, è un elemento, perché la sua molecola è formata da due atomi di ossigeno. Anche il rame è un elemento, perché è costituito da molecole formate ognuna da un atomo di rame. Molecola di ossigeno O2
Composti
- I composti sono sostanze la cui molecola è costituita da atomi tra loro diversi. Il sale da cucina (o cloruro di sodio), in cui sono presenti atomi di cloro e atomi di sodio, è appunto un composto, e così l'acqua e tante altre. CI - Na + Sale da cucina
Metano (CH4)
Aspetto a temperatura ambiente: gassoso. Utilizzi: Il metano viene utilizzato in cucina, nella produzione di acqua calda e nel riscaldamento autonomo e centralizzato degli edifici. Viene utilizzato anche nel settore industriale, in particolare in quello meccanico e metallurgico. Pericolosità/tossicità: Estremamente infiammabile F+
Permanganato di potassio (KMNO4)
Aspetto a temperatura ambiente: solido cristallino di colore viola scuro. Utilizzi: Viene utilizzato come comburente; in soluzione diluita, come agente disinfettante deodorante; come collutorio, e come antidoto per l'avvelenamento da fosforo. Pericolosità/tossicità: NOCIVO COMBURENTE DANNOSO PER L'AMBIENTE
Perossido di idrogeno (H2O2)
Aspetto a temperatura ambiente: Liquido incolore e viscoso. HO 2 2 H 0-0 H Utilizzi: In soluzione acquosa fino al 5% è utilizzato come sbiancante; in soluzione ancora più diluita (3%) è usato come disinfettante per escoriazioni e ferite. Pericolosità/tossicità: COMBURENTE CORROSIVO
Magnesio (Mg)
Aspetto a temperatura ambiente: Metallo di colore bianco argenteo. Utilizzi: Il magnesio viene utilizzato principalmente nei rivestimenti delle fornaci per la produzione di ferro e acciaio, metalli non ferrosi, vetro e cemento. Pericolosità/tossicità: FACILMENTE INFIAMMABILE