Cinetica enzimatica e reazioni biochimiche: principi e influenza del pH
Slide sulla cinetica enzimatica e le reazioni biochimiche di condensazione e idrolisi. Il Pdf esplora i principi della cinetica enzimatica, le reazioni di condensazione e idrolisi, la stabilità molecolare e l'idrolisi dell'ATP, con un focus sull'influenza del pH sull'attività enzimatica e la costante catalitica (Kcat), utile per lo studio universitario di Biologia.
Mostra di più32 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
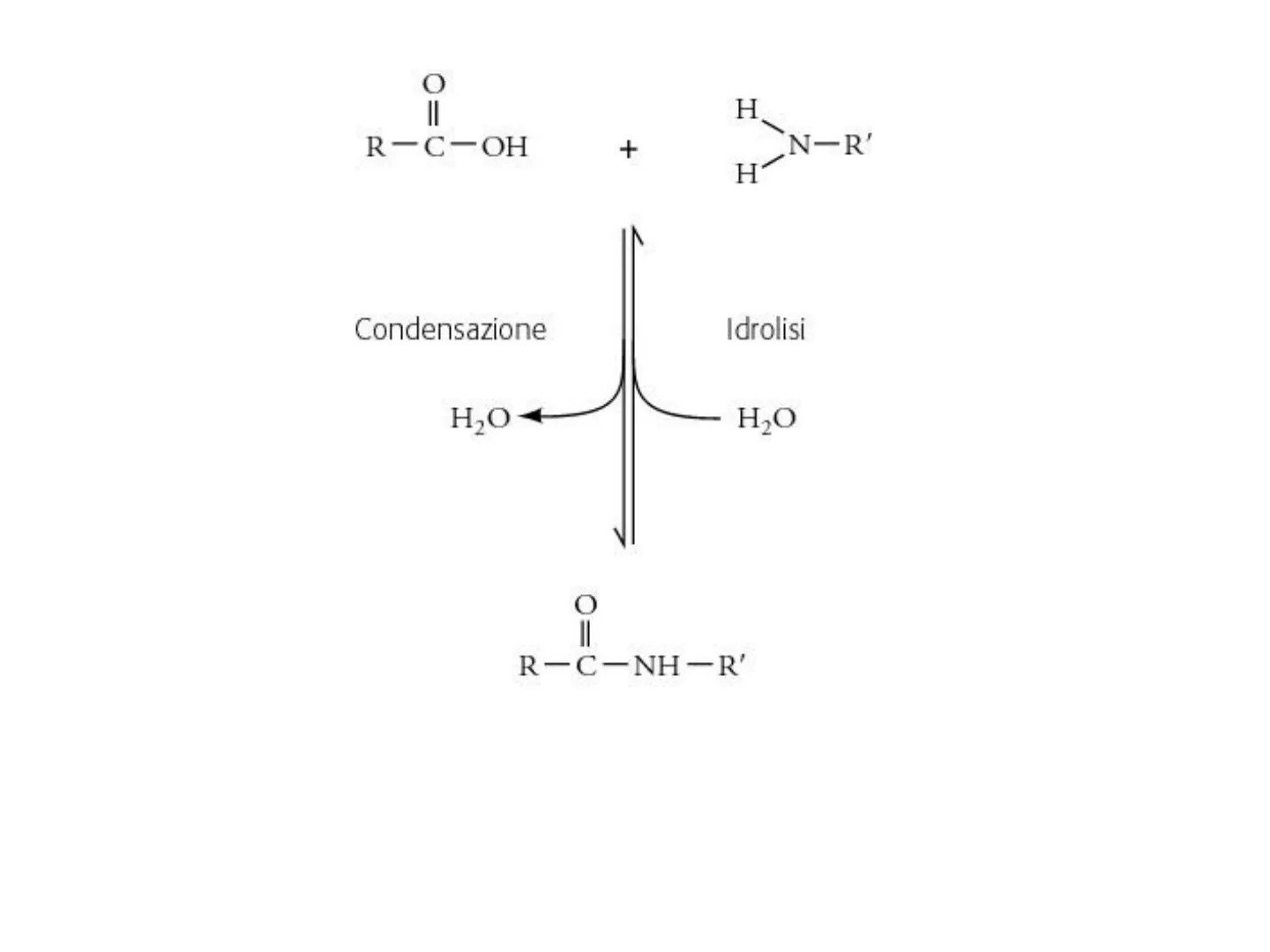
Reazioni di Condensazione e Idrolisi
O
ǁ
H
R-C-OH
+
N-R'
H
Condensazione
Idrolisi
H2O
H2O
O
R-C-NH-R'
Una trasformazione chimica - come l'idrolisi o la condensazione
di un legame peptidico - non può avvenire spontaneamente nella
cellula in condizioni fisiologiche di pH 7.0, temperatura 37°℃ e
pressione di 1 atmosfera.
La stabilità di una molecola in condizioni fisiologiche è tanto
maggiore quanto più elevato il livello di energia dello stato di
transizione necessario perché la molecola subisca una
modificazione chimica.
Ad esempio:
ATP
ADP + Pi
L'ATP richiede un'energia di attivazione relativamente alta per
idrolizzarsi in ADP + Pi.
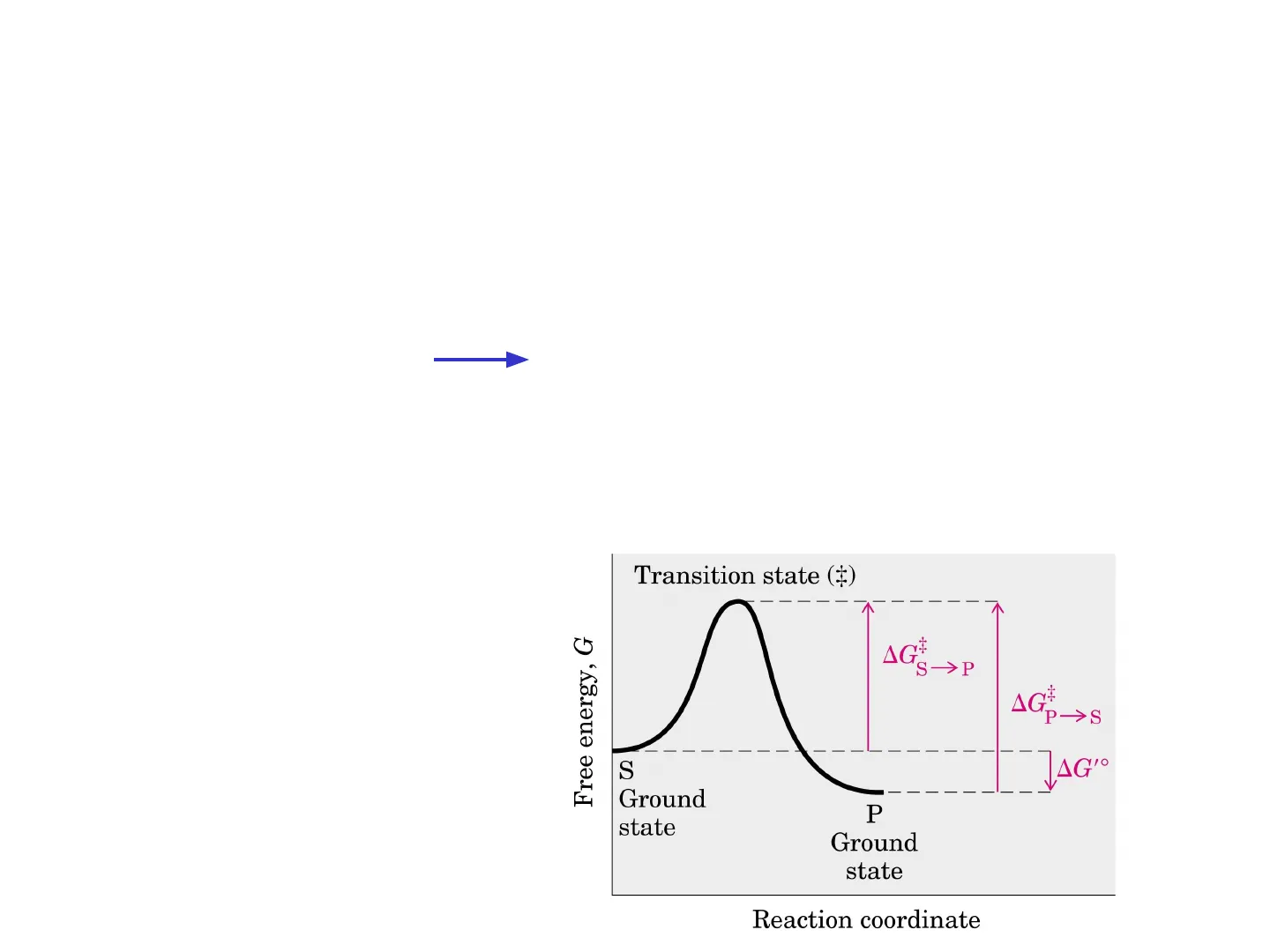
Energia Libera e Coordinata di Reazione
Stato di Transizione e Stati Fondamentali
Transition state (¿)
Free energy, G
S->P
AG
P->S
"JAG"O
S
Ground
state
P
Ground
state
Reaction coordinate
Effetto dell'Enzima sull'Energia Libera
Transition state (¿)
Free energy, G
S->P
AGF
P->S
JAG10
S
Ground
state
P
Ground
state
Reaction coordinate
Con enzima:
Transition state (¿)
Free energy, G
AG
uncat
¢
AG+
cat
-ES -EP-
S
P
Reaction coordinate
L'enzima:
- riduce
l'energia di
attivazione della
reazione (AG*);
- non altera
l'equilibrio della
reazione (K'
e
AG'º).
eq
Enzimi: Catalizzatori Biologici
- Gli enzimi sono proteine ed RNA precursori nel processo
autocatalitico di maturazione dell'RNA detto "splicing". - L'enzima aumenta la velocità di una reazione chimica
diminuendo l'energia di attivazione. - L'enzima non altera i livelli di energia libera del substrato e del
prodotto allo stato basale. - L'enzima non altera l'equilibrio della reazione chimica.
- L'enzima non viene consumato nel corso della reazione
chimica. - L'enzima ha substrati specifici.
Modelli di Interazione Enzima-Substrato
(a) No enzyme
0
Substrate
(metal stick)
Transition state
(bent stick)
Products
(broken stick)
Free energy, G
AG+
S
F
(b) Enzyme complementary to substrate
Fischer, 1894
Magnets
Free energy, G
AG+
10#
1
S
AGM
P
ES
(c) Enzyme complementary to transition state
Koshland, 1958
++
Free energy, G
AGM
++
uncat
S
ES
P
+
Reaction coordinate
L'enzima induce una molecola di substrato ad esso legato ad
adottare una conformazione simile allo stato di transizione.
Energia di Legame e Cambiamento Conformazionale
+
-Energia di legame (4G,
)
B
AG
B
è la somma delle interazioni (legami deboli) che si
stabiliscono tra enzima e substrato, e che cedono una dote di
energia necessaria ad abbassare l'energia di attivazione
(AG*)
della reazione chimica.
Di fatto, l'enzima induce un cambio conformazionale del substrato
utile a velocizzare la trasformazione del substrato in prodotto
perchè riduce l'energia di attivazione della reazione.
Free energy, G
AGF
AGB
uncat
AG*
cat
-ES -EP --
S
P
Reaction coordinate
Interazioni Deboli Enzima-Substrato
Le interazioni deboli che intervengono tra enzima e
substrato portano in dote l'energia di legame necessaria
per ridurre l'energia di attivazione.
| Tipo di legame | Energia di stabilizzazione (KJ/mole) |
|---|---|
| Legami idrogeno | 8 - 21 |
| Interazioni ioniche attrattive | 42 |
| Interazioni ioniche repulsive | - 21 |
| Interazioni idrofobiche | 4 - 8 |
| Interazioni di van der Waals | 4 |
Complesso Enzima-Substrato (ES)
Il complesso Enzima-Substrato è un intermedio della reazione
catalizzata da enzima.
+
+
E
S
ES
E
P
L'enzima lega il substrato a livello del proprio sito catalitico tramite
legami deboli (legami idrogeno, interazioni elettrostatiche o
idrofobiche, forze di van der Waals). Tale associazione determina:
- La corretta posizione ed orientamento del substrato verso i residui
amminoacidici catalitici dell'enzima;
- La desolvatazione del substrato;
-La modifica conformazionale del substrato favorevole alla
trasformazione in prodotto.
Classificazione degli Enzimi
La maggior parte degli enzimi catalizza il
trasferimento di elettroni, atomi o gruppi
funzionali.
Esiste una classificazione internazionale degli
enzimi distinti in categorie differenti in base al
tipo di reazione di trasferimento, donatore del
gruppo o accettore del gruppo.
Categorie Enzimatiche
ENZIMI: CLASSIFICAZIONE (http://www.expasy.org/enzyme)
- Ossidoriduttasi: reazioni redox per trasferimento di equivalenti riducenti, quali
elettroni, atomi d'idrogeno o ioni idruro ( :H" ). Es. lattato deidrogenasi, glucosio
6-fosfato deidrogenasi. - Transferasi: trasferimento di gruppi funzionali (fosforici, acilici, glicosilici,
sulfidrilici, metilici). Es. esochinasi. - Idrolasi: reazioni di idrolisi per trasferimento di gruppi funzionali ad H,0.
Es. proteasi, nucleasi, fosfatasi. - Liasi: formazione di doppi legami per sottrazione di gruppi o, viceversa, scissione
di doppi legami per addizione di gruppi. Es. aldolasi, citrato sintasi. - Isomerasi: trasferimento di gruppi all'interno di molecole per formare isomeri.
Es. trioso-fosfato isomerasi. - Ligasi: formazione di legami C-C, C-S, C-O, C-N, mediante reazioni di
condensazione accoppiate a scissione di ATP o cofattori simili. Es. DNA ligasi.
Cofattori Enzimatici
Un enzima può essere coadiuvato nella catalisi
enzimatica da componenti chimici addizionali detti
cofattori.
I cofattori possono essere ioni inorganici (es. Fe2+
, Mg
2+
oppure complesse molecole organiche dette
coenzimi. Molte vitamine sono precursori di
coenzimi.
Un cofattore legato covalentemente all'enzima è
definito gruppo prostetico.
Il complesso enzima-cofattore è definito oloenzima.
Cinetica Enzimatica
La cinetica enzimatica è una metodica d'analisi che misura la
velocità di una reazione chimica catalizzata da enzima.
La velocità di una reazione chimica catalizzata da un enzima
è misurata come quantità di prodotto che si forma nell'unità di
tempo in funzione della concentrazione di substrato.
0,5[P] 1[P] 1,5[P] 2[P] 2,5[P] 2,5[P]
0
0
1[S]
2[S]
3[S]
4[S]
5[S]
6[S]
[E]
Velocità di Reazione in Funzione della Concentrazione di Substrato
Velocità di una reazione enzimatica in funzione di [S]
La curva è un'iperbole rettangolare.
La velocità della reazione è
direttamente proporzionale alla
concentrazione
di
substrato
quando questo è presente in
concentrazioni iniziali basse. La
reazione è di primo ordine
rispetto al substrato in questa
parte della curva.
V ([P]/ min)
Initial velocity, Vo (M/min)
Ordine zero
Primo ordine
[S]
Substrate concentration, [S] (mM)
Per alte concentrazioni di substrato, l'enzima viene saturato da
questo, e la velocità della reazione diventa indipendente da ulteriori
aumenti della concentrazione di substrato. A questo punto la reazione
diventa di ordine zero rispetto al substrato.
Formazione del Complesso ES
E+S > E+P
In base all'analisi della cinetica enzimatica in funzione della [S] si
osserva:
Initial velocity, Vo (M/min)
Vmax
V
0
enzima saturo: la velocità della
reazione è indipendente da [S].
[S]
Substrate concentration, [S] (mM)
Quindi, si può formulare l'ipotesi di formazione di un complesso
ES come tappa intermedia della reazione enzimatica:
E + S
ES
E + P
Variazione delle Concentrazioni nel Tempo
Variazione della concentrazione di enzima libero [E], del
substrato [S] e del complesso enzima-substrato [ES] in
funzione del tempo di reazione.
[So]
Concentrazione
[S]
[P]
[E]= []+ [ES]
d[ES]
=0
de
[ 日 ]
[ES]
Tempo
Nella fase iniziale della
reazione enzimatica la
concentrazione ES
rimane costante =
stato stazionario.
Stato Stazionario della Reazione Enzimatica
Stato stazionario di una reazione enzimatica
Nelle fasi iniziali di una reazione catalizzata da un enzima si
forma un complesso ES che rimane costante nella
concentrazione finchè c'è substrato disponibile.
Pertanto, si può definire stato stazionario di una reazione
enzimatica quello in cui la concentrazione del complesso ES
( [ES] ) resta costante nel tempo.
E + S
ES
E + P
Poiché la [ES] è costante allo stato stazionario, la velocità di
formazione di ES è uguale alla velocità di dissociazione di ES.
Velocità di una Reazione Chimica
La velocità di una reazione chimica dipende dalla
concentrazione dei reagenti e dalla costante di velocità (k).
La costante di velocità (k) indica la probabilità che la reazione
avvenga in condizioni standard di pH, temperatura e
concentrazione molare. Ad es. : k = 0,03 s indica che il 3%
di quantità di substrato è convertito in prodotto in un secondo.
Per la reazione unimolecolare:
S
k
P
l'equazione di velocità è V = k [S]
Per la reazione a due substrati:
S + S2
k
P
l'equazione di velocità è V= k [S ] [S ]
Equazione di Michaelis-Menten
E' l'equazione della velocità di una reazione a
singolo substrato catalizzata da un enzima.
Vmax
max
[S]
Vo
0
-
K + [S]
mV.
max
[S]
Vo =
0
K + [S]
Se Km = [S]
V = Vmax [S] = Vmax [S]
[S]+ [S]
2[S]
dividendo per [S], ne deriva che:
Km= [S] quando V = Vmax
2
Km è la concentrazione di substrato alla quale la velocità della
reazione enzimatica è pari alla metà della velocità massima.
E' espressa come unità di moli/ litro.
Derivazione di Km
V =
max
K + [S]
m
Se Vo= Vmax
2
Vmax = Vmax [S]
2
Km + [S]
Dividendo per Vmax, ne deriva che:
1 = [S]
2
Km + [S] e risolvendo per Km :
Km + [S] = 2[S]; e quindi:
Km= [S]
Km è la concentrazione di substrato alla quale la velocità della
reazione enzimatica è pari alla metà della velocità massima.
E' espressa come unità di moli/ litro.
Curva della Velocità Iniziale
Curva dell'andamento della velocità iniziale (Vo) della
reazione in funzione della concentrazione iniziale del
substrato.
V
max
Prodotto
nell'unità
di tempo
Initial velocity, Vo (M/min)
1
1
¿V,
max
1
Km
m
Substrate concentration, [S] (mM)
Concentrazione
di substrato
Parametri Km e Vmax
Vmax e Km sono parametri calcolabili sperimentalmente.
Tali parametri misurati in condizioni standard consentono
di valutare, caratterizzare e confrontare l'efficienza
catalitica di enzimi diversi.
| table 8-6 | ||
|---|---|---|
| Km for Some Enzymes and Substrates | ||
| Enzyme | Substrate | Km (mm) |
| Catalase | H2O2 | 25 |
| Hexokinase (brain) | ATP | 0.4 |
| D-Glucose | 0.05 | |
| D-Fructose | 1.5 | |
| Carbonic anhydrase | HCO3 | 26 |
| Chymotrypsin | Glycyltyrosinylglycine | 108 |
| N-Benzoyltyrosinamide | 2.5 | |
| ß-Galactosidase | D-Lactose | 4.0 |
| Threonine dehydratase | L-Threonine | 5.0 |
Diagramma di Lineweaver-Burk
Il diagramma di Lineweaver -Burk è la trasformazione
lineare dell'equazione di Michaelis-Menten ed è utile
per determinare i valori di Km e Vmax graficamente.
Plot V0 vs [S]
Plot Lineweaver - Burk
(doppi reciproci)
V
max
Initial velocity, Vo (M/min)
-
VouM/min
1
1
V.
max
1
1
1
1
Km
m
[S]mM
Km
Substrate concentration, [S] (mM)
Km
Slope
=
V.
max
1
V max
Inibitori Enzimatici
Composti in grado d'interferire con una reazione enzimatica
sono detti inibitori enzimatici.
L'inibizione enzimatica può essere:
- Competitiva se l'inibitore previene il legame del substrato
all'enzima libero competendo direttamente con il substrato per il
legame al sito catalitico dell'enzima.
-Incompetitiva se l'inibitore si lega al complesso
Enzima-Substrato ma non all'enzima libero, ed impedisce la
catalisi presumibilmente per alterazione del sito catalitico (il
complesso ESI è di fatto cataliticamente inattivo).
-Di tipo misto (non competitiva) se l'inibitore si lega sia
all'enzima libero che al complesso Enzima-Substrato ed
impedisce al reazione catalitica.