Il destino del piruvato: ossidazione e ciclo di Krebs in Biologia
Documento di Nicoletta Bianchi sul destino del piruvato. Il Pdf esplora l'ossidazione del piruvato e il suo ruolo nel ciclo di Krebs, con diagrammi esplicativi, utile per lo studio universitario di Biologia.
Mostra di più16 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Il destino del piruvato
Ossidazione del piruvato
Nella lezione di oggi continuiamo ad analizzare il destino del Piruvato. Nella lezione precedente abbiamo visto come il piruvato, insieme ad altri metaboliti come il glucosio6 fosfato e l'acetil coenzima A, sia il crocevia di varie reazioni metaboliche che convogliano in altre vie. Abbiamo visto l'importanza del piruvato nella fermentazione lattica, sia in contesti fisiologici che tumorali, e soprattutto il piruvato verrà affrontato nelle vie cataboliche. Dunque, per concludere il percorso di ossidazione dei carboidrati, vediamo come il piruvato venga indirizzato verso la produzione di energia. Quando abbiamo parlato della glicolisi, abbiamo sottolineato come il piruvato, quale prodotto finale della glicolisi, sia comunque un composto che contiene ancora parecchia energia, siccome non siamo ancora arrivati a degradarlo completamente a CO2 e H2O come avverrà nella catena di trasporto degli elettroni; ancora, abbiamo visto che quando il piruvato si trasforma in lattato, può rappresentare il carburante convogliato sul fegato per generare glucosio e quindi riciclare energia da questa molecola. Oggi vedremo come, in presenza di ossigeno, il piruvato segua la via del ciclo di Krebs.
Innanzitutto, con la glicolisi e la fermentazione lattica noi siamo localizzati nel citoplasma, quindi gli enzimi di queste vie sono a livello del citosol; invece, le reazioni riguardanti l'ossidazione del piruvato avvengono nella matrice mitocondriale; quindi il piruvato, accumulato nella glicolisi, deve entrare nel mitocondrio. Per quanto riguarda le membrane mitocondriali, possiamo dire che i mitocondri presentano una doppia membrana: una interna ed una esterna. Di fatto, le molecole che possono superare la prima Glucose (glycolysis) - membrana, sono molecole che possono raggiungere un certo peso molecolare (comunque Pyruvate LDH Lactate (fermentation) - piccole molecole, ma non così piccole); si tenga, cytosol inoltre, presente che la membrana mitocondriale esterna possiede una serie di trasportatori che, MPC1/ MPC2 mitochondria come per le porine, aiutano il trasporto dei Pyruvate metaboliti dal lato più concentrato verso quello PDH meno concentrato. Va da sé che il piruvato Oxaloacetate (gluconeogenesis or anaplerosis) Acetyl-CoA (OXPHOS) accumulato nel citosol può attraversare la prima membrana senza bisogno di proteine, essendo 1minore di 10 kDalton; la seconda membrana è estremamente selettiva: possono passare acqua, anidride carbonica e ossigeno, ma non le altre molecole.
Come fa quindi il piruvato ad arrivare nella matrice mitocondriale per essere metabolizzato? Come abbiamo detto, la prima membrana viene attraversata grazie alle sue piccole dimensioni, dopodiché incontra un complesso mitocondriale che può essere chiamato MC1 o MC2 (di fatto sono dei trasportatori) che aiutano il passaggio del piruvato a livello della membrana mitocondriale interna. A questo punto il piruvato raggiunge la matrice. Si tenga presente che, nelle cellule tumorali, il complesso MC1 è spesso mutato; quindi, il piruvato si accumula a livello citosolico. Le cellule tumorali sono quindi 'costrette' a compiere la fermentazione attraverso la lattato deidrogenasi. Dunque, nelle cellule tumorali, l'indirizzo verso la fermentazione è dovuto al fatto che il piruvato non riesce ad entrare in modo efficace nei mitocondri. Una volta che il piruvato arriva nel mitocondrio può seguire due vie ed essere substrato di diversi enzimi: ad esempio, può essere la sorgente energetica per la gluconeogenesi oppure, se c'è bisogno di produrre ATP piuttosto che glucosio, il piruvato verrà indirizzato verso il Krebs.
Il primo enzima che metabolizza il piruvato è la piruvato deidrogenasi, un enzima complesso anche dal punto di vista evolutivo.
Complesso della piruvato deidrogenasi
La piruvato deidrogenasi va a trasferire i due carboni del piruvato, quindi un gruppo acetilico, sul coenzima A. Quest'ultimo l'abbiamo già visto in altre reazioni, siccome è una molecola chiave e un crocevia in vie metaboliche, perché può seguire diverse vie biosintetiche oppure, in caso di necessità di ATP, verrà convogliata nel ciclo di Krebs.
- Piruvato
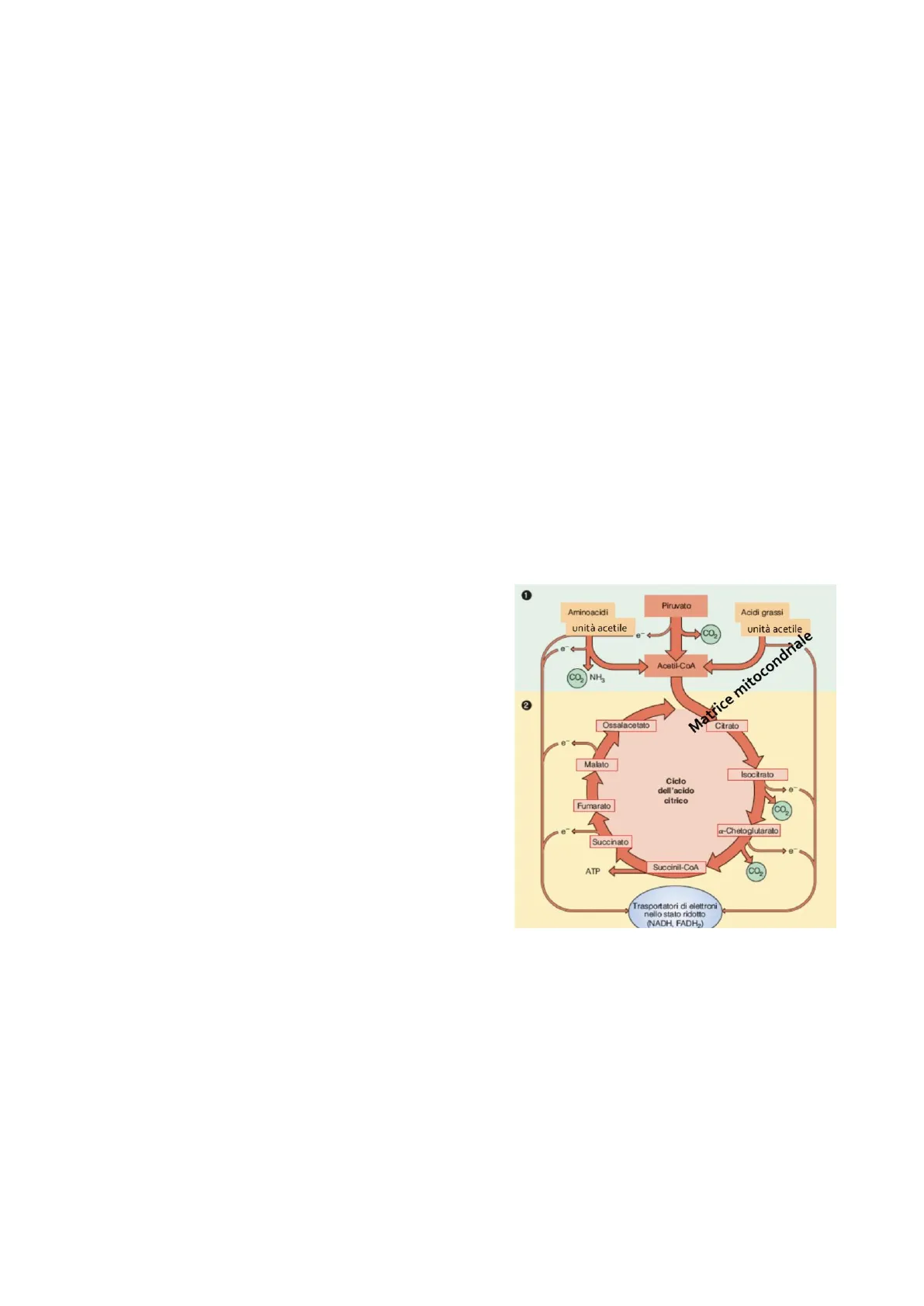
Aminoacidi unità acetile Acidi grassi unità acetile CO2 Acetil-CoA Matrice mitocondriale CO2) NH3 2 Ossalacetato Citrato Malato Isocitrato Ciclo dell'acido citrico e Fumarato CO2 e @-Chetoglutarato Succinato e ATP Succinil-COA CO2 Trasportatori di elettroni nello stato ridotto (NADH, FADH2) Nello sfondo dell'immagine vi sono due colori, ma non lasciatevi confondere perché entrambi i passaggi avvengono nella matrice mitocondriale; è solamente suddivisa la prima fase in cui la molecola di piruvato viene decarbossilata attraverso una redox e una decarbossilazione, e una seconda fase in cui la molecola di Acetil Co-A entra nel ciclo. Tra gli scienziati che hanno impiegato la loro vita per dare un contributo alla scienza, cito F. Lipmann che per primo isolò l'acetil coenzima A, vincendo il nobel. In realtà lui lo studiò nel metabolismo degli acidi grassi, ma ciò che evidenziò fu la potenzialità di questo composto che appartiene alla lista dei composti ad alta energia (trattati nelle prime lezioni).
2Dunque, il trasferimento del gruppo acetilico sul coenzima A avviene a livello dello zolfo, che è un residuo molto reattivo e che forma un legame tiolico (essendoci uno zolfo al posto dell'ossigeno). Questa molecola è quindi un composto ad alta energia perché, quando il gruppo acetilico verrà trasferito su molecole bersaglio, si romperà questo legame liberando energia e rendendo la reazione estremamente favorevole. In definitiva, la reazione da piruvato ad acetil coenzima A genera un composto altamente reattivo, ed è fondamentale perché andrà a trascinare le altre reazioni metaboliche. Come si nota dall'immagine, è la parte acetilica del piruvato ad essere trasferita al coenzima A. Acetil-CoA -+ forma attivata per il trasporto di gruppi acilici Acetyl group gruppo reattivo tiolico O «acetato attivo» gruppo acilico «attivato» ₹.C - CH3 CH2 B-Mercaptoethylamine residue CH NH c=0 CH2 Adenosine-3'- phosphate CH NH NH C=0 N H-C-O H3C -C -CH3 O O 2 La parte del gruppo carbossilico, invece, viene eliminata come CH2 -0-P- -P- - CH 0 0 0 H CO2; questa è la prima reazione della respirazione cellulare in cui H H H 0 OH eliminiamo la CO2, derivante da una parte di piruvato appunto. 1-SH 0-P-0 Acetyl-coenzyme A (acetyl-CoA) 0 L'enzima piruvato deidrogenasi (PDH) svolge la reazione in modo complesso: non solo è una reazione di decarbossilazione, ma anche una redox che utilizza il NAD+ come agente riducente (diventa NADH). Il PDH ha una struttura multimerica e non utilizzasolo il coenzima A e il NAD+, ma anche altri tre coenzimi. Quindi ha tre subunità enzimatiche e utilizza ben cinque coenzimi, di cui 4 derivanti da vitamine (si sottolinea il ruolo importante delle vitamine che non sempre viene evidenziato).
(a) (b) E2 24 subunità E1 Figure 21-4 dimeri John Wiley & Sons, Inc. All rights reserved. (c) La PDH è un complesso talmente grande da essere visibile al microscopio elettronico. È costituita da tre tipi di subunità (non tre subunità, ma tre 'tipi' di subunità); ciascuna delle subunità è presente un numero n di volte. La E2 (in verde), si dispone attorno ai margini di un ipotetico cubo. Sopra vediamo delle 'palline rosse', che rappresentano la E1 e centralmente le subunità E3. Avremo quindi questi tre tipi di subunità che andranno a costituire un complesso multiproteico che si dispone come in immagine.
Nella visione dall'esterno, la PDH è circondata dalla E1, mentre internamente c'è un core (in verde nell'immagine) che sarebbe la dominio lipoilico di E2 E1 100 A E2 E3 3 Ogni organismo ha la sua piruvato deidrogenasi, con differenze nel numero e nella conformazione delle subunità e nella disposizione dei coenzimi. Per semplicità, analizziamo quella del batterio E. Coli, siccome è stata la prima ad essere evidenziata con la cristallografia e una delle meglio analizzate. dimeri E3 Pantothenic acid residue NE2. Ancora più internamente, in rosso, abbiamo E3, visibile solo con una sezione sagittale dell'enzima. I piccoli filamenti azzurri rappresentano il coenzima Lipoato. La subunità E2 può presentare un coenzima, il lipoato, che rappresenta un braccio molecolare. Tra i vari coenzimi avevamo già visto la biotina che ha la funzione di 'gru', ma in realtà questi bracci molecolari avvicinano dei substrati spostandoli da un sito attivo all'altro dell'enzima, favorendo la catalisi. Tra l'altro in questo modo, i substrati elaborati nella successione di reazioni enzimatiche, non devono staccarsi dall'enzima, ma si possono semplicemente spostare attraverso questo braccio. Va precisato anche che il dominio lipoidico è diverso a seconda della specie; dunque, non solo il complesso multiproteico è diverso nei diversi organismi per il diverso numero n di 'sferette', ma lo è anche nella ripetizione di domini che legano il lipoile. Ad esempio, nei mammiferi vi sono due domini che legano questa 'gru' molecolare; oppure, negli E. Coli sono 3, nel lievito 1 ecc ... anche questo aggiunge variabilità all'enzima. In questa ricostruzione al computer si notano le dimensioni della piruvato deidrogenasi: 50 nM, cioè cinque volte più grande del complesso ribosomiale, a dimostrazione del fatto che sia un enzima molto importante.
La prof mostra un video per spiegare il funzionamento dell'enzima enase complex (https://www.youtube.com/watch?app=desktop&v=EuvUOxHmX7I): va osservato 50 nm come il piruvato entri attraverso i trasportatori, percorra le due membrane e, a questo punto, si trovi nella matrice mitocondriale. Questa è la PDH e il braccio azzurrino con estremità rossa è il lipoile. Abbiamo la E1, E2 ed E3 con il lipoile che si sposta da una subunità all'altra portando con sè i vari metaboliti che vengono a generarsi durante il processo catalitico. Va osservato, quindi, che lo schema della PDH è importante dal punto di vista evolutivo; infatti, è stato utilizzato anche in altri contesti che poi vedremo. Si noti che l'ossidazione del piruvato è ancora oggi oggetto di indagine, infattil'articolo che prenderemo in considerazione è uscito due anni fa; questo perchè la biochimica non è una scienza antica e già arrivata a conclusioni definitive, ma è in evoluzione ed alcune cose vengono continuamente indagate e chiarite. Procediamo ora a descrivere le diverse reazioni e come sono coinvolti gli enzimi. Abbiamo detto che abbiamo cinque enzimi coinvolti: tiamina pirofosforato (TPP), il braccio lipoidico (che possiede una catena con ponte di solfuro), il coenzima A(che entra come reagente nella reazione), una molecola di FAD(legata alla subunità E3) e il NAD+(che è legato all'enzima quando necessario, ma non saldamente, si può anche dissociare).
4