Appunti sulle proteine: composizione, struttura e amminoacidi
Documento di Matilde Griva sulle proteine. Il Pdf esplora la composizione e le diverse strutture delle proteine, analizzando gli amminoacidi e le loro proprietà, inclusa la struttura primaria e secondaria con alpha elica e foglietto beta. Questi appunti di Biologia per l'Università sono arricchiti da schemi e illustrazioni chiare.
Mostra di più16 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Le Proteine: Composizione e Struttura
Matilde Griva/Valeria Merangolo Lezione 2. Genetica Molecolare, prof.Porporato LE PROTEINE Gli organismi risultano essere sistemi piuttosto complessi in quanto composti da diversi organi, tessuti e cellule.
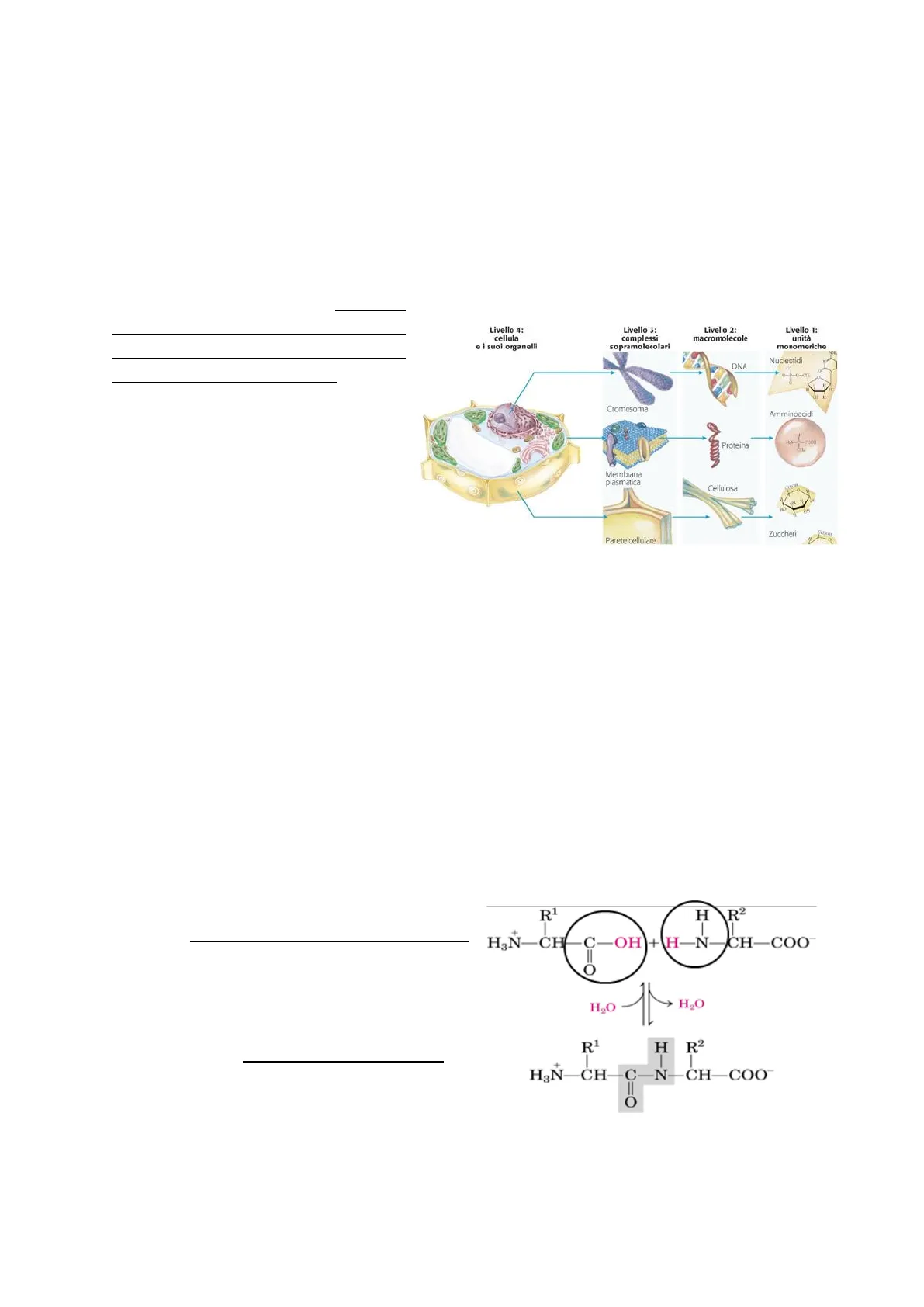
Importante è comprendere che ogni parte della singola cellula è formata poi da strutture diverse via via sempre più complesse e sempre più piccole. Il nucleo di una cellula, ad esempio, contiene i cromosomi costituiti da DNA, a sua volta formato da unità monomeriche, che prendono il nome di nucleotidi. Lo stesso accade con la membrana plasmatica, struttura complessa formata da parti sempre più piccole come proteine e fosfolipidi. La parete cellulare di cellule vegetali, invece, a livello macromolecolare, è formata da cellulosa, che a sua volta è formata da unità di zuccheri.
Livelli di Organizzazione Biologica
Livello 4: cellula e i suoi organelli
Livello 3: complessi sopramolecolari
Livello 2: macromolecole
Nucleotidi DNA Cromosoma
1 Proteina Membrana plasmatica Cellulosa Parete cellulare Zuccheri
Livello 1: unità monomeriche Amminoacidi
Molte molecole biologiche sono polimeri, insieme di unità più piccole (monomeri). L'uomo, per analizzare con i propri occhi queste unità, deve far uso di microscopi ad altissima risoluzione: con il microscopio ottico è possibile osservare come funzionano una cellula vegetale, animale, i batteri ed i cloroplasti, ma per esaminare strutture più piccole, come un fago T2 (un virus che infetta un batterio), proteine e lipidi, è doveroso utilizzare un microscopio elettronico a trasmissione o a scansione.
Gli organismi viventi sono costituiti al 70% da acqua, il restante 30% è un mix di ioni ma soprattutto macromolecole (proteine, carboidrati, acidi nucleici e lipidi).
Macromolecole e Processi di Condensazione
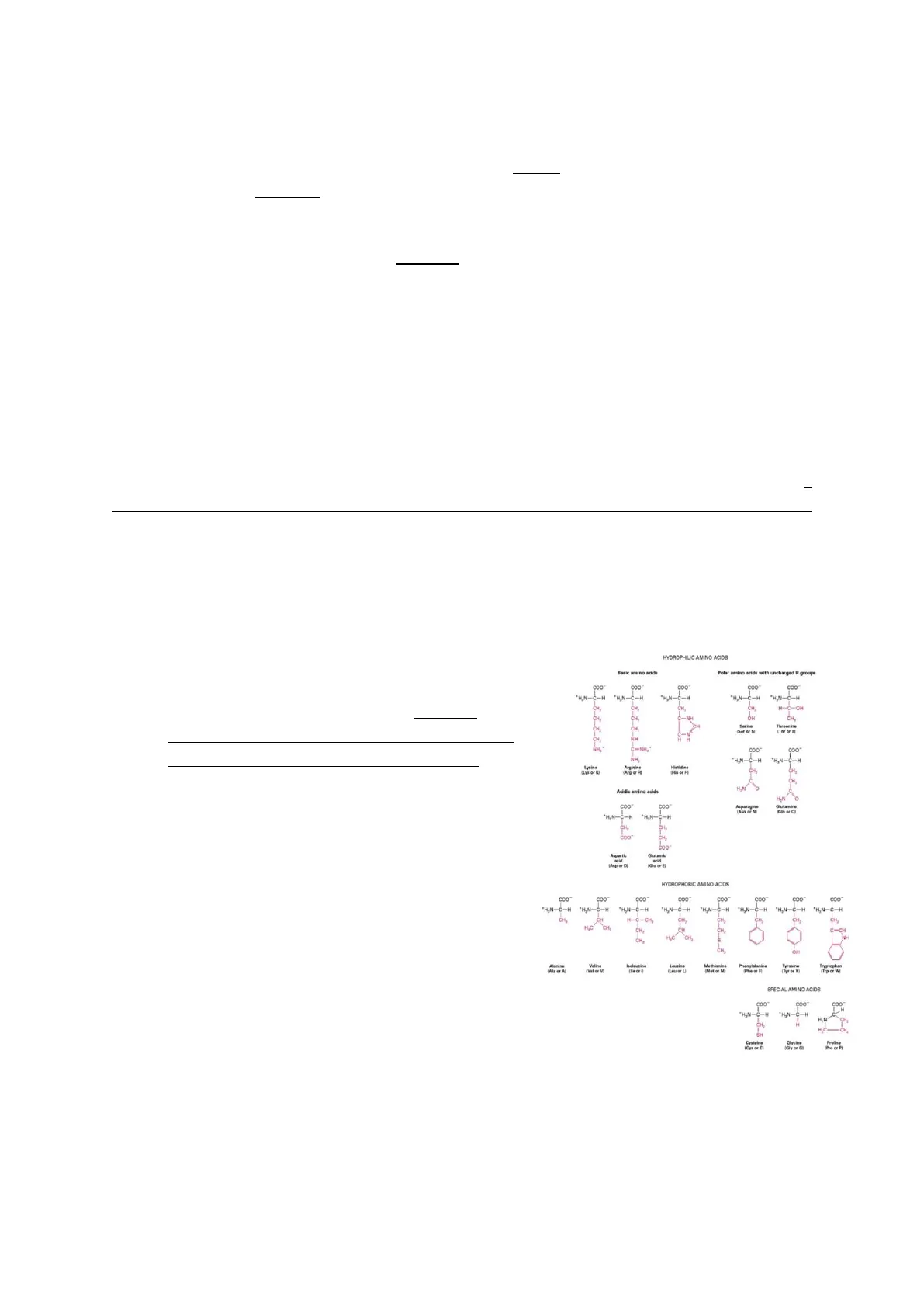
Le macromolecole sono polimeri costituiti da unità monomeriche e si formano attraverso processi di condensazione, ovvero addizione di diversi monomeri con il rilascio di una molecola di acqua. Quando un monomero si addiziona ad un altro monomero, il gruppo ossidrilico stacca il protone che va via sotto forma di molecola di acqua.
Diversamente invece quando un polimero deve essere scomposto serve una molecola di acqua per rompere il legame e quindi andare incontro a un processo noto come idrolisi.
R1 H \R2 H3N-CH-C-OH +H-N-CH-COO Ö L H2O > H2O R1 H R2 H3N-CH-C-N-CH-COO - Ö 1Le proteine sono divise in due gruppi:
- Funzionali: hanno una funzione che può essere di catalisi (enzimi), oppure possono avere una funzione di trasporto. Un esempio di proteina funzionale è l'emoglobina, un complesso proteico che permette ai globuli rossi di trasportare le molecole di ossigeno nel sangue.
- Strutturali: hanno la funzione di supporto. L'actina e la cheratina per come sono strutturate hanno la funzione di reggere l'impalcatura della cellula e sono, infatti, presenti in grande quantità nella pelle o nei capelli.
Amminoacidi: Struttura e Classificazione
Come è Fatto un Amminoacido?
Tutte le proteine sono formate da amminoacidi. Un amminoacido è una molecola formata da un gruppo amminico e un gruppo carbossilico, legati ad un atomo centrale che viene definito carbonio alpha. Attaccato a questo carbonio sono presenti un protone e un gruppo R laterale, che è caratteristico di ogni singola proteina e impone le peculiarità di un certo amminoacido.
Gli amminoacidi che vengono codificati nel nostro DNA sono 20. Sono suddivisi in:
- non polari -> presenza di una catena idrocarburica non polare
- polari -> non carichi, presenza di un gruppo ossidrilico o solfidrilico, gruppi elettronegativi che attirano verso di se le nubi elettroniche degli atomi, creano una polarizzazione e si verifica un addensamento di cariche negative. Questo è importante perché permetterà poi interazioni con altri elementi, i famosi dipolo-dipolo indotto. (es. serina, treonina, cisteina, asparagina e glutammina)
HYDROPHILIC AMINO ACIDS Basic amino acids 8386661 coo" *HN- COO COC *HẸN-C-H *HẠN- CH, C-NH CH CH. CH2 C-N CH Serine (Ser or Si NH C-NH, *HẸN- NH2 *HẠN-C-H Lysine (Lys or K) Arginine (Arg or R) Histidine (His or Hi Polar amino acids with uncharged R groups coo *HAN-C-H H-C -OH Threonine (Thr or T) :- H Acidic amino acids H.N Asparagine (Asn or N) Glutamine IGin or Gi LN-C-H *H,N-C-H CH2 COO coo" Aspartie [Asp or Di Glutamic (Glu or E) HYDROPHOBIC AMINO ACIDS COO coo COO COO Coo COO COC COO *H,N -H *H,N-C-H "H,N-C-H "H,N-C-H *H,N- *H,N-C-H "H.N V-C- "HN-C-H CH. CH H-C-CH, CH CH CH CH CH, H.C `CH CH CH OH Alanine (Ala or A) Valine (Val or V) Isoleucine Leucine (Leu or LI Methionine Met or M) Phenylalanine (Phe or F) Tyrosine (Tyr ce Y) Tryptophan (Trp or W) SPECIAL AMINO ACIDS *H.N H. CH CH. Cysteine (Cys or Ci Glycine (Gly er Gl Proline (Pro or P)
Gli amminoacidi sono divisi in:
- Amminoacidi essenziali sono quelli che l'essere umano deve necessariamente assumere con la dieta in quanto non ha la capacità di sintetizzarli.
- Amminoacidi non essenziali sono invece quelli che il DNA umano è in grado di codificare e sintetizzare.
2 · aromatici -> presenza di gruppi benzenici all'interno della struttura (es. fenilalanina, tirosina e triptofano) · carichi positivamente -> presenza di un gruppo amminico che in condizioni fisiologiche è protonato e rende la molecola carica positivamente (es. arginina) · carichi negativamente ->presenza di un gruppo carbossilico che perde il protone e carica negativamente la molecola (es. acido glutammico) C-CH COOIL LEGAME PEPTIDICO
Il Legame Peptidico
Alla base di una catena polipetidica c'è la formazione di un legame detto peptidico. Si tratta sempre di un processo di condensazione: un amminoacido interagisce con l'altro e avviene l'eliminazione di una molecola di acqua. L'interazione avviene tra il gruppo carbossilico di un amminoacido e il gruppo amminico dell'altro amminoacido; il gruppo carbossilico strappa il protone, questo andrà a riversarsi sull'altro lato in quanto è elettronegativo, successivamente l'ossigeno strappa un ulteriore protone, viene eliminata una molecola di acqua e si forma il legame peptidico, un legame covalente.
Diversamente da altri tipi di legame singoli questo è un legame molto forte e in termini di angstrom (di lunghezza) è anche più corto di altri legami singoli. Il carbonio essendo elettronegativo attira la nube elettronica su sé stesso; anche l'azoto è un atomo molto elettronegativo, che cercherà di addensare su se stesso la nube elettronica. In questo modo, dunque, carbonio e azoto si attirano l'uno verso l'altro. Differentemente da un classico legame singolo, questa forte attrazione fa in modo che la distanza tra i due atomi sia più corta, in pratica si tratta di un legame singolo rinforzato.
Caratteristiche dei Legami Peptidici
LEGAMI PEPTIDICI Gli amminoacidi sono comunemente uniti insieme da un legame ammidico, chiamato legame peptidico.
1 H2O R H O H H 1 N-C-C-N-C-C 0 H 1 R H 1 N-C-C + N-C-C H 0 R - H / H R H / OH H H 0 1 OH OH SH N-terminale CH2 Le proteine sono lunghi H 1 0 H H polimeri di amminoacidi uniti 1 - da legami peptidici e vengono +HIN-C-C-N-CT-C-N-C-COO 0 1 sempre scritte con CH2 I'N-terminale verso sinistra. La H CH 1 sequenza di questo tripeptide CH è istidina-cisteina-valina, o amminoterminale C-terminale o carbossiterminale
Questi due legami singoli permettono rotazione, pertanto HN CH3 CH3 HC=NH+ le lunghe catene di amminoacidi sono molto flessibili.
È importante sottolineare che essendo un legame rinforzato non c'è possibilità di rotazione intorno ad esso. Bisogna immaginare, quindi, come se tutto il legame peptidico fosse su uno stesso piano, che è impossibile ruotare. Al contrario, la rotazione può avvenire sugli altri legami come tra il carbonio e l'azoto e tra il carbonio e il carbonio. Attenzione però perché non tutte le rotazioni attorno a questi legami sono consentite.
Legame peptidico: i quattro atomi in ciascun riquadro grigio formano un'unità planare rigida. Non c'è rotazione intorno al legame C-N.
Nella seguente immagine è possibile osservare come gli amminoacidi si vanno a legare uno con l'altro formando una catena polipeptidica.
R R3 Rs H O O H H H II N C N C C N C N H 0 H 0 H O R2 R4
La parte in nero rappresenta lo scheletro della proteina. Tutte le proteine sono fatte in questo modo, ovvero hanno questo scheletro peptidico. L'unico elemento che differenzia una proteina dalle altre è la presenza dei diversi gruppi R.
Dal punto di vista convenzionale, una proteina viene letta e scritta: dal residuo ammino-terminale al residuo carbossi-terminale
Quando viene saldato un legame peptidico, da un lato abbiamo un legame amminico, dall'altra parte abbiamo un legame carbossilico, qualora si debba agganciare un nuovo amminoacido.
OH CH3 CH HO O H2C H2C. H H I-Z 0= H H H H +HN U=0 HH N H U=0 HỌC Tyr Gly Gly Phe Leu Residuo amminoterminale Residuo carbossiterminale H N C H H -I 3STRUTTURA DELLE PROTEINE
Struttura delle Proteine
Le proteine sono caratterizzate da una struttura:
Primary structure Secondary structure Tertiary structure Quaternary structure
Lys Lys Gly Gly Leu Val Ala His Amino acid residues & Helix Polypeptide chain Assembled subunits
- primaria: la sequenza amminoacidica delle proteine, costruita come se fosse un filo di perle dove ogni perla è un amminoacido che compone la proteina.
- secondaria: il filo di perle si può sistemare nello spazio in modi diversi dando origine a strutture più complesse, note proprio come strutture secondarie, che possono essere alpha n Fina elica o foglietto beta; è la conformazione spaziale che assume un determinata sequenza amminoacidica nello spazio.
- terziaria: come le diverse strutture secondarie si dispongono nello spazio ed interagiscono tra di loro.
- quaternaria: raccoglie tutti i tipi di interazioni che avvengono tra catene polipeptidiche diverse.
N.B la struttura secondaria, terziaria e quaternaria derivano tutte dalla struttura primaria. È sempre la struttura primaria, la sequenza amminoacidica, che determina la sua conformazione primaria. A seconda di quanti amminoacidi ci sono nella sequenza, la proteina assume diverse conformazioni e poi queste, all'interno della sequenza polipeptidica, a loro volta interagiscono tra di loro e con altre catene polipeptidiche.
4