Il clonaggio del DNA: metodiche di laboratorio e standardizzazione
Documento di Appunti sul clonaggio del DNA, le metodiche di laboratorio e la standardizzazione. Il Pdf esplora la struttura e la chimica degli acidi nucleici, le differenze tra librerie genomiche e di cDNA, e i metodi di costruzione e screening delle librerie, utile per lo studio universitario di Biologia.
Mostra di più41 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Il Clonaggio del DNA: Panoramica e Metodiche
Ad oggi la maggior parte delle tecniche di biologia molecolare sono acquistabili già pronte (ad esempio i kit per il dosaggio delle proteine; I kit per l'individuazione di specifici anticorpi; I vettori contenenti particolari geni ecc ... ). Per questo verranno trattati i meccanismo principali, senza entrare troppo nel dettaglio. La standardizzazione della metodica permette alle industrie la produzione in serie e quindi l'abbassamento del costo, la prevenzione all'esposizione di sostanze tossiche e una riduzione della possibilità d'errore nella preparazione, oltre che a una maggior rapidità e precisione nella riproducibilità del dato (molto importante in laboratorio). Spesso, per una questione di brevetto, vengono tenute segrete le composizioni dei kit, dei quali vengono però fornite indicazioni precise per l'uso (esempio kit Elisa).
Per clonare il DNA si possono utilizzare meccanismi differenti a seconda di quello che si vuole ottenere:
- Metodica 1, sistema più complesso, che prevede numerosi passaggi. Tramite un vettore si inserisce il DNA che si vuole clonare in una cellula ospite (coltura cellulare) che, grazie al suo corredo complesso, può amplificare il gene ed esprimerne il prodotto sintetizzando la proteina (metodica utilizzata, ad esempio, per sintetizzare l'insulina).
- Metodica 2, più semplice. Si limita all'analisi degli acidi nucleici (sia DNA che RNA) mediante la tecnica della polymerase chain reaction (PCR). Viene usata ad esempio per fare confronti tra geni patologici e sani, per vedere quali geni vengono espressi maggiormente nelle cellule tumorali. Anche per eseguire il tampone molecolare del COVID-19 viene usata questa tecnica: una volta raccolte le secrezioni oro- e naso-faringee, esse vengono processate con PCR per amplificare e quantificare le molecole di genoma virale eventualmente presenti. Questa metodica è più semplice valuta direttamente gli acidi nucleici utilizzando un mix di reagenti e non il prodotto del gene, quindi del polipeptide (come invece accade nella clonazione tramite vettore che necessita di modelli sperimentali complessi come le colture cellulari in vitro).
Natura Chimica del Gene
Gene Natura chimica DNA Sequenza nucleotidica 1 RNA Sequenza nucleotidica Polipeptide Sequenza amminoacidica
La sequenza nucleotidica del gene a livello dell'acido desossiribonucleico (DNA), viene trascritta in RNA e poi tradotta in sequenza amminoacidica.
Acidi Nucleici: Purine e Pirimidine
Le purine sono già state descritte parlando dell'adenosina trifosfato (ATP) e della guanosina trifosfato (GTP), che hanno come basi azotate rispettivamente l'adenina e la guanina. Le pirimidine sono invece la timina (esclusiva del DNA), l'uracile (al posto della timina nell'RNA) e la citosina (già citata parlando di lipidi complessi, nelle strategie di sintesi dei fosfolipidi (citosina difosfato (CDP) per attivare il diacilglicerolo)). Per quanto riguarda i carboidrati degli acidi nucleici possiamo avere ribosio (nell'RNA) o 2'-deossiribosio (esclusivamente nel DNA). I nucleotidi che abbiamo visto con varie funzioni (attivatori, fornitori di energia, etc.) son tutti ribonucleotidi. A completare il nucleotide c'è il gruppo fosfato (in base al numero di gruppi P presenti si distinguono nucleosidi mono-, di- o tri-fosfato) che si impegna a
Basi O NH2 TNH Purine 9 3. NH2 H H Adenina (A) Guanina (G) NH2 Pirimidine H3C ENH NH 6 1 H -T Citosina (C) Timina (T) (DNA) Uracile (U) (RNA)
Zuccheri e Fosfato negli Acidi Nucleici
Zuccheri 5 5' 3' 2 3 2 OH H OH OH 2'-deossiribosio (DNA) Ribosio (RNA) Fosfato O HO-P-O Anche rappresentato come P 3 5 2-I
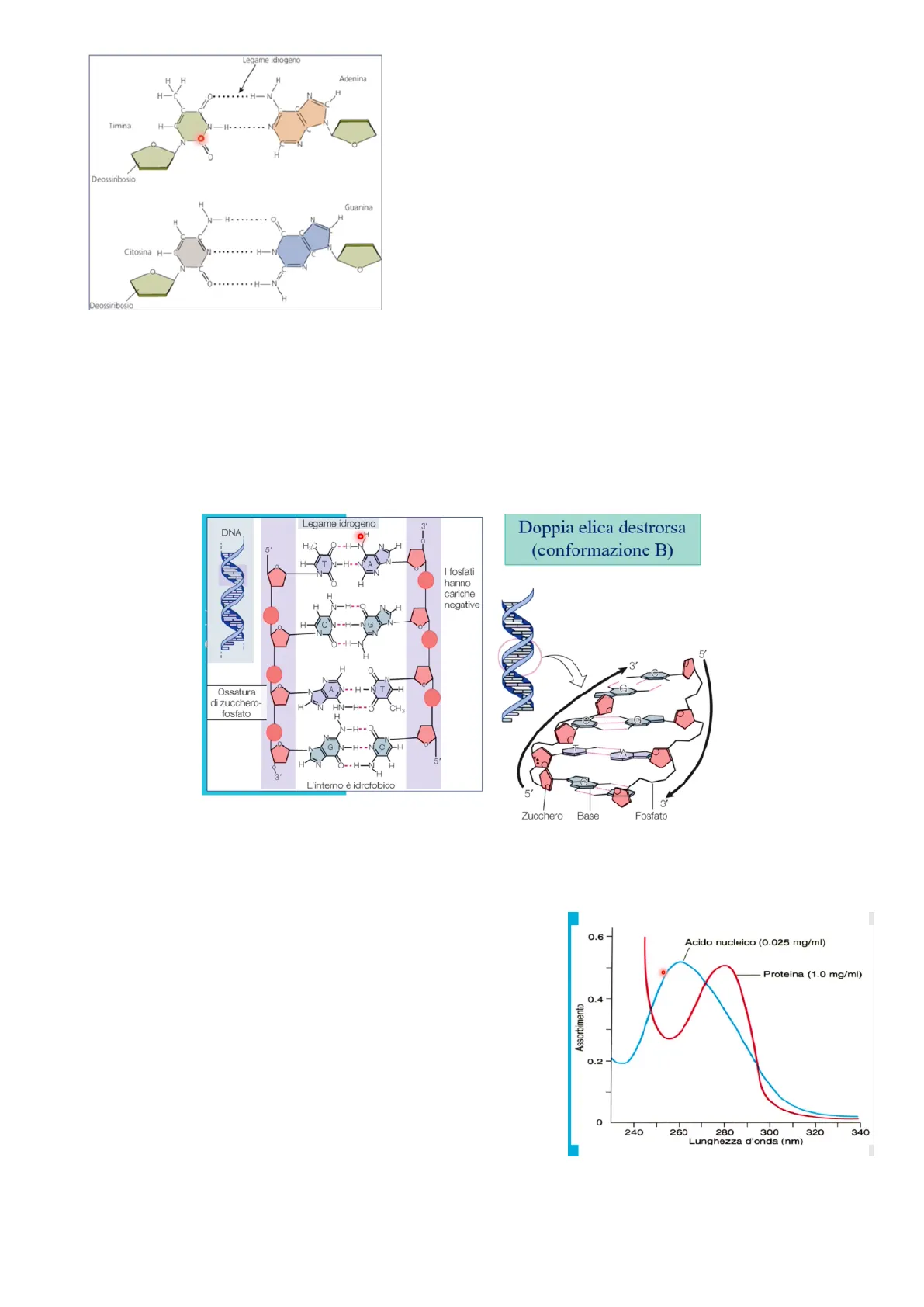
Legami Idrogeno nel DNA
OLegame idrogeno H H Adenina H- Timina H C =0 Deossiribosio H Guanina Citosina H- Deossiribosio formare il legame fosfodiesterico a ponte 5'-3' tra nucleotidi per ottenere la catena di acidi nucleici. Per unire le due catene sono inoltre presenti legami a H tra le basi complementari, in particolare:
- 2 legami a idrogeno tra A-T;
- 3 legami a idrogeno tra G-C.
Il legame a idrogeno è un legame debole ma, essendo presente in grande quantità, determina una gran forza che tiene uniti i due filamenti del DNA a livello delle basi azotate. La differenza del numero di legami tra le basi complementari determina una diversa temperatura di fusione (T alla quale i legami vengono rotti, per cui le due catene si separano). Se in un doppio filamento prevalgono coppie C-G la temperatura di fusione tende ad aumentare poiché sono presenti più legami a idrogeno da rompere, e viceversa se prevale la percentuale di A-T la temperatura di fusione sarà più bassa poiché servirà meno energia (fornita con l'aumento della temperatura) per rompere il minor numero di legami a idrogeno, per cui sarà più facile farlo.
Struttura del DNA e Legami
Legame idrogeno 3' DNA o H.C H-N 5 H I fosfati hanno cariche negative H 5' 3" H- -H Ossatura di zucchero- CH3 fosfato H- - N CH H-N H H 3" L'interno è idrofobico 5' 3 Zucchero Base Fosfato
Aspetto Chimico-Fisico del DNA
Aspetto chimico-fisico del DNA: Le basi azotate sono tendenzialmente aromatiche (aromaticità non completa). Gli acidi nucleici messi in soluzione hanno una lunghezza massima di assorbimento a 260 nm. Al di sotto dei 290-300 nm siamo negli UV: la soluzione osservabile è trasparente (la colorazione è visibile in genere sopra i 300 nm). Se si inserisce la soluzione in uno spettrofotometro (con capacità di lettura da 240 nm a lunghezze d'onda di tutto il visibile), posso leggere la concentrazione degli acidi nucleici grazie appunto all'assorbimento delle basi azotate di lunghezze d'onda pari a 260 nm. La lettura delle proteine è spostata invece a 280 nm. Con i metodi colorimetrici abbiamo visto che è possibile spostare le letture nel visibile (con l'acido nucleico questo non viene fatto).
0.6 - Acido nucleico (0.025 mg/ml) O Proteina (1.0 mg/ml) 0.4 Assorbimento 0.2 - 0 240 260 280 300 320 340 Lunghezza d'onda (nm) G 5 Doppia elica destrorsa (conformazione B) 254
Condizioni per il Clonaggio di un Frammento di DNA
La clonazione è conosciuta in biologia come la tecnica per ottenere una popolazione di individui che sono geneticamente identici ad un individuo di partenza. Il clonaggio, in biologia molecolare, indica invece il clonare un segmento di DNA in una cellula per ottenere un insieme di molecole di DNA identiche a quelle di partenza, che vengono prodotte in corrispondenza della replicazione cellulare. In pratica la cellula acquisisce in qualche modo il frammento (spesso perché esprime una proteina di forte interesse) che, successivamente, con delle metodiche particolari e l'organizzazione di un modello sperimentale, viene espresso e amplificato ogni qual volta che la cellula si replica. La cellula esprime tante copie del gene, fornendo quindi tante copie di proteine. Questo metodo, che sfrutta una cellula ospite nella quale viene introdotto un gene estraneo (alla quale viene quindi ricombinato il DNA) viene chiamato tecnologia del DNA ricombinante, ed ha reso possibile il clonaggio dei geni, permettendo di isolare, amplificare e sequenziare frammenti di DNA. Per sequenziare e analizzare un gene, è necessario avere tante copie a disposizione per poterlo studiare, per questo si amplifica.
Perché Manipolare i Geni?
- Per facilitare lo studio dell'espressione genica e della sua regolazione fisiologica;
- Per identificare il prodotto di un gene e/o per ottenere la sovraespressione;
- Per studiare la relazione tra struttura e funzione delle proteine;
- Per identificare componenti cellulari che interagiscono con particolari sequenze di acidi nucleici o con particolari domini proteici.
Applicazioni del Clonaggio
- Ricerca di base: studio dei meccanismi della replicazione genica e dell'espressione nei procarioti e negli eucarioti.
- Ricerca applicata: per ottenere microrganismi in grado di produrre molecole proteiche come l'insulina umana, l'interferone e l'ormone della crescita, utilizzate poi nella terapia.
24.11.21
Cosa Serve per un Clonaggio?
- Gene o cDNA: frammento di DNA di interesse;
- Enzimi di restrizione;
- Vettore;
- DNA ligasi;
- Cellula ospite.
Procedura di Clonaggio
Procedura Si seleziona un frammento di genoma (che può derivare o dalla frammentazione del genoma stesso o da una sua copia) che viene inserito in un vettore (quello più utilizzato e standardizzato è il plasmide batterico, presentante un DNA circolare), il quale a sua volta verrà immesso in una cellula ospite. Essa sarà poi in grado di garantire prima una replicazione, poi una trascrizione ed infine l'espressione del gene selezionato, permettendone così una produzione su larga scala. Nella maggior parte dei casi la cellula ospite sarà un batterio in grado di fornire numerose copie dello stesso gene, dato che lo scopo è quello di amplificare la sintesi.
Figura 2.1 Un tipico esperimento di clonaggio. Clonaggio di frammenti di DNA di un organismo eucariote all'interno di un vettore di clonaggio plasmidico, seguito da trasformazione e selezione delle cellule di Escherichia coli trasformate, cioè contenenti le molecole di DNA ricombinante. Cellula batterica Cellula eucariote DNA plasmidico Isolamento e purificazione del PHA DNA cromosomico Taglio con un enzima drestrizione 4 gazione Molecola di DNA ricombinante Trasformazione e selezione Cellula batterica trasformata contenente numerosi plasmidi ricombinanti
Enzimi di Restrizione
In natura varie specie di batteri posseggono e sfruttano enzimi di restrizione con funzione difensiva, poiché capaci di "tagliare" sequenze di DNA esogeno, come quello virale, per evitare che di essere infettate da quest'ultimo, che potrebbe inserirsi nel genoma batterico ed indurlo alla sintesi di proteine virali. L'azione di questi enzimi di restrizione non può essere rivolta verso il DNA del batterio che se ne serve, perché questo risulta metilato e dunque non viene riconosciuto. Tra questi enzimi si riconoscono le endonucleasi, quelle più utilizzate sono quelle di tipo II, in quanto sono molto più specifiche, riconoscendo sequenze da 4 a 6 nucleotidi di vario tipo e tagliando legami fosfodiesterici, mentre la I e la III risultano di scarso interesse, perché operano un taglio casuale, a valle dei siti sopra citati. Gli enzimi di restrizione generalmente prendono il nome del batterio di origine, che se ne serve per scagionare possibili infezioni virali da parte di un DNA fagico. Si ottengono così frammenti contenenti geni per l'espressione proteica richiesta, inseriti in plasmidi prodotti dall'industria biotecnologica. Ogni enzima taglia in siti precisi il genoma e riconosce una precisa sequenza. Il taglio può lasciare estremità piatte o sporgenti. Si possono ottenere sequenze non regolari di varia lunghezza, a seconda del sito in cui avviene il taglio. Se il sito di restrizione risulta poco frequente i frammenti saranno più lunghi, se risulta più frequente il DNA verrà tagliato in diversi punti ed otterremo frammenti più brevi.
Siti di Riconoscimento e Taglio degli Enzimi di Restrizione
A Siti di riconoscimento e taglio di alcuni ER B Gli ER possono tagliare il DNA generando estremità piatte o sporgenti ER che riconoscono 4 paia di basi ER che riconoscono 6 paia di basi 5' 3 3 5 Mbol EcoRI 5'-GATC-3' 3'-CTAG-5' 5'-GAATTC-3' 3'-CTTAAG-5' 5 Haell HindIII 5'-GGCC-3' 3'-CCGG-5' 5'-AAGCTT-3' 3'- TTCGAA-5' Alul BamHI 5'- AGCT-3' 3'- TOGA-5' 5'-GGATCC-3' 3'-CCTAGG-5' C Le estremità sporgenti prodotte dagli ER possono sporgere al 5' o al 3' 5 GGATCC CCTAGG 3 5 5 3 CTGCAG GACGTC 3' Hhal Sall 5'-GCGC-3' 3'-CGCG-5' 5'-GTCGAC-3' 3'-CAGCTG-5' BamHI Pstl Mbol Smal 5' 3 G GATCC CTGCAS G G 5'-GTAC-3' 3'-CATG-5' o'-CCC GGG-3' 3'-GGGCCC-5' CCTAG 5 G ACGTO 3 Figura 2.2 Siti di riconoscimento e modalità di taglio sul DNA da parte degli enzimi di restrizione. Gli enzimi di restrizione (ER) sono endonucleasi che riconoscono specifiche sequenze di nucleotidi sul DNA. La lunghezza di queste sequenze varia tra 4 e 8 nucleotidi. (A) Sequenze riconosciute da alcuni ER e tipo di taglio. (B) Gli ER possono tagliare la sequenza riconosciuta nel mezzo generando estremità "piatte" (blunt); oppure, gli ER possono tagliare la sequenza riconosciuta in modo asimmetrico sui due filamenti di DNA lasciando delle estremità "sporgenti" (protruding). (C) Queste estremità a singolo filamento possono sporgere al 5' o al 3' (sticky end), come mostrato per i due esempi BamHI e Pstl.
Mappe di Restrizione e Frammenti di DNA
Ogni determinato enzima fornirà una determinata sequenza di genoma. Conoscendo a priori i siti riconosciuti da questi enzimi, è possibile utilizzarli per descrivere a livello molecolare un frammento più o meno lungo di DNA. Si ottengono, in questo modo, le cosiddette mappe di restrizione. Per definire queste mappe occorre prendere un frammento di DNA genomico ed inserirlo in una miscela con un enzima di restrizione. Lasciando all'enzima tutto il tempo per individuare i suoi siti bersaglio esso li scinderà, mentre, lasciandogli poco
Siti di restrizione - - - DNA genomico O Digestione incompleta Collezione di frammenti sovrapposti Figura 2.20 Preparazione di frammenti sovrapposti di DNA genomico mediante digestione parziale con un enzima di restrizione. La digestione parziale di DNA genomico con un enzima di restrizione che riconosce i siti indicati dalle frecce genera una collezione di frammenti sovrapposti, esemplificata dallo schema nel riquadro in basso. La digestione completa che si ottiene tagliando tutti i siti indicati dalle frecce rosse genererebbe, invece, frammenti di DNA non sovrapposti. 256 is in 5' 0 in Estremità piatte Estremità sporgenti 3