Strutture e compartimentazione cellulare in biochimica
Documento sulle strutture e compartimentazione cellulare. Il Pdf, utile per lo studio universitario di Biologia, esplora le differenze tra cellule eucariotiche e procariotiche, i metodi di isolamento degli organelli tramite centrifugazione e la composizione delle membrane cellulari.
Mostra di più16 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Strutture e Compartimentazione Cellulare
L'importanza del conoscere le strutture e compartimentazioni cellulari in biochimica sta nel fatto che queste organizzazioni sono il primo metodo di regolazione delle varie funzioni e vie metaboliche: esse infatti costituiscono una barriera fisica, che impedisce lo svolgimento contemporaneo e nella stessa zona di certi processi e reazioni. Il primo compartimento è ovviamente la membrana plasmatica, che separa l'interno della cellula dall'ambiente esterno rimanendo però comunque semipermeabile e permettendo quindi il passaggio di alcune sostanze. Quindi nelle cellule eucarioti abbiamo tutta un'altra serie di divisioni, che invece non sono presenti nei procarioti (vedi approfondimento): innanzitutto il nucleo, delimitato dalla membrana nucleare e che contiene il materiale genetico. Poi i mitocondri, che possiedono una membrana doppia come il nucleo; il reticolo endoplasmatico, rugoso e liscio, l'apparato di golgi, ed infine strutture minori come lisosomi, perossisomi, ecc.
Membrana Plasmatica
Plasma membrane Tough, flexible lipid bilayer. Selectively permeable to polar substances. Includes membrane proteins that function in transport, in signal reception, and as enzymes.
Ognuno di questi organelli, e ovviamente anche la membrana plasmatica, ha lo scopo di separare il contenuto interno dall'ambiente esterno, isolando alcuni processi, e permettendo il passaggio di sostanze solo in base alle proprietà chimiche e fisiche sia della membrana che fa da barriera sia delle molecole che cercando di passare.
Eucarioti e Procarioti
E' sempre bene ricordare le differenze tra queste due grandi classi di organismi:
| EUCARIA | PROCARIA | |
| Dimensioni | Tra 5 e 100 um | Tra 1 e 10 um |
| Genoma | Organizzato con proteine istoniche e compattato nella cromatina all'interno del nucleo | Libero nel citoplasma e privo di proteine istoniche |
| Divisione | Per mitosi | Binaria o per gemmazione |
| Compartimentazione | Presente | Assente |
| Nutrizione | Per ingestione (endocitosi, pinocitosi, fagocitosi), assorbimento, fotosintesi | Per assorbimento e fotosintesi |
| Vie metaboliche | Pattern enzimatici limitati e presenza di mitocondri | Pattern enzimatici numerosi e vari, con enzimi sulle membrane plasmatiche |
| Citoscheletro | Presente e dinamico, con monomeri che polimerizzano in strutture e filamenti associati e contribuiscono a varie funzioni | Pressoché assente |
| Movimento intracellulare | Presenza di trasporto vescicolare, endocitosi ed esocitosi | Nessuna vescicola |
Funzioni degli Organelli e Separazione
Prima di addentrarci ulteriormente e parlare di quali siano queste proprietà, analizzando la composizione delle membrane, occorre precisare come sappiamo quali funzioni vengono svolte all'interno degli organelli, e perché vengono così separate. Prendiamo come esempio la degradazione degli acidi grassi, che avviene nei mitocondri, mentre la loro sintesi è attuata nel citoplasma: ovviamente questi due processi non possono coesistere nello stesso ambiente, in quanto si "annullerebbero" a vicenda, per cui la cellula attua una separazione (che alla fine dei conti è comunque un mezzo di regolazione) fisica. Per capire però che la sintesi avveniva nel citoplasma e non viceversa è stato necessario isolare i vari compartimenti cellulari ed analizzarli singolarmente, ricercando gli enzimi coinvolti nelle vie metaboliche; questo si attua tramite centrifugazione. Dopo aver rotto la membrana cellulare, solitamente utilizzando una provetta in vetro e un pestello di teflon che hanno tra loro una distanza minore rispetto al diametro di una cellula, per cui le "schiacciano" e rompono, si ottiene in soluzione un misto di organelli ancora intatti e citoplasma. Esso può venire centrifugato a velocità sempre più alte, separando per peso i vari organelli (prima si centrifuga a velocità bassa per eliminare eventuali cellule ancora intere): il primo a depositarsi nel pellet sarà il nucleo, più pesante. Quindi si depositano i mitocondri, poi il reticolo endoplasmatico ed infine tutti gli altri, lasciando soltanto il citoplasma che può infine essere analizzato.
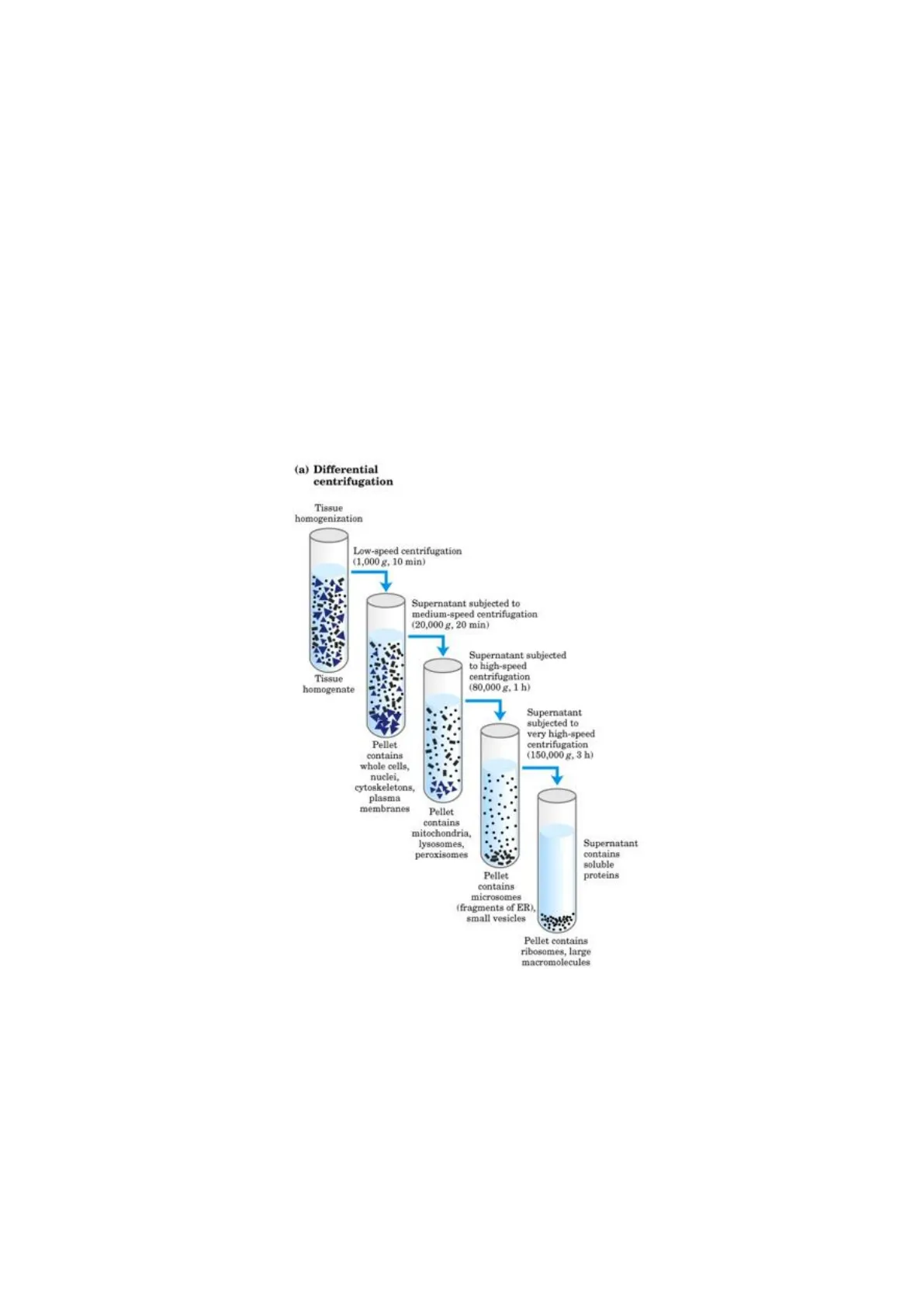
Centrifugazione Differenziale
(a) Differential centrifugation Tissue homogenization Low-speed centrifugation (1,000 g, 10 min) Supernatant subjected to medium-speed centrifugation (20,000 g, 20 min) Tissue homogenate Supernatant subjected to high-speed centrifugation (80,000 g, 1 h) Pellet contains whole cells, nuclei, cytoskeletons, plasma membranes Supernatant subjected to very high-speed centrifugation (150,000 g, 3 h) Pellet contains mitochondria, lysosomes, peroxisomes Supernatant contains soluble proteins Pellet contains microsomes (fragments of ER), small vesicles Pellet contains ribosomes, large macromolecules
Permeabilità della Membrana Plasmatica
Detto questo vediamo allora di analizzare le varie compartimentazioni, con particolare attenzione alla membrana plasmatica. Come abbiamo già detto, essa separa l'interno della cellula dall'esterno ed è semipermeabile, per cui può essere attraversata da molecole solo in base alle rispettive proprietà chimico- fisiche. La membrana plasmatica è infatti apolare, in quanto costituita da un doppio strato di fosfolipidi, per cui la possono attraversare direttamente generalmente solo molecole piccole e apolari o leggermente polari: per esempio degli ioni carichi per quanti minuscoli non riusciranno mai a passare, mentre il glicerolo che è polare ma possiede solo 3 atomi di carbonio sì, ma il glucosio a 6C è già troppo grande. Vediamo come le proprietà chimiche (carica e polarità) o fisiche (dimensioni) della specie influenzino le sue interazioni con la membrana.fatty acid tails lipid head groups - water molecules
Osmolarità e Permeabilità della Membrana
La permeabilità della membrana è molto importante in primis per una questione di osmolarità: se una cellula si trova infatti in una soluzione ipertonica, ossia che ha osmolarità maggiore della sua ed è molto concentrata in soluti, la cellula tende a far passare acqua all'esterno per riequilibrare la situazione, causando il fenomeno di shrinking. Se invece la soluzione in cui la cellula è immersa è ipotonica e con osmolarità minore, la cellula assorbe acqua al suo interno, gonfiandosi fino all'estremo per poi rompersi ed espellere il suo contenuto. E' evidente come entrambe le situazioni siano deleterie, e l'unica accettabile sia di isotonicità con stessa concentrazione fuori e dentro dalla cellula: questo va quindi mantenuto tramite il passaggio di soluti e molecole.
Globuli Rossi e Concentrazione Ionica
crenated normal swollen lysed RED BLOOD CELL ion concentration in extracellular space HYPERTONIC ISOTONIC HYPOTONIC VERY HYPOTONIC
Diffusione Semplice e Gradiente Elettrochimico
Tuttavia fino ad ora abbiamo parlato solo di un passaggio "diretto" ossia di una diffusione semplice: le molecole possono naturalmente attraversare la membrana (si dice che essa è permeabile a queste sostanze) e il passaggio avviene secondo gradiente di concentrazione o secondo gradiente elettrico. In parole semplici, le molecole si muovono spontaneamente dentro e fuori dalla cellula in base alla loro concentrazione o alla concentrazione di cariche: se all'interno c'è una bassa concentrazione della sostanza si osserverà un flusso dall'esterno, mentre se ad esempio all'esterno c'è una concentrazione di cariche positive molecole con carica negativa tenderanno a uscire per compensare. Generalmente le membrane presentano una differenza di potenziale tra il lato esterno, solitamente carico positivamente, e quello interno carico negativamente: questo influenza la diffusione di specie cariche a parità di concentrazione. Una specie carica positivamente infatti entra più facilmente se all'interno della membrana c'è un eccesso di cariche negative, e viceversa invece per una carica negativa che verrebbe respinta e tenderebbe a passare ancora più lentamente che in una situazione senza differenza di potenziale: è più corretto allora parlare di gradiente elettrochimico.
Gradiente Elettrochimico
+ + + + + + + + + + + + OUTSIDE INSIDE + + + + + + electrochemical gradient with no membrane potential electrochemical electrochemical gradient with gradient with membrane potential membrane potential negative inside positive inside
Trasporto Attraverso la Membrana
In quest'ultimo esempio possiamo trovare però una discordanza: ioni carichi non riuscirebbero a passare da soli attraverso la membrana plasmatica, ed infatti esistono delle modalità di scambio differenti, che coinvolgono la presenza di trasportatori. Si tratta di proteine che legano selettivamente una molecola e la trasportano attraverso la membrana, oppure creano dei veri e propri canali di passaggio mediando il trasporto di sostanze che altrimenti non riuscirebbero a diffondere (come lo stesso glucosio prima citato).
Meccanismi di Trasporto
I trasportatori tendono a essere specifici e a legare solitamente una o poche specie, e la velocità di passaggio attraverso la membrana di esse non dipende più solo dalla concentrazione della sostanza in questione ma transporter-mediated Vmax diffusion anche dal numero di trasportatori: quando infatti essi sono tutti occupati nel trasporto di una sostanza si raggiunge una velocità massima che non può aumentare, per cui si dice che il sistema è saturabile: solo all'inizio l'aumento della velocità è 1/2Vmax lineare con l'aumento della concentrazione. Anche per questo simple rate of transport diffusion motivo alcune cellule come i villi intestinali producono delle estroflessioni, in modo da massimizzare la superficie disponibile per l'assorbimento. Km concentration of transported molecule
Affinità dei Trasportatori
Oltre che da una velocità massima le proteine di trasporto sono anche definite da un'affinità per certe specie specifiche, che si può calcolare con la costante di affinità e ci da anche informazioni sulla concentrazione di una certa molecola necessaria per raggiungere la velocità massima: se ad esempio per la specie 1 bastano 0,01 mmol per arrivare a vmax, mentre per la specie 2 ne occorrono ben 10, è chiaro che il trasportatore è molto più affine alla prima specie.
Trasporto di Anioni e Cationi
Un esempio di questo può essere il trasporto di anioni e cationi tra l'esterno e l'interno della cellula: confrontando infatti le concentrazioni di diversi ioni, possiamo osservare come siano differenti. Il sodio Na+ è presente in concentrazioni tra 5 e 15 mmol all'interno della cellula, mentre fuori si arriva a 140mmol, e per il potassio K+ è esattamente il contrario. Il valore di concentrazione ionica all'interno ed esterno della cellula è complessivamente lo stesso, non c'è differenza osmotica, ma la composizione cambia: è presente una diversa selettività nei confronti di questi ioni, che vengono mantenuti a questi specifici livelli da sistemi attivi (altrimenti anche se sono carichi prima o poi, nel lungo periodo, la concentrazione si riequilibrerebbe). Lo stesso vale poi per il calcio, che è presente nel citoplasma in concentrazioni bassissime, 10-4 mmol, ma ve ne sono 12mmol all'esterno: apparentemente c'è uno squilibrio, ma in realtà il Ca2+ complessivo all'interno della cellula è lo stesso che all'esterno. Esso infatti è conservato in compartimenti specifici, soprattutto nel reticolo endoplasmatico, dove è mantenuto sempre da processi attivi ad alte concentrazioni senza farlo fluire spontaneamente nel citoplasma.
| COMPONENT | INTRACELLULAR CONCENTRATION (mM) | EXTRACELLULAR CONCENTRATION (mM) |
| Cations | ||
| Na+ | 5-15 | 145 |
| K+ | 140 | 5 |
| Mg2+ | 0.5 | 1-2 |
| Ca2+ | 10-4 | 1-2 |
| H+ | 7 × 10-5 (10-7.2 M or pH 7.2) | 4 × 10-5 (10-7.4 M or pH 7.4) |
| Anions* | ||
| CI- | 5-15 | 110 |
Specificità del Trasportatore
La specificità di un trasportatore dipende solitamente dalla sua struttura tridimensionale, che è accuratamente formata per riconoscere solo una o poche molecole simili: essa si modifica cambiando di conformazione in risposta al legame della specie bersaglio, per permetterne il passaggio. Il passaggio che viene mediato può essere di una sola molecola o di due, nella stessa direzione nel caso di simporto o in quella opposta nel caso di antiporto.