Acidi e Basi: Teoria di Bronsted-Lowry e Stereochimica degli Alcani
Documento su Acidi e Basi. Il Pdf, utile per lo studio universitario di Chimica, esplora la teoria di Bronsted-Lowry, la forza degli acidi e delle basi coniugate, e la stereochimica degli alcani, inclusi risonanza ed effetti induttivi.
Mostra di più16 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Acidi e Basi
Un concetto di fondamentale importanza, che influenza tantissime reazioni della chimica organica, e dipende dall'elettronegatività e polarità di cui abbiamo parlato precedentemente, è quello di acidità e basicità. Si può definire sia secondo Bronsted-Lowry che secondo Lewis, ma cominceremo dalla prima teoria.
Teoria di Bronsted-Lowry
Secondo Bronsted-Lowry un acido è una sostanza che cede protoni, mentre una base li accetta: generalmente per protoni intendiamo ioni H+, ossia il solo nucleo dell'idrogeno, privato del suo elettrone, e che contiene appunto solo un protone. Le mappe di potenziale ci aiutano a capire quando ci troviamo in presenza di acidi e di basi: in un acido infatti sarà sicuramente presente un H legato ad un atomo molto elettronegativo, e quindi "spoglio" di elettroni. Il suo colore nella mappa sarà allora blu, che ci indica un potenziale acido, mentre una base avrà una zona colorata di rosso e ricca di elettroni da donare all'idrogeno, acquistandolo. Quando un acido perde un protone (deprotonazione) diventa la sua base coniugata, ad esempio lo ione cloruro è la base coniugata dell'acido cloridrico; viceversa una base che si protona diventa il suo acido coniugato, come lo ione idronio rispetto all'acqua. Gli acidi e le basi differiscono tra loro per la capacità di donare ioni o di accettarli: gli acidi più forti reagiscono quasi completamente con l'acqua, mentre quelli più deboli si scompongono solo in parte, e lo stesso vale per le basi. Alcuni composti possono anche comportarsi in entrambi i modi se ne hanno le caratteristiche, come l'acqua che in certi ambienti si comporta da base e in altri da acido. La forza esatta degli acidi in soluzione acquosa viene espressa dalla loro costante di equilibrio, ossia:
Kc = [A~][H30+] [H20][HA] Essendo normalmente in soluzioni diluite la concentrazione dell'acqua costante, e pari circa a 55,4M a 25℃, possiamo calcolare la costante di dissociazione acida:
Ka = Kc[H20] = [A ][H30+] [HA] Ed eventualmente è possibile anche utilizzare una scala logaritmica per esprimere questo valore, ossia la pKa = - log Ka: un acido forte avrà un valore basso di pKa (e alto di Ka) mentre un acido debole ha un valore alto. Rispettivamente, come possiamo vedere dalla tabella, le basi coniugate di acidi forti sono deboli, mentre quelle di acidi deboli tendono a essere forti.
Tabella Acidi e Basi Coniugate
Acid Name pKa Conjugate base Name Weaker acid CH3CH2OH Ethanol 16.00 CH3CH20- Ethoxide ion Stronger base H2O Water 15.74 HO- Hydroxide ion HCN Hydrocyanic acid 9.31 CN- Cyanide ion H2PO4 Dihydrogen phosphate ion 7.21 HPO42- Hydrogen phosphate ion CH3CO2H Acetic acid 4.76 CH3CO2- Acetate ion H3PO4 Phosphoric acid 2.16 H2PO4- Dihydrogen phosphate ion HNO3 Nitric acid -1.3 NO3 Nitrate ion Stronger acid HCI Hydrochloric acid -7.0 CI- Chloride ion Weaker basePossiamo capire questa relazione osservando la struttura delle molecole e delle loro basi coniugate:
Acido Acetico e Ione Acetato
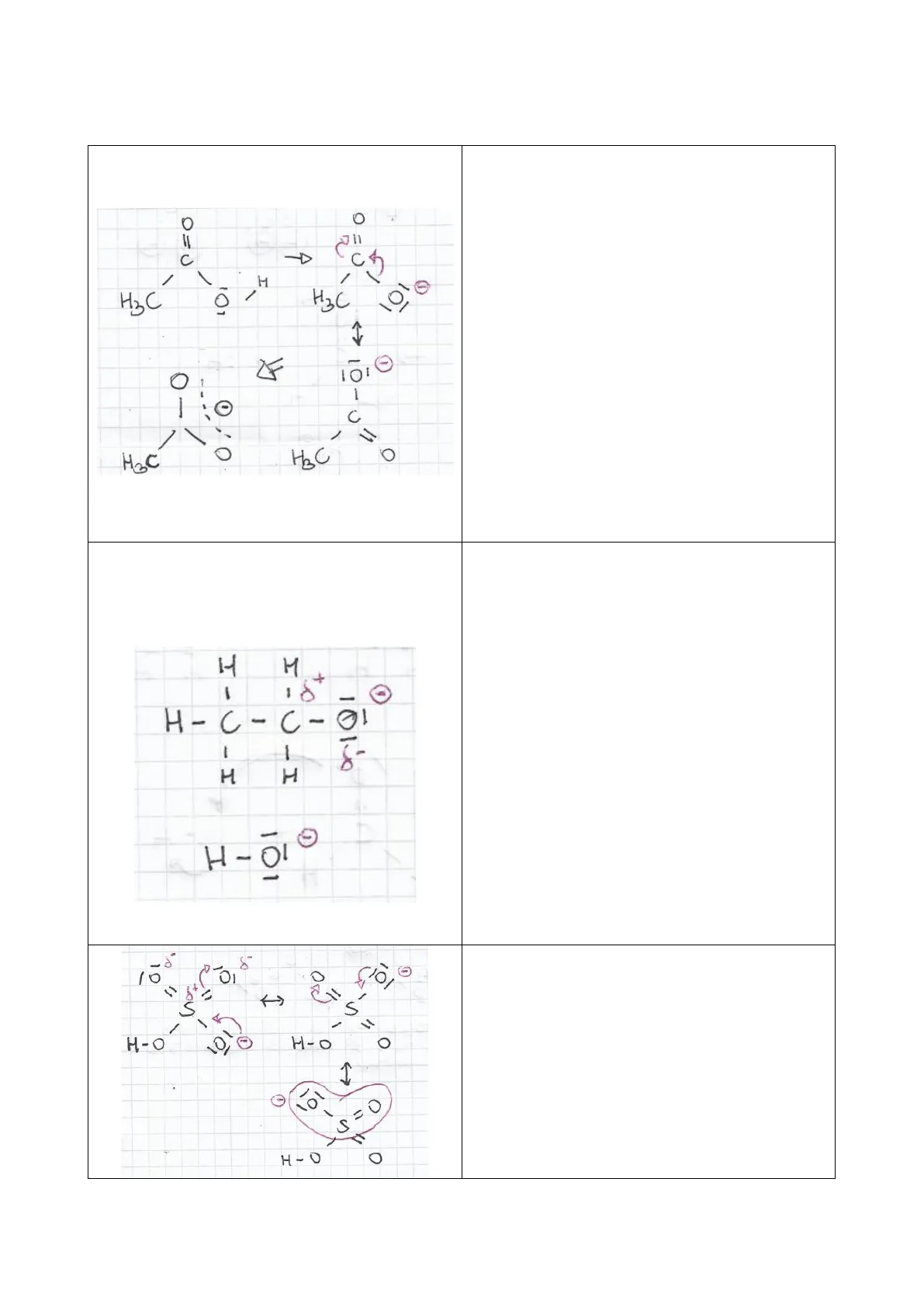
0 0 11 C -D ch / H H3C 0 / H3C 101 1 0 1 1 , 0 ,0 C - 11 H3C Iniziamo dall'acido acetico, che perde un idrogeno dal gruppo OH (la sua parte acida, dove c'è un idrogeno legato ad un elemento elettronegativo) trasformandosi nella base coniugata ossia lo ione acetato. Come abbiamo osservato precedentemente in questo ione c'è un raggruppamento di 3 atomi dotati di un orbitale p, e con un doppio legame e uno singolo, in cui si può verificare un fenomeno di risonanza: questo lo stabilizza, rendendolo poco incline a ri-acquistare il protone perso e quindi è una base debole. Inoltre la carica negativa è situata sull'ossigeno, dove può essere ben accolta grazie alla sua elettronegatività. Essendo le due forme equivalenti l'ultima scrittura può essere usata per mostrare la distribuzione della carica negativa, che oscilla continuamente tra i due ossigeni; un po' come nelle mappe di potenziale vediamo dove è effettivamente "situata"
Etanolo e Ione Etossido
H M + 1 18 - H-C-C-01 1 1 I- H H H- 01 L'etanolo è invece un acido debole, così come l'acqua, e la loro differenza di pKa è minima. Tuttavia la base coniugata dell'etanolo, lo ione etossido, è più forte rispetto allo ion idronio. Questo perché nel primo abbiamo una carica intera negativa su O dovuta alla perdita dell'elettrone, che viene rafforzata dalla catena carbonilica ad esso legato: essendo C meno elettronegativo di O infatti la catena ha un effetto elettronico induttivo di elettron-donazione I+, rendendo ancora più propenso l'ossigeno ad acquistare elettroni (questo effetto lo hanno tutte le catene alchiliche!). E' quindi una base forte grazie a questo effetto, che invece non si verifica con il solo idrogeno legato ad O in HO: infatti l'acqua può agire in entrambe le direzioni, e anche se la base coniugata ha una carica negativa sull'ossigeno (elettronegativo) non è particolarmente più stabile della sua altra forma, non ci sono effetti elettronici ulteriori a stabilizzarla.
Base Coniugata dell'Acido Solforico
-8 8 - 0 10 0 0 101 1, I S 5 1 H-O 101 H-O 0 1 - 10 5=0 11 H-O 0 H3C 0 F /1 1 La base coniugata dell'acido solforico ha una carica negativa sull'ossigeno, che fa parte di un gruppo triatomico dove si può verificare risonanza; lo zolfo infatti è parzialmente positivo, essendo meno elettronegativo dell'ossigeno, quindi la coppia tenderà a passare su di esso formando un doppio legame. Complessivamente quindi ci sono 3 forme di risonanza, e la coppia elettronica è continuamente ridistribuita o delocalizzata, stabilizzando questa forma.
Risonanza nell'Acetone
0 11 1, + jx Anche l'acetone può presentarsi in una forma di risonanza, in cui si forma una divisione di carica con la rottura del doppio legame C=O: l'ossigeno prende tutta la coppia elettronica. Prima c'erano solo delle parziali cariche positive e negative, e questa forma contribuisce maggiormente all'ibrido di risonanza.
Risonanza nel Carbocatione
8 80 11 0 1 / 0 Anche in questo carbocatione possiamo osservare la risonanza, in quanto esiste un sistema a tre centri su cui distribuire la carica negativa; la seconda forma contribuisce più della prima, visto che la carica negativa è situata sull'ossigeno elettronegativo e non sul carbonio.
Stabilità di NH2, OH e SH-
NH2 < OH < SH" Per capire le differenze di stabilità tra NH2, OH e SH- non possiamo fare riferimento ad effetti elettronici, che non sono presenti. Allora tra i primi due possiamo dire che O è più elettronegativo di N, quindi acquista meglio la carica negativa ed è più stabile: OH è una base più debole di NH e quindi l'acqua è un acido più forte dell'ammoniaca. Invece tra OH e SH l'elettronegatività è molto simile, ed appartengono allo stesso gruppo: qui possiamo confrontare le dimensioni atomiche, e lo zolfo distribuisce meglio la carica negativa grazie alle sue dimensioni più voluminose. Quindi complessivamente la sua base è più stabile dello ione idrossido ed infatti l'acido solforico è più forte dell'acqua.
Stabilizzazione del Carbocatione e Carboanione
f + O Il primo carbocatione si può stabilizzare per risonanza: ricordiamo infatti che alla fine di una linea in una struttura scheletrica c'è un CH3, ma qui trovando una carica positiva avremo un CH2. Esso è legato a un carbonio sp2, con quindi un orbitale p, legato ad un altro dello stesso tipo con un doppio legame: abbiamo quindi il classico gruppo triatomico in cui formare la risonanza. Il secondo carbocatione non si può invece stabilizzare, non avendo a disposizione doppi legami. L'ultimo carboanione ha invece ben due centri triatomici, e quindi si stabilizza in due forme di risonanza (si ha una catena di rotture e formazioni di doppi legami)
Fattori di Stabilità della Base Coniugata
In generale allora, cosa rende una base coniugata più stabile rispetto ad un'altra, e quindi il suo acido più forte?
- Fattore di elettronegatività nel periodo - quando una carica negativa si sposta su un elemento più elettronegativo, che supporta meglio la densità elettronica, si ha una situazione più stabile.
- Dimensioni atomiche nel gruppo - come abbiamo visto nell'esempio (6) a parità di elettronegatività la dimensione atomica influisce sulla stabilità, in quanto un atomo più voluminoso distribuisce meglio la carica negativa e dà maggiore stabilità.
- Effetti elettronici induttivo e di risonanza - a seconda del tipo di effetto possono aumentare la stabilità, come per la risonanza, o diminuirla, come nell'effetto induttivo di elettron-donazione dell'esempio (2) che aumenta ulteriormente la carica negativa e lo rende prono a riacquistare il protone.
Esercizi di Deprotonazione
In modo simile a come abbiamo fatto finora possiamo anche risolvere esercizi come i seguenti:
Deprotonazione del Gruppo OH
OH H2N O H2N NECA IV-I -> INICJ / 0 J-I Nella catena presentata in figura il gruppo più acido è quello OH, in quanto l'ossigeno è più elettronegativo dell'azoto e tenderà a cedere più facilmente il suo protone, essendo più stabilizzato di NH alla fine. Quindi durante una deprotonazione con una base adeguata sarà l'ossigeno a perdere il suo idrogeno.
Stabilizzazione della Base Coniugata con Triplo Legame
Anche con una situazione del genere (dopo una deprotonazione, c'erano due H legati a C) la base coniugata si può stabilizzare per risonanza: il triplo legame funziona infatti esattamente come quello doppio.
Deprotonazione del Gruppo NH
0 1 0 11 T N 2 € H M 1 0 +1 +1 11 0 / N 1 N M エ ー て Se volessimo capire dove si deprotona questa molecola, usando una base adeguata, dovremmo nuovamente chiederci qual è il gruppo più acido. In questo caso sarà il secondo gruppo NH: l'elettronegatività è la stessa, trattandosi dello stesso elemento, ma questo gruppo è legato a un gruppo carbonilico C=O, e quindi si può stabilizzare per risonanza. Così la carica negativa passa sull'ossigeno, che la accetta meglio. Nel caso opposto invece non solo non ci sarebbe stata la risonanza, ma i gruppi alchilici circostanti avrebbero fatto un effetto induttivo di elettron-donazione incrementando ancora di più la carica negativa e rendendola più instabile e più propensa a riacquistare il protone.
Elettronegatività e Risonanza nell'Acidità
Ricordiamo anche in generale che quando valutiamo l'acidità di un composto, l'elettronegatività ha quasi sempre la meglio sulla risonanza: un composto con due forme di risonanza che delocalizzano su degli ossigeni è una base coniugata più stabile di una con 4 forme di risonanza, ma che delocalizzano su dei carboni: Ovviamente possiamo capire la maggiore o minore forza di un acido anche dai valori della pKa: essi sono in particolare utili per prevedere se una reazione avrà luogo o meno. Infatti una reazione può avvenire solo se un acido donerà un protone alla base coniugata di un acido più debole, e la base coniugata dell'acido più debole rimuoverà un protone dall'acido più forte; in altre parole l'acido e la base coniugata che si formano 56 -D 2-I 1 1 120