Appunti di Biologia Applicata: molecole biologiche e patologie
Documento da Università su Biologia Applicata, focalizzandosi su molecole biologiche, patologie e matrice extracellulare. Il Pdf, utile per lo studio universitario di Biologia, presenta in modo schematico carboidrati, acidi grassi, proteine e patologie come l'epidermolisi bollosa.
Mostra di più50 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
BIOLOGIA APPLICATA
(1.2) Dimensione cellula: 10-20 micrometri Spessore membrana cellulare: 5 nanometri
MOLECOLE BIOLOGICHE
Carboidrati (o zuccheri) (2.1)
- Formula generale: (CH2O)n
- Si differenziano in base alla presenza del gruppo aldeidico H-C=O o del gruppo chetonico C=O › La gliceraldeide è lo zucchero più semplice, formato da soli tre atomi di carbonio
- Attraverso la condensazione di due monosaccaridi, si ottiene un disaccaride (legame glicosidico)
- Polisaccaridi derivanti dal glucosio: cellulosa (polimero lineare costituito da atomi di glucosio uniti da legami ß 1-4 glicosidici che si trova nelle pareti delle cellule vegetali) e amido (si divide in amilosio, polimero lineare formato da legami alpha 1-4 glicosidici, e amilopectina, polimero ramificato che presenta legami a 1-4 glicosidici e legami a 1-6 glicosidici) > La riserva umana di glucosio è sotto forma di granuli di glicogeno situati negli epatociti
Acidi grassi (2.2)
- Formato da testa polare idrofilica (-COOH) e coda apolare idrofobica
- Si dividono in:
- Trigliceridi > una molecola di glicogeno e tre di acido grasso
- Fosfolipidi > una molecola di glicerolo e due code di acido grasso. Il terzo gruppo OH del glicerolo è legato ad un gruppo fosfato. Se posti in acqua formano il doppio strato fosfolipidico
- Steroidi > il principale è il colesterolo, una molecola anfipatica
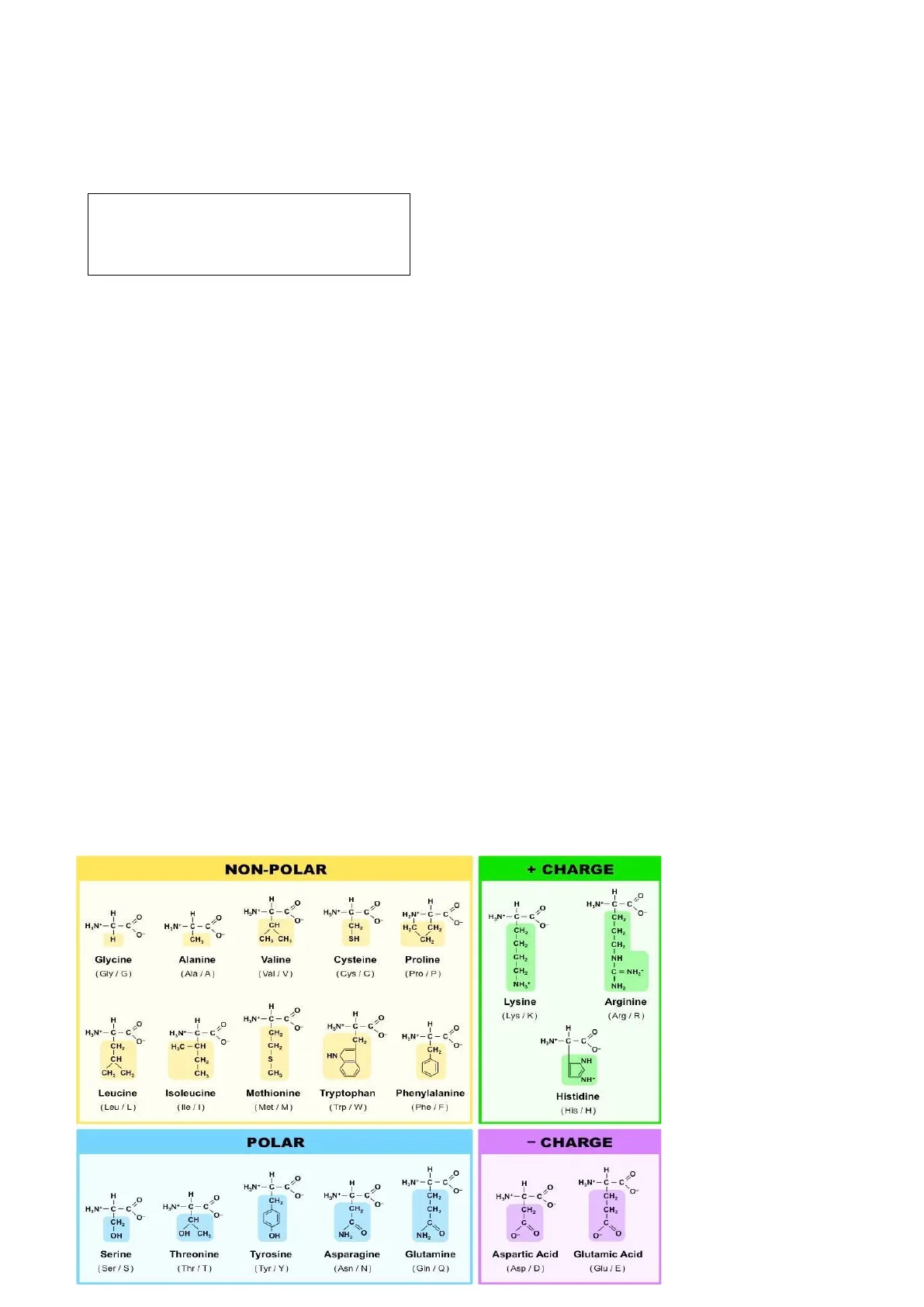
Proteine (3.1)
NON-POLAR H H H H H O O H3N+-C-C - CH H3N+-C-C H2N+-C- C H3N+-C-C CH2 C CH CH2 1 CH2 CH2 CH2 NH CH2 C = NH2+ NH,+ NH2 Lysine Arginine (Arg /R) H H H3N+-C-C. I-C Os H H3N+- C-C H3N+-C- C CH H3N+-C -0- . C 0 H H3N+-C- O CH CH2 NH CH3 CH3 CH, CH3 Leucine (Leu / L) Isoleucine (Ile /1) Methionine (Met /M) Tryptophan (Trp / W) Phenylalanine (Phe /F) (His / H) POLAR - CHARGE H O H H3N+- C - C. H3N+-C C. H o CH H3N+- C C CH CH CH2 CH. C OH OH NH2 NH2 Serine (Ser / S) Threonine (Thr / T) Tyrosine (Tyr / Y) Asparagine (Asn / N) Glutamine (Gin / Q) + CHARGE H I- O H3N+-C-C H3N+-C-C HỌC CH2 O H CH3 CH3 CH3 CH2 Glycine (Gly / G) Alanine (Ala / A) Valine (Val / V) Cysteine (Cys / C) Proline (Pro / P) H 0 O O O 1 CH2 O HAN+-C- C o CH2 HỌC - CH CH2 CH HN CH2 1 o H3N+- C -C I-0- C H3N+- C-C CH H3N+- C C. CH 0 CH OH CH3 o O O Aspartic Acid (Asp / D) Glutamic Acid (Glu / E) In natura esistono 20 amminoacidi, ma recentemente ne sono stati scoperti altri 2: la selenocisteina (SEC) e la pirrolisina. H .O H H3N+- C-C O. C I-0- O. O H3N+-C-C (Lys / K) 15- "NH Histidine CH2 SH 0Aminoacido 1 Aminoacido 2 H H H H H H N N c c H 0 0 R R H legame peptidico H O H N H H I- H N R H O R Dipeptide acqua Un amminoacido presenta un'estremità con un gruppo -COOH libero, detta estremità C-terminale o carbossi-terminale, e un'estremità con un gruppo amminico libero detta estremità N- terminale o estremità ammino-terminale. Struttura primaria: Una proteina si forma unendo due aminoacidi tramite un legame peptidico (legame covalente). Struttura secondaria: è permessa grazie al legame a idrogeno. Esistono due forme ben definite: 1. l'a-elica: si forma una spirale costituita da uno scheletro di carboni legati da legami peptidici, mentre i residui laterali sono tendenti verso l'esterno 2. Il ß-foglietto: lo scheletro è disposto su un piano (non spiralizza) e i residui laterali spuntano da entrambe le parti di esso. -I- 3 legame a idrogeno I- 0 Legame disolfuro: si forma tra due cisteine Proteina monomerica: proteina che funziona da sola senza doversi legare ad altre catene peptidiche
Struttura terziaria e quaternaria delle proteine (3.2)
Struttura terziaria: unione di più strutture secondarie. La proteina si ripiega grazie alle interazioni tra amminoacidi (legame ionico, a idrogeno, ponti disolfuro, salini, forze di Van der Waals), occupando così uno spazio tridimensionale. Struttura quaternaria: una o più subunità proteiche si uniscono a formare una funzionale struttura multimerica. Un esempio è l'emoglobina.
Malattie correlate alle proteine
- Morbo della mucca pazza > detta anche encefalopatia spongiforme bovina, è causata da una conformazione errata della proteina PrPc: invece di essere ad a-elica, si presenta a ß-foglietto, diventando praticamente impossibile da degradare. Questa condizione porta alla morte dei neuroni e quindi alla formazione di "buchi" nel cervello.
- Alzheimer -> normalmente l'APP (proteina precursore della beta amiloide) è ripiegata ad a- elica, ma a causa di un errore nel suo metabolismo va ad assumere una conformazione a ß- foglietto. Questo fa sì che la proteina formi placche di depositi fibrosi tra i neuroni, causando la malattia.
Acidi nucleici
Legame C1 - B.A. = legame N-glicosidico Legame C5 - P = legame estere Legame P - P = legame anidridico (ad alta energia) (A) (G) (c) (T) (U) adenosina/ guanosina / citosina/ timidina/ uridina PURINA Adenina Guanina 2 ANELLI NUCLEOSIDE BASE AZOTATA PIRIMIDINA -> 1 ANELLO B.A. P 5' 4 Z. P. RIBOSIO - RNA 3 2 ZUCCHERO PENTOSO DESOSSIRIBOSIO -> DNA (-1 OH in Cz:) NUCLEOTIDE Timina/Uracile Citosina 1' H O H(4.1) In un acido nucleico, il nucleotide numero 1 ha un'estremità 5' fosfato libero, mentre l'ultimo ha un'estremità 3' OH libero. Ogni nucleoside è legato a quello successivo mediante un legame covalente, il legame fosfodiesterico.
Regole di Chargaff
- In una molecola di DNA la quantità di adenina è sempre uguale a quella di timina, e la quantità di citosina è sempre uguale a quella di guanina.
- Ogni specie avrà un diverso numero di adenine, timine, guanine e citosine estremità 5' 5' endo 0 -4- O HỌC 5 c H H H H 3 O H C -P=0 O H2C 5 O A H H H H 3 0 H O-P=0 O H2C 5' O G H H H H 3 OH H estremità 3' 3' end
Rosalind Franklin e la struttura del DNA
Rosalind Franklin Utilizzò la tecnica della cristallografia a raggi X > consiste nel prelevare il DNA, purificarlo e cristallizzarlo (il dna diventava così un cristallo di sale, stabile e fermo in modo tale da poterlo sottoporre ad un'analisi della struttura tridimensionale). Successivamente si sottopone a radiografia, colpendolo con raggi X per poi impressionare l'immagine in una lastra fotografica.
Struttura del DNA (4.2)
S 3 CC G KA 3.4 nm G A G A G 6 3 1- 2 nm- Spessore doppia elica: 2 nm (2 x 10-9 m) Passo dell'elica: 3,4 nm (l'elica fa un giro completo e torna nella posizione iniziale ogni 3,4 nm) Avanzamento di ogni base: 0,34 nm
Forme di DNA
- Forma A: è destrorsa, corta, spessa, ogni avanzamento di base è lungo 2.3 Å (Ångström. È uguale a 10-10 m) e ci sono 11 bp per giro.
- Forma B: è quella descritta da Watson e Crick nel 1953. Il DNA ha una forma destrorsa, lunga, sottile, ogni avanzamento di base è lungo 3.4 Å e ci sono 10 bp per giro.
- Forma Z: è sinistrorsa, lunga, sottile, ogni avanzamento di base è lungo 3.8 Å e ci sono 12 bp per giro. T 28 A 1 A form B form 7. form
- Lo scheletro idrofilico, costituito da zucchero e gruppo fosfato (conferisce una carica negativa al DNA), è rivolto verso l'esterno, mentre le basi azotate sono rivolte verso l'interno della doppia elica
- Le basi azotate sono disposte una di fronte all'altra su un piano perpendicolare all'asse della doppia elica, seguendo le regole di Chargaff
- I due filamenti formano un major groove (solco maggiore) e minor groove (solco minore) 0.34 nm
- i filamenti sono complementari e antiparalleli, e l'elica è destrorsa
- L'energia di un singolo legame idrogeno è di 4 Kcal/mol
Strutture secondarie particolari del DNA
- DNA a tripla elica > tali parti sono meno accessibili, rendendo la trascrizione più difficile
- DNA a quadrupla elica > coinvolto in diverse patologie
- DNA cruciforme > ha una parte della sequenza che è complementare a quella successiva, e quindi una parte del filamento forma al suo interno una doppia elica.
- DNA circolare > come il DNA batterico TOÇÇAĞ AGTGG ÇA CTT AÇO G· · - 3' CGTCACCGTGAATGGC .. . 5 DNA sequence with inverted repeats G T C A A C === A --- T C --- G C --- G G --- C T --- A G --- C 5' - + -ATAC GG TTACCG. .. 3' 3. . . TATGCC A AT G G C . . . 5' C --- G A --- T C --- G G --- C G --- C T --- A G --- C T A G 0 Base pairing between complementary segments on the same strand of DNA
Differenze tra RNA e DNA
| RNA | DNA |
| Presenta lo zucchero ribosio | Presenta lo zucchero desossiribosio |
| A, G, C e U | A, G, C e T |
| Single strand, ma alcuni presentano zone a double strand (come l'rRNA, che presenta 40 zone a doppia elica) | Double strand |
| Inizia con un fosfato libero all'estremità 5' e termina con un OH libero all'estremità 3' | Inizia con un fosfato libero all'estremità 5' e termina con un OH libero all'estremità 3' |
| Serve solo in specifici momenti, quindi ha vita breve | È portatore dell'informazione genica, quindi ha vita lunga |
Genoma umano (5.1)
Tutte le cellule umane presentano due genomi: 1. Genoma nucleare, che comprende tutti i cromosomi ed è costituito da 6.4 miliardi di bp (in un diploide) 2. Genoma mitocondriale
(6.1) La lunghezza dei cromosomi umani è estremamente variabile: infatti, mentre il cromosoma 1 (il più grande) è composto da 250 milioni di basi, il 22 (il più piccolo) ne contiene 48 milioni.
Tipologie di sequenze nel genoma
Il nostro genoma è composto per il 50% da sequenze uniche e per la restante metà da sequenze ripetute. Con sequenze uniche si intende: - sequenze relative ai geni, di cui si distinguono introni non codificanti ed esoni codificanti (rispettivamente 20% e 1.5% del genoma totale); - sequenze che non sono né esoni né introni (30%). percentage O 10 20 30 40 50 60 70 80 90 100 LINEs SINES introns protein-coding regions retroviral-like elements DNA-only transposon 'fossils' GENES TRANSPOSONS non-repetitive DNA that is neither in introns nor codons simple sequence repeats segmental duplications REPEATED SEQUENCES UNIQUE SEQUENCES 50% 50%Con sequenze ripetute invece ci si riferisce a determinate sequenze presenti in più copie all'interno del genoma, in quanto vengono ripetute in tandem. Si tratta di quei geni codificanti per proteine la cui produzione all'interno della cellula è richiesta in elevata quantità (come istoni e rRNA). Esistono diversi tipi di sequenze ripetute: > LINEs (long interspersed nuclear element), costituite da 7000 basi disperse nel DNA di cui esistono centinaia di migliaia di copie; > SINEs (short interspersed nuclear element), costituite da 300 basi ripetute circa un milione di volte; > Elementi trasponibili (trasposoni e retrotrasposoni), ossia sequenze di alcune migliaia di basi in grado di spostarsi all'interno del genoma. Ogni individuo presenta inoltre delle personali ripetizioni di basi collocate in determinati loci presenti unicamente nel proprio genoma. Lunghezza totale DNA: 2 metri Lunghezza cromosoma: 1-2 cm
Compattazione del DNA (6.2)
Esistono 5 diversi tipi di istoni, che prendono i nomi di: H2A, H2B, H3, H4 e H1. Ognuno di essi presenta gli amminoacidi K, R e H, ovvero Lisina, Arginina e Istidina, tre amminoacidi contenenti una catena laterale dotata di carica positiva, che permette la formazione di un legame molto forte con il DNA, che presenta una carica negativa.
Ottamero istonico
Ottamero istonico: composto da 2 istoni H2A, 2 H2B, 2 H3 e 2 H4.
Livelli di compattazione del DNA
- 150 bp di DNA compiono 1.65 giri attorno all'ottamero istonico NUCLEOSOMA coda H4 coda H2B coda H2A coda H3 coda H2A coda H4 coda H2B (A) coda H3 Core Histones H3 H4 H2A H2B DNA H1 + 2x Tetramer 2x 147 bp Linker DNA Histone Tails Nucleosome core particle (NCP) Nucleosome Chromatosome
- Nucleosomi uniti da DNA filamentoso e istoni H1 (linker) > FILO DI PERLE
- Nucleosomi del filo di perle si legano tra di loro > FIBRA A 30 NANOMETRI (forma assunta dalla cromatina per la maggior parte del ciclo cellulare)
- Fibra a 30 nanometri continua ad avvolgersi fino alla formazione dei LOOPS e delle SPIRALI CONDENSATE
- Cromatina continua ad addensarsi > CROMOSOMI
DNA polimerasi (7.1)
Abbiamo 14 DNA polimerasi diverse, codificate da 14 geni diversi. Questo perché, nonostante le polimerasi compiano sempre lo stesso lavoro fisico (attaccare un nucleotide), sono necessarie funzioni specifiche, come per esempio: replicazione DNA mitocondriale, replicare il leading strand, replicare il lagging strand, riparare il DNA quando serve ... Le DNA polimerasi sono dei complessi formati da una proteina che svolge il lavoro principale, detta subunità catalitica, a cui si associano altre proteine dette accessorie.