Trattamento pre-analitico in biochimica clinica, appunti del Prof. Roberto Gambino
Documento del Prof. Roberto Gambino su trattamento pre-analitico. Il Pdf esplora i principi della biochimica clinica, coprendo l'identificazione e l'uso dei biomarcatori, l'interpretazione dei valori di riferimento di laboratorio e il metabolismo del ferro, utile per studenti universitari di Biologia.
Mostra di più17 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Trattamento Pre-Analitico
Il trattamento pre-analitico prevede diverse tappe che devono essere monitorate per garantire la correttezza del trattamento analitico.
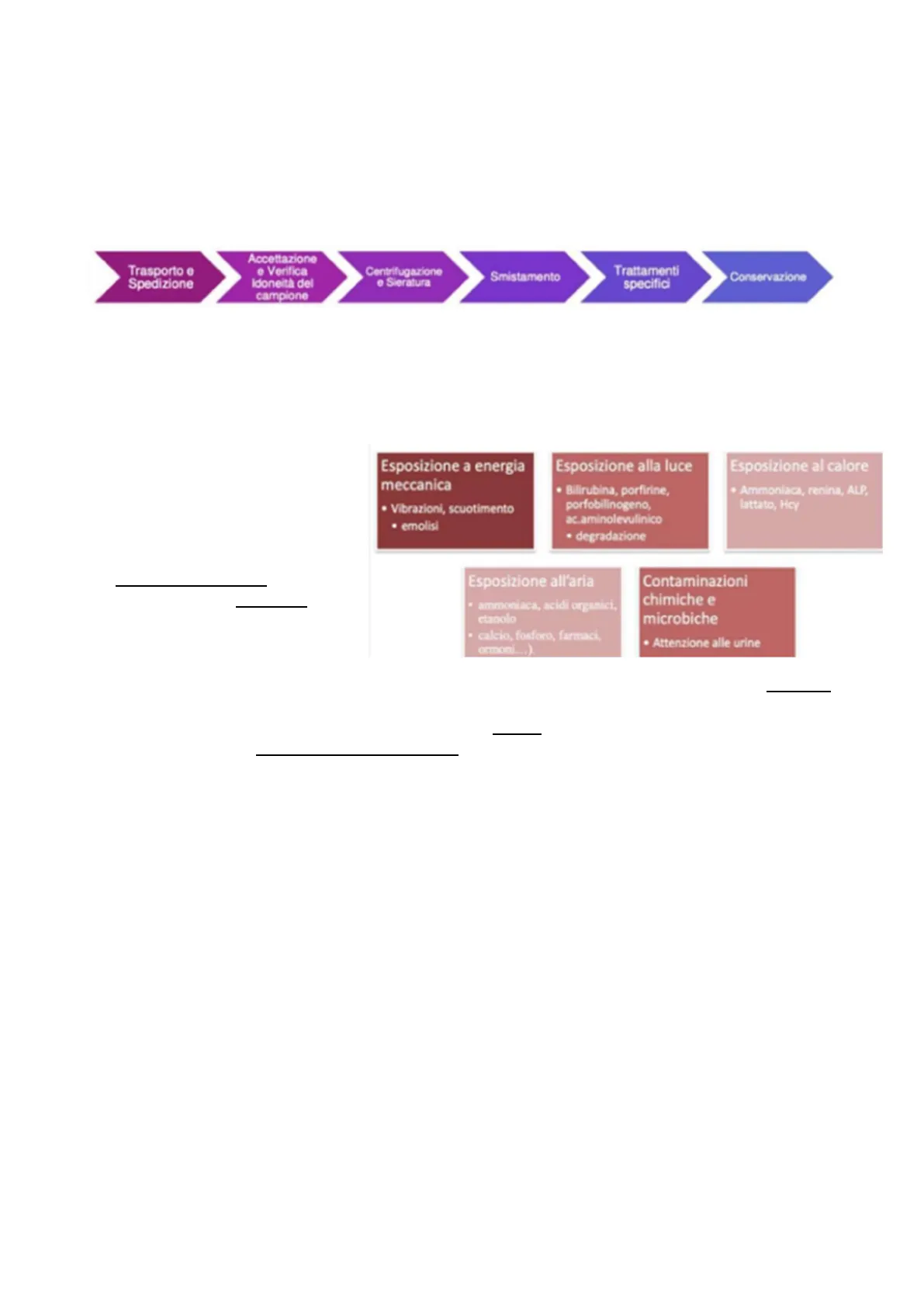
In questa immagine sono elencate le varie tappe del trattamento pre-analitico.
Trasporto e Spedizione Accettazione e Verifica Idoneità del campione Centrifugazione e Sieratura Smistamento Trattamenti specifici Conservazione
Il trasporto può essere intramurale (dentro lo stesso laboratorio) o extramurale (da presidio a presidio). Quest'ultimo prende sempre più piede, perché c'è la politica del laboratorio centralizzato.
Ci sono diversi tipi di refrigerazione per il trasporto, come il ghiaccio o l'azoto liquido, per poter conservare enzimi, fattori di coagulazione e vari ioni, che, liberi, potrebbero causare l'emolisi del campione.
Condizioni di Trasporto del Campione
Il trasporto è il momento in cui il campione più probabilmente si Esposizione a energia Esposizione alla luce meccanica trova in condizioni non · Bilirubina, porfirine, porfobilinogeno, · Vibrazioni, scuotimento · degradazione · emolisi ac.aminolevulinico standardizzate.
Il controllo del trasporto deve essere effettuato per evitare che il campione sia esposto a: energia meccanica, che può Esposizione all'aria causare emolisi; alla luce, che · ammoniaca, acidi organici, etanolo Contaminazioni chimiche e microbiche danneggia il dosaggio della bilirubina, del porfobilinogeno, · calcio, fosforo, farmaci, ormoni ... ). dell'acido aminolevulinico, poiché · Attenzione alle urine sono fotosensibili (infatti solitamente il campione è mascherato con dei fogli di alluminio); al calore, per esempio per la renina bisogna usare un bagno a freddo, perché è labilissima, come anche con l'omocisteina, che può trasformarsi in omocistinina; all'aria, per esempio l'ammoniaca e gli acidi organici sono volatili; a contaminazioni chimiche (in questo caso bisogna prestare attenzione alle urine).
Esposizione al calore · Ammoniaca, renina, ALP, lattato, Hcy
Gestione Campioni con Radioattività
Un caso particolare è quello dei pazienti che il giorno stesso sono stati sottoposti a radiologia con la somministrazione di anticorpi marcati con sostanze radioattive. I campioni presi da questi pazienti "sparano" radioattività, per cui devono essere schermati in appositi contenitori di piombo e tenuti separati da altri campioni. Per questo motivo è consigliabile richiedere un esame, conoscendo l'emivita del marcatore anticorpale usato.
Variabilità Pre-Analitica
La capacità diagnostica di un test sarà massima quando gli effetti di tutte le cause di variabilità pre-analitica sono minimizzati. Invece sarà minima quando agiscono fattori di variabilità non controllati o non conosciuti.
La variabilità pre-analitica costituisce una sorta di rumore di fondo che disturba le analisi.
Tenendola controllata si riesce a misurare la variabilità biologica, che è lo scopo principale della medicina di laboratorio.
Dosaggi di Laboratorio
La definizione di dosaggi di laboratorio è: "Procedura di biochimica clinica che consiste nell'analisi di un liquido biologico (sangue, urine e altre matrici biologiche)". L'analita si può misurare dal punto di vista qualitativo (se è presente o meno), oppure quantitativo (concentrazione esatta). L'analita può essere una proteina, DNA, mRNA o un segnale biologico (come l'attivazione di un enzima). L'esame diagnostico serve al paziente, al clinico, ma anche alla collettività.
sbobinatore: Mattia Gambuti Revisore: Giulia Fasano3. biochimica clinica 09/10/2024 Prof. Roberto Gambino
Criteri di Utilità di un Esame di Laboratorio
L'esame di laboratorio è utile:
- Per scopi diagnostici;
- Per scopi prognostici;
- Per valutare lo stato generale di salute;
- Per valutare se ci sono trattamenti di routine o d'urgenza;
- Per valutare patologie subcliniche attraverso test dinamici. Un esempio è la somministrazione orale di glucosio chiamata oGTT (oral glucose tolerance test), ossia il test di tolleranza al carico orale di glucosio;
- Per il follow-up: si monitorano tanti farmaci;
- Per lo screening: fenilchetonuria a livello neonatale, ipotiroidismo congenito e fibrosi cistica;
- Per scopi medico-legali.
Biomarcatore
Il biomarcatore è un analita, ad esempio una proteina, un enzima, un ormone, filamenti di DNA o mRNA e intermedi metabolici (es. singolo lipide). L'analita può essere direttamente misurato e usato come indicatore di processi biologici normali o patologici, in risposta ad un intervento terapeutico farmacologico o chirurgico.
Processo di Selezione dei Biomarcatori
Ogni anno per la stessa patologia si selezionano 5000 marcatori nuovi. In questi 5000 marcatori si ha una selezione precisa per cui al termine del processo ne viene selezionato solo uno. Dalla scoperta all'isolamento di un solo biomarcatore sono necessarie tappe intermedie:
- Validazione pre-clinica, associando i dati tra l'epidemiologia e la malattia. Viene effettuata su animali o volontari (un piccolo numero);
- Trials clinici, effettuata su popolazioni più numerose;
- Commercializzazione;
- Standardizzazione, per selezionare marcatori efficaci, ma soprattutto che siano utili (per esempio è inutile selezionare un biomarcatore che impiega 4-5 ore);
- Redazione delle linee guida, dando consigli sull'utilizzo del marcatore;
- Introduzione nella pratica clinica.
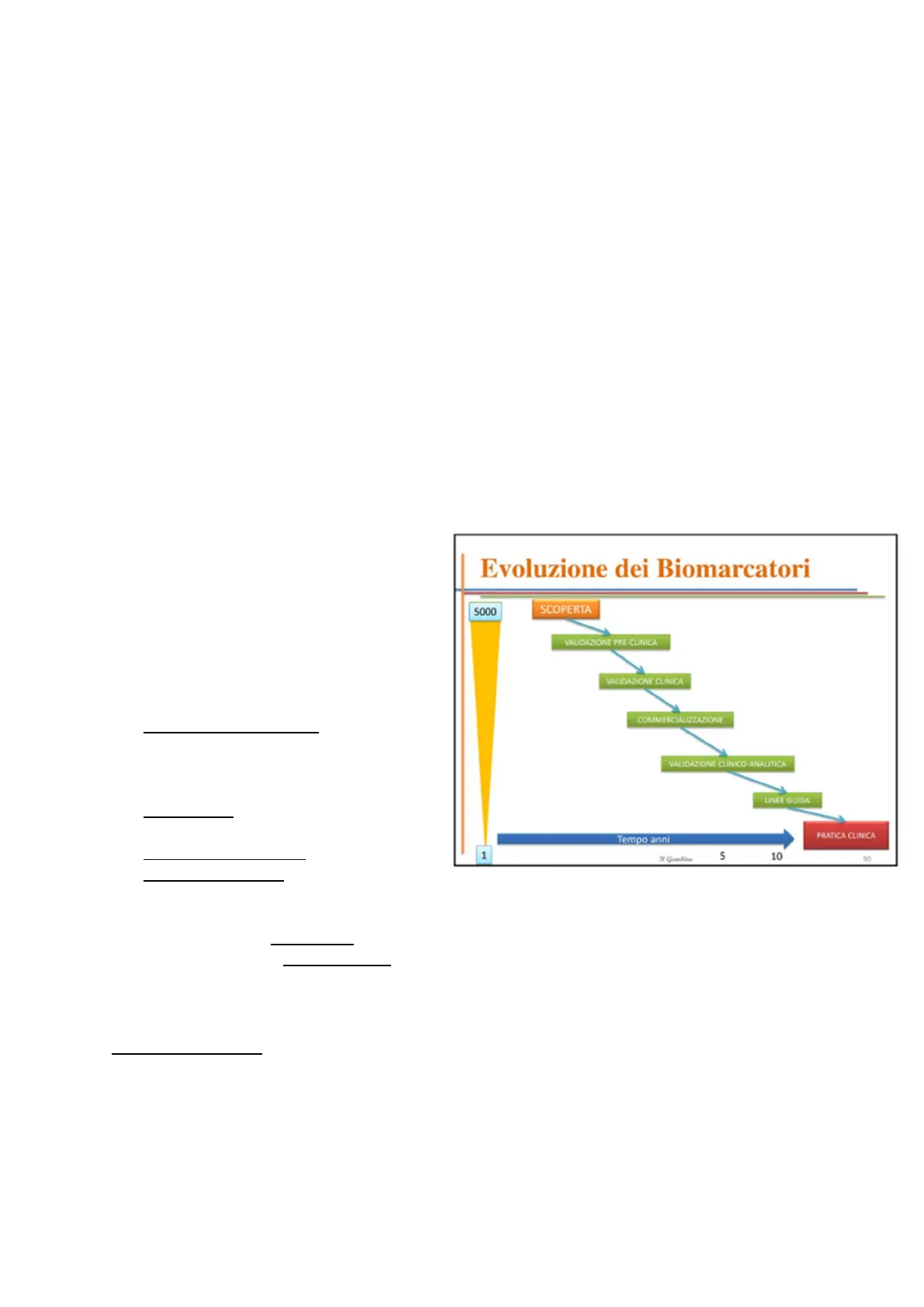
Evoluzione dei Biomarcatori 5000 SCOPERTA VALIDAZIONE PRE-CLINICA VALIDAZIONE CLINICA COMMERCIALIZZAZIONE VALIDAZIONE CLINICO-ANALITICA LINEE GUIDA PRATICA CLINICA Tempo anni 1 5 10 90
La durata di questi processi va dai 5 ai 10 anni. Per esempio il biomarcatore APO E dell'Alzheimer viene utilizzato solo ora nei laboratori, ma la sua sperimentazione è iniziata circa 25 anni fa.
Caratteristiche Ideali di un Marcatore
Le caratteristiche ideali di un marcatore sono:
- Essere presente in elevate concentrazioni nell'organo o tessuto bersaglio;
- Essere assente in organi o tessuti non bersaglio;
- Essere assente nei liquidi biologici di soggetti sani;
sbobinatore: Mattia Gambuti Revisore: Giulia Fasano3. biochimica clinica 09/10/2024 Prof. Roberto Gambino OFNOGETNO
Concentrazione biomarcatore -B. 0 1 2 3 4 5 6 7 8 9 10 Ore 0 1 2 3 4 5 6 7 8 9 10 Ore
Nella figura sono mostrati due marcatori A e B che si riferiscono a una patologia epatica. Il marcatore A sulla sinistra è presente in condizioni normali e si eleva quando il fegato è colpito da una certa malattia. Il marcatore A impiega un paio d'ore ad alzarsi e deve superare un certo valore di riferimento. Il marcatore B invece è assente in condizione normale e si eleva quando il fegato è malato. Ha un aumento più rapido rispetto al marcatore A e diventa significativo quando supera il valore di soglia.
- Essere rilasciato rapidamente nel liquido biologico a seguito di una patologia;
- Persistere in circolo o nel liquido biologico per un periodo di tempo sufficiente a garantire una finestra diagnostica.
Esempio: Marcatori Infarto del Miocardio
Esempio: nella figura ci sono tre marcatori coinvolti nell'infarto del miocardio. Il lattato raggiunge un picco dopo 30 minuti. Questo sarebbe utile, ma nel giro di un'ora ritorna normale. Infatti solitamente un paziente Determinazione impiega del tempo prima di giungere in ospedale, quindi rischierebbe di non presentare più questo valore elevato, quando viene visitato dal medico.
La lattato Concentrazione biomarcatore deidrogenasi dopo 3-4 ore sale rapidamente, ma è un . · Finestra diagnostica tempo di attesa troppo lunga. Ultimamente si usa la 0 1 2 4 5 Ore 7 8 9 troponina che a partire dalla prima ora sale rapidamente 6 e rimane elevata, per questo è il marcatore che garantisce la finestra diagnostica più adeguata.
·- Lattato -+- Troponina ++-LDH --- Cut-off 10 11 12
- Manifestare aumenti nei liquidi biologici che sono correlabili alla gravità del danno e alla prognosi;
- Deve essere misurabile nel liquido biologico in modo semplice, rapido ed economico.
Criteri per l'Introduzione di un Nuovo Marcatore
I criteri per l'introduzione di un nuovo marcatore sono:
- Misurazione dell'efficienza o prestazione diagnostica;
- Deve avere impatto clinico sull'out-come del paziente ovvero efficacia;
- Deve avere un vantaggio rispetto al marcatore vecchio (cioè deve avere un'aggiunta);
- Rapporto costo-beneficio vantaggioso. Il costo comprende tutte le fasi pre e post analitiche;
- Analisi sull'impatto organizzativo, perché deve essere introdotto in diverse terapie, percorsi terapeutici e protocolli di laboratorio.
Cause di Aumento dei Biomarcatori
Le cause di aumento dei biomarcatori sono:
- Per effetto diretto della patologia. Per esempio il CEA (proteina carcino embrionaria) è un marcatore del tumore colon-retto. Le troponine cardiache aumentano in seguito a infarto del miocardio.
- Per associazione che dipende dalla patologia. Ci sarà una conseguenza metabolica della patologia locale o sistemica, inoltre la patologia può anche avere delle complicanze. Ad esempio, la creatinina aumenta durante il diabete a causa di alterazioni della funzionalità renale; mentre la calcemia aumenta a causa di metastasi ossee.
- Per associazioni indipendenti dalla patologia, quindi per pura casualità.
sbobinatore: Mattia Gambuti Revisore: Giulia Fasano3. biochimica clinica 09/10/2024 Prof. Roberto Gambino
Efficienza ed Efficacia Diagnostica
Efficienza diagnostica: si basa su specifiche prestazioni diagnostiche di un biomarcatore identificate in base alla sensibilità diagnostica, alla specificità diagnostica e al valore predittivo.
Efficacia diagnostica: capacità di un biomarcatore di modificare l'out-come del paziente (cioè un esito biochimico).
Sensibilità e Specificità Diagnostica
Specificità diagnostica: capacità del test di individuare i soggetti realmente sani. È il rapporto tra i veri sani e la somma dei veri negativi con i falsi positivi. Indica la percentuale di sani con test negativo.
Sensibilità diagnostica: capacità del test di individuare i soggetti realmente malati. È il rapporto tra i veri malati e la somma dei veri positivi con i falsi negativi. Indica la percentuale di malati con test positivo.
VP X 100 · Specificità X 100 VP + FN VN + FP
Ho riportato lo schema delle formule (prese da internet). VP: VERO POSITIVO, VN: VERO NEGATIVO, FN: FALSO NEGATIVO, FP: FALSO POSITIVO.
L'immagine a destra rappresenta due curve che dividono la popolazione in sani e malati. Le due curve sono separate da un valore di cut-off. La separazione non è netta e generalmente c'è un po' di promiscuità tra i veri positivi, che hanno dei parametri diagnostici negativi (falsi negativi), e i veri negativi con parametri alterati (falsi positivi). Spostando la linea di cut-off a destra aumenta la specificità però si riduce la sensibilità.
Nell'immagine in basso sono rappresentate due popolazioni in rosso e in blu. Nel grafico, sull'asse delle ordinate ci sono i veri positivi e sulle ascisse i falsi positivi. Dalla curva sigmoidea che si ottiene si può capire qual è il valore ideale di cut-off per un determinato test analitico; infatti si prende come valore ideale il punto più in alto a sinistra della curva. Le due curve vengono chiamate curve ROC.
Sensibilità e Specificità Diagnostica Sensibilità Specificità % dei sani con test negativo % dei malati con test positivo a d a+b c+d CUT OFF + Specificità d Malattia V- a V+ F- F+ 98 b & Çamfine Curve ROC (Receiver Operating Characteristic) 100% True Positive Rate (sensitivity) 0% 0% 100% False Positive Rate (1-specificity) 3 Gambina 99
Predittività di un Test
La predittività indica la probabilità che un paziente con test positivo sia veramente malato e che un paziente con test negativo sia veramente sano.
sbobinatore: Mattia Gambuti Revisore: Giulia Fasano . VN · Sensibilità