Medicina moderna e nuove tecnologie: progressi e applicazioni
Documento dall'Università sulla Medicina Moderna e le Nuove Tecnologie. Il Pdf esplora i progressi della medicina, dalla chirurgia ricostruttiva ai trapianti d'organo e alla terapia cellulare, con diagrammi esplicativi sulla biocompatibilità e la composizione del sangue, utile per studenti universitari di Biologia.
Mostra di più17 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Medicina Moderna e Nuove Tecnologie
In primi interventi chirurgici avevano due problematiche principali:
- Mancanza di farmaci anestetici
- Sviluppo di infezioni: questa problematica venne risolta nel 1929, quando il batteriologo Fleming scoprì che una muffa (Penicillium) conteneva una sostanza (antibiotico) capace di bloccare la crescita di alcuni batteri.
Si sviluppa cosi la chirurgia ricostruttiva che andava a sostituire i tessuti danneggiati con nuovi tessuti. Diventa così necessario trovare tessuti che possano sostituire quelli naturali. Così negli anni 60' nasce la medicina degli organi artificiali e dei trapianti d'organi. I limiti per questa medicina sono:
- Il rigetto: il sistema immunitario riconosce le cellule estranee da quelle interne grazie a un sotto-gruppo di LINFOCITI T e cerca quindi di eliminarle. Questo problema è stato in parte risorto grazie ad alcuni farmaci in grado di inibire la reazione di rigetto del sistema immunitario (es. ciclosporina)
- Gli organi artificiali non sono in grado di sostituire in modo complete le funzioni biologiche
- La quantità limitata di organo (da donatori o cadaveri) ciò causa liste d'attese molto lunghe dove solo il 10 % di chi necessita l'organo riesce ad accedevi
Negli ultimi anni ha preso piede la terapia cellulare: sfrutta cellule embrionali prelevate da un altro soggetto o create in laboratorio, che essendo cellule staminali sono facili da manipolare. Tuttavia per evitare il rigetto si dovrebbero utilizzare quelle del paziente (non sempre facili da ottenere). Il trapianto, quindi deve essere sempre accompagnato dalla terapia anti-rigetto oppure terapia del auto-trapianto.
Oggi si parla di evidence based medicine ovvero si curano i pazienti sulla base di cure scientificamente dimostrate. Per cui la sperimentazione clinica deve dimostrare che un certo trattamento è efficace. Il tutto si basa sul clinical trials che consiste nella misurazione e la raccolta dei dati sfruttando la tecnologia. Possiamo anche parlare di medicina personalizzata poiché i medici creano per ogni paziente un trattamento ad hoc.
La Biocompatibilità
I materiali che vengono inseriti nel corpo, così come le loro forme e geometrie, non devono indurre fenomeni che possono alterare il funzionamento del corpo umano o dell'organo/tessuto. Non esiste un materiale biocompatibile al 100% quindi alcune complicanze possono sempre insorgere. anche quando il dispositivo viene accettato dall'organismo. È quindi importante cercare di minimizzare queste complicanze e tenerle sotto controllo.
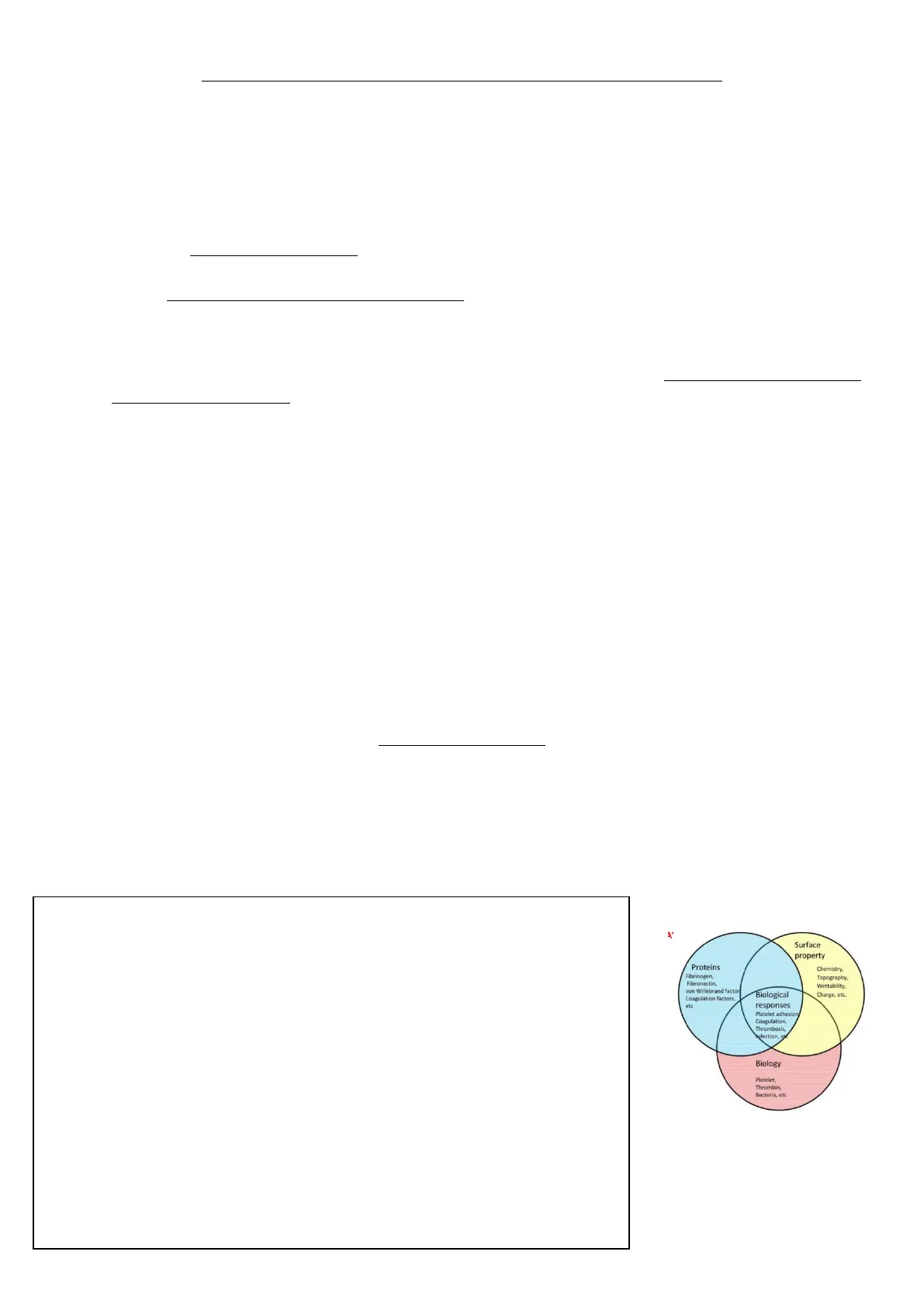
Diagramma di Venn della Biocompatibilità
Diagramma di Venn: ogni cerchio rappresentante un aspetto chiave della biocompatibilità. L'immagine sottolinea che la biocompatibilità dipende dall'interazione complessa tra:
- Le proprietà del materiale (chimiche e fisiche),
- Il comportamento delle proteine adsorbite, che influenzano la risposta cellulare,
- Il sistema biologico ospite (cellule e molecole).
In sintesi, un materiale biocompatibile deve armonizzare questi tre aspetti per evitare risposte avverse (ad esempio, trombosi o infezioni) e supportare l'integrazione funzionale nel corpo umano. Tra le poste biologiche è importante quella cellulare che si attiva quando perturbiamo il tessuto o un organo.
Surface property Proteins Fibrinogen, Fibronectin, von Willebrand factor Coagulation factors, etc Chemistry, Topography, Wettability, Charge, etc. Biological responses Platelet adhesion Coagulation, Thrombosis, fection, ey Biology Platelet, Thrombin, Bacteria, etc
Composizione del Sangue
[ sangue è un tessuto connettivo fluido essenziale per il trasporto di sostanze, la regolazione del corpo e la difesa immunitaria. È composto da una parte liquida (plasma) e da una parte corpuscolata (cellule e frammenti cellulari). Di seguito, la sua composizione:
- Parte liquida: Plasma Il plasma rappresenta circa il 55% del volume totale del sangue. È un liquido giallastro composto da:
- Acqua (circa il 90%): Agisce come solvente per sostanze trasportate nel sangue.
- Proteine plasmatiche: o Albumina: Mantiene la pressione osmotica e trasporta molecole come ormoni e farmaci. o Globuline: Comprendono anticorpi (immunoglobuline) e proteine di trasporto. o Fibrinogeno: Coinvolto nella coagulazione del sangue.
- Sali e ioni: Sodio, potassio, calcio, magnesio, cloruro, bicarbonato, ecc., essenziali per il bilancio elettrolitico e il pH.
- Sostanze nutritive: Glucosio, aminoacidi, lipidi.
- Ormoni: Molecole regolatrici del metabolismo.
- Prodotti di scarto: Urea, acido urico, creatinina.
- Gas disciolti: Ossigeno, anidride carbonica, azoto.
- Parte corpuscolata: Elementi figurati Rappresenta circa il 45% del volume del sangue e comprende tre tipi principali di cellule:
Globuli Rossi (Eritrociti)
a. Globuli rossi (Eritrociti)
- Funzione: Trasportano l'ossigeno dai polmoni ai tessuti e l'anidride carbonica dai tessuti ai polmoni.
- Struttura: Dischi biconcavi privi di nucleo (negli adulti) contenenti emoglobina, una proteina che lega l'ossigeno.
- Concentrazione: Circa 4,5-6 milioni per microlitro di sangue.
Globuli Bianchi (Leucociti)
b. Globuli bianchi (Leucociti) > BUFFY COAT 1% è formato da globuli bianchi e piastrine
- Funzione: Difesa immunitaria e risposta contro infezioni e agenti estranei.
- Tipi: o Granulociti: · Neutrofili: Fagocitosi di batteri e detriti. · Eosinofili: Difesa contro parassiti e reazioni allergiche. · Basofili: Producono istamina e sono coinvolti nelle risposte allergiche. o Agranulociti: · Linfociti: Immunità adattativa (linfociti T e B). · Monociti: Si trasformano in macrofagi nei tessuti e fagocitano patogeni e cellule morte.
- Concentrazione: Circa 4.000-11.000 per microlitro di sangue.
Piastrine (Trombociti)
c. Piastrine (Trombociti)
- Funzione: Coinvolte nella coagulazione e nella riparazione dei vasi sanguigni danneggiati.
- Struttura: Frammenti cellulari derivati dai megacariociti.
- Concentrazione: Circa 150.000-450.000 per microlitro di sangue.
- Sono prodotti mediante teso di grassi di megacarioblasti e hanno una vita media di 10 giorni . Sono attivatori del processo di coagulazione ed emettono pseudopodi che si occupano di adesione, attivazione, secrezione e aggregazione. . Nucleo e questo permette loro di cambiare forma quando aderiscono a qualcosa
Ruolo del Sangue
Ruolo del sangue
- Trasporto: Di ossigeno, anidride carbonica, nutrienti, ormoni e prodotti di scarto.
- Regolazione: Del pH, temperatura corporea ed equilibrio idrico.
- Protezione: Attraverso leucociti, anticorpi e meccanismi di coagulazione.
L'emostasi e la coagulazione sono i due processi che arrestano la fuori uscita di sangue da un vasp danneggiato. Sono 3 le fasi:
- Formazione di fibrilla:
a. Vasocostrizione: il danno alla superficie provoca il rilascio di alcuni fattori vasocostrittori che agiscono nelle arterie a livello della lesione per contrastare la perdita di sangue b. Aggregazione plastica: le cellule endoteliali a causa della lesione secernono una proteina che permette l'adesione delle piastrine, che a loro volta rilasciano citochine (trombossano A2) che attirano altre piastrine che a loro volta si accumulano lungo la lesione. c. Coagulazione: la fibrina stabilizza l'aggregato. Il processo di attivazione della fibrina segue meccanismo a catena a cui partecipano molti fattori:
Via Intrinseca
i. Via intrinseca: si attiva quando il sangue entra in contatto con superfici anomale (ad esempio, superfici cariche negativamente, come il collagene esposto in un vaso danneggiato). È la via più lenta che si innesca con l'attivazione di XI che si verifica quando il sangue entra in contatto con la matrice extracellulare. Il contatto attiva il Fattore XII che una volta attivato (XIIa) converte il Fattore XI in Fattore XIa che a sua volta converte il Fattore IX in Fattore IXa. Il Fattore IXa si associa al Fattore Villa e al calcio su una superficie fosfolipidica (ad esempio, piastrine attivate). Questo complesso attiva il Fattore X, portando alla via comune.
Via Estrinseca
ii. Via estrinseca: si attiva in risposta a danni tissutali che portano all'esposizione del fattore tissutale (tromboplastina) un elemento che normalmente non è presente nel sangue circolante. Il TF si lega al Fattore VII, formando un complesso TF-FVIIa che converte il Fattore X in Fattore Xa, portando direttamente alla via comune.
Via Comune
iii. Via comune: Le due vie, intrinseca ed estrinseca, convergono nella via comune per generare fibrina. Il Fattore Xa, insieme al Fattore Va e al calcio, forma il complesso protrombinasi, che converte la protrombina in trombina. La trombina a sua volta converte il fibrinogeno solubile in fibrina insolubile. La fibrina viene poi reticolata dal Fattore XIIIa (attivato dalla trombina), formando una rete stabile che sigilla il sito del danno. IL fibrinogeno presenta tre eliche con ponti di solfuro, finché sono attaccati non crea coaguli, ma se si staccano il fibrinogeno crea la catena di fibrina
- Detrazione del coagulo: è il processo in cui le piastrine contraggono la rete di fibrina, riducendo il volume del coagulo e stabilizzandolo. Questo favorisce la chiusura della ferita, la riparazione del tessuto e il ripristino del flusso sanguigno. È fondamentale per prevenire emorragie e garantire una guarigione efficace.
- Fibrolisi: è il processo che dissolve i coaguli di fibrina dopo la guarigione della lesione. Il plasminogeno viene trasformato in plasmina dal t-PA (attivatore tissutale del plasminogeno) o dal u-PA (urochinasi), che degrada la fibrina in frammenti solubili. t-PA è sintetizzato dalle cellule endoteliali che lo riversano continuamente in circolo, dove si trova libero o complessato con gli inibitori. Questo ripristina il normale flusso sanguigno e previene l'eccessiva trombosi.
Tutto questo per dire che quando dobbiamo inserire un materiale artificiale dobbiamo fare in modo che le piastrine lo accettino tenendo sotto controllo la cascata coagulativa per evitare la formazione di coaguli trombi. La componente cellulare che riveste la superficie più interna dei vasi è la cellula endoteliale. Gli elementi circolanti nel sangue non entrano direttamente contatto con le cellule endoteliali grazie a uno stato di proteine (proteoglicani, acido ialuronico e carboidrati) chiamato glicocalice. Esso presente una carica negativa che permette la repulsione delle proteine plasmatiche e delle piastrine.
- Se sulla superficie aderisce il fibrinogeno le piastine si attivano e di conseguenza si forma il trombo
- se il fibrinogeno è circolante espone dei siti di legame non utilizzabili dalle piastrine e quindi non avviene la coagulazione
> Il fattore di von Willebrand (vWF) è una glicoproteina essenziale per l'emostasi, coinvolta sia nell'adesione piastrinica sia nella stabilizzazione del fattore VIII della coagulazione. Ha una struttura complessa e dinamica. Si tratta di una glicoproteina multimerica, con forme che variano da monomeri a grandi multimeri, i quali rappresentano la forma biologicamente più attiva. Bene come il VWF sono sensibili alle condizioni di moto I materiali artificiali non hanno un rivestimento simile al glicocalice quindi potrebbe esserci qualcosa che faccia aderire le piastrine. Le proteine del biomateriale a contatto con l'organismo possono quindi dare origine alle:
- cascata coagulativa
- attivazione del sistema del complemento: quando l'anticorpo riconosce l'antigene attiva la cascata coagulativa.
Sistema del Complemento
l sistema del complemento è costituito da oltre 30 proteine, principalmente prodotte dal fegato, che circolano nel sangue in forma inattiva (proenzimi). Quando ANTIGENE: SOSTANZA ESTRANEA CHE STIMOLA LA ANTIGENE PRODUZIONE DI ANTICORPI attivato, il sistema opera attraverso una cascata di reazioni enzimatiche per proteggere l'organismo da agenti patogeni. Il sistema del complemento può essere attivato attraverso tre vie SITI DI LEGAME PER L'ANTIGENE principali: LA REAZIONE FRA ANTICORPO E ANTIGENE E SPECIFICA: SI PARLA DI ANTICORPI MONOCLONALI QUANDO QUESTI SONO DEI CLONI DI UN ANTICORPO PRODOTTO DAI LINFOCITI B
Via Classica
1. Via classica: Si attiva quando gli anticorpi (IgG o IgM) legano un antigene sulla superficie di un patogeno. CATENA LEGGERA Questo complesso antigene-anticorpo attiva la proteina C1 che a sua volta produce una catena più ridotta C1a che permette l'interazione con altre molecole. Trasforma C4 CATENA PESANTE in C4b e C2 in C2a questo permette altre trasformazioni fino alla produzione del complesso molecolare MAC (membrane attack complex). Il MAC ha una forma ad M MEDICINA ONLINE anello con un diametro di circa 10 nm ed è in grado di attraversare il doppio strato lipidico della membrana cellulare, creando un canale idrofilo. Gli ioni cambiano il potenziale di membrana fino a distruggere il batterio ANTICORPO LA MOLECOLA DI UN ANTICORPO HA UNA FORMA A Y FORMATA DA DUE IDENTICHE CATENE PESANTI E DUE IDENTICHE CATENE LEGGERE
Via Alternativa
2. Via alternativa: si attiva in modo spontaneo quando il complemento riconosce superfici non-self, come quelle dei patogeni. Il materiale a contatto con il sangue fa aderire le proteine C3 che si trasformano in C3a e C3b. Le C3a permettono di attivare le cellule del sistema immunitario che crea le citochine (attivano i macrofagi, i neutrofili e altre cellule coinvolte nella risposta immunitaria rapida, Promuovono l'infiammazione per contenere e distruggere gli agenti patogeni), che una volta esaurita la propria funzione da inizio alla fagocitosi (osponization) Le malattie autoimmuni, come le allergie, si verificano quando gli anticorpi attivano reazioni autoimmuni contro un antigene che è dell'organismo stesso.