Formule di Lewis: Ibridi di risonanza e carica formale, Presentazione
Slide da Adt su Formule di Lewis: Ibridi di risonanza e carica formale. Il Pdf è una presentazione di Chimica di livello universitario che esplora il calcolo delle cariche formali per molecole come HCN, con esempi dettagliati e tabelle riassuntive.
Mostra di più17 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Chimica
Ibridi di risonanza e carica formale
Ibridi di risonanza
Gli ibridi di risonanza sono delle molecole la cui struttura reale è intermedia tra due o più possibili strutture di Lewis.
Non tutte le proprietà manifestate da una specie chimica possono essere di norma spiegate in base ad un'unica formula di struttura. A volte una specie chimica si comporta come se, contemporaneamente, avesse formule di struttura diverse.
Ibridi di risonanza dell'ozono
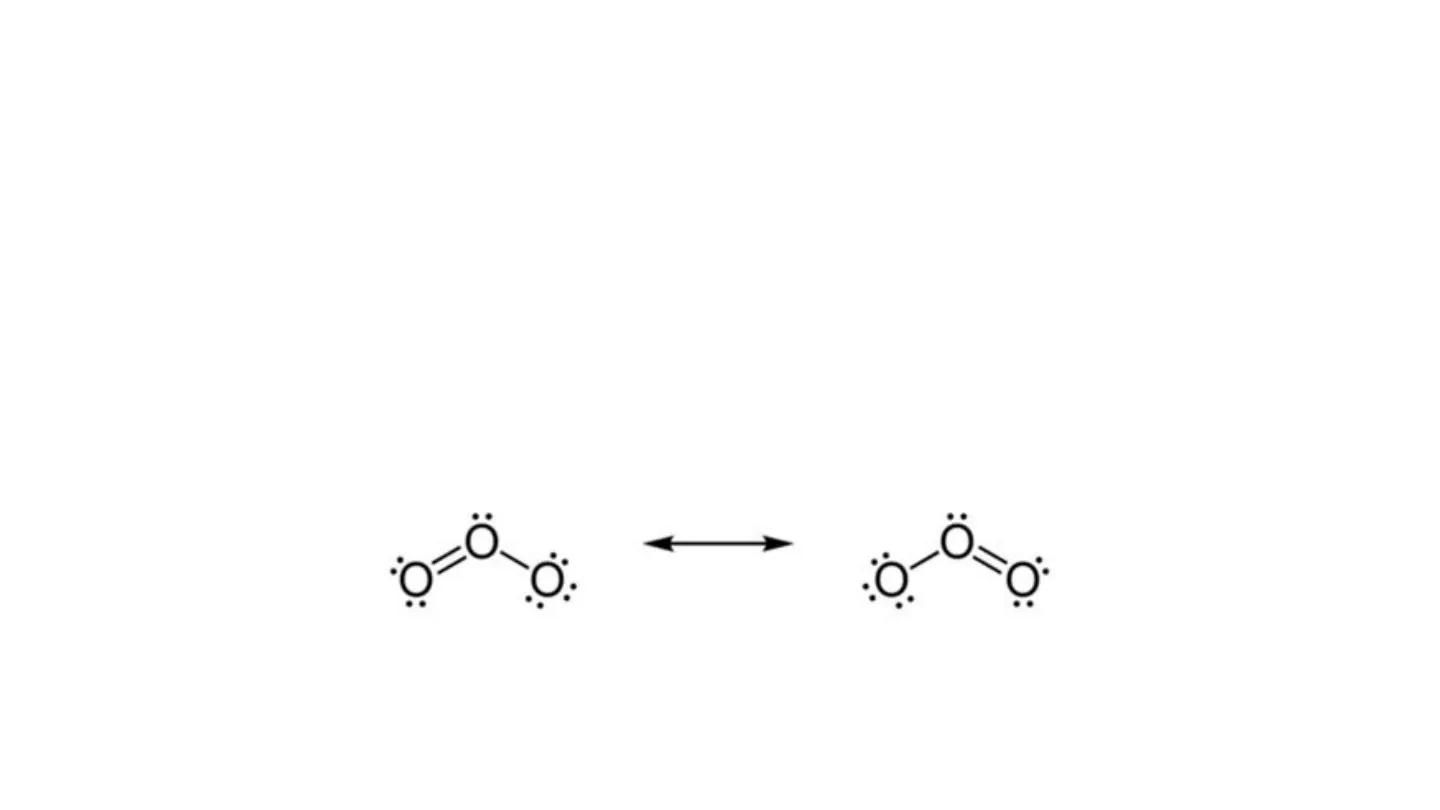
La molecola dell'ozono O3 è formata da tre atomi di ossigeno legati tra loro. Essa può essere rappresentata dalla seguente struttura di Lewis:
Tuttavia, l'evidenza sperimentale suggerisce che in O3 i due legami tra gli atomi di ossigeno sono identici e che la loro lunghezza è circa a metà tra quella di un legame semplice e quella di uno doppio. Questa formula di struttura, quindi, non rappresenta la realtà.
Poiché non è possibile distinguere un legame dall'altro, possiamo di fatto scrivere due diverse strutture, che si differenziano solo per la posizione del doppio legame:
Entrambe le formule di struttura soddisfano la regola dell'ottetto.
Forme limite e risonanza
Tali formule di struttura sono dette forme limite. La molecola reale è un ibrido derivato dal contributo di entrambe le forme limite. A questo ibrido si dà il nome di ibrido di risonanza.
La risonanza tra le formule limite viene indicata da una freccia a doppia punta 7.
Altro esempio: SO3 2- :0: :0: S S S 1 0 O :0 O O:
La regola dell'ottetto è soddisfatta in ognuna delle forme di risonanza!
Quando un composto possiede due o più strutture di Lewis che contribuiscono a determinare la struttura reale, diciamo che quel composto mostra la proprietà della risonanza.
Importanza della risonanza
NOTA BENE:
- La presenza della risonanza fa aumentare la stabilità di una molecola. Più forme di risonanza si possono scrivere, maggiore è la stabilità della molecola che esse rappresentano.
· Molto spesso nella spiegazione della risonanza si pensa che la molecola reale oscilli fra le varie strutture di risonanza, ma non si tratta di un equilibrio tra più forme!
· Le diverse forme risonanti di una molecola non rappresentano né stati separati coesistenti né stati successivi nel tempo, ma esprimono il fatto che la molecola presenta contemporaneamente le proprietà di tutte le forme risonanti.
- La risonanza è piuttosto un modello che ci aiuta a rappresentare visivamente la disposizione degli elettroni nei casi in cui essa è troppo complessa da poter essere descritta adeguatamente con un'unica struttura di Lewis.
. Il fatto che queste vengano rappresentate in modo separato è dovuto alla difficoltà di rappresentare una molecola con un unico schema.
Definizione di carica formale
Cos'è la carica formale?
- Si definisce carica formale la carica che un atomo avrebbe se in una molecola tutti i suoi legami fossero considerati covalenti puri.
- La carica formale è un'indicazione della misura con cui gli atomi hanno acquistato o ceduto elettroni nei loro orbitali durante la formazione dei legami covalenti.
- Come si calcola la carica formale per ogni atomo della molecola/dello ione? Carica formale = n.elettroni valenza - n.legami - n.elettroni solitari
- La carica globale di un composto è sempre uguale alla somma delle cariche formali degli atomi che costituiscono tale composto.
Cariche formali e struttura di Lewis
Le cariche formali non sono cariche reali e non sono misurate esse sono utili solo nel contesto della rappresentazione di Lewis di una molecola e aiutano a prevedere la disposizione più favorevole degli atomi nelle molecole e la struttura di Lewis più probabile per tale disposizione.
La somma delle cariche formali degli atomi di una molecola o di uno ione deve sempre essere uguale alla carica netta sulla molecola o ione.
Calcolo cariche formali: HCN
Calcolo cariche formali: HCN H-C=N:
| Elemento | Elettroni valenza | Numero legami | Numero elettroni solitari | Carica formale |
|---|---|---|---|---|
| H | 1 | 1 | 0 | 0 |
| C | 4 | 4 | 0 | 0 |
| N | 5 | 3 | 2 | 0 |
Calcolo cariche formali: HCN (alternativa)
Calcolo cariche formali: HCN H-N=C:
| Elemento | Elettroni valenza | Numero legami | Numero elettroni solitari | Carica formale |
|---|---|---|---|---|
| H | 1 | 1 | 0 | 0 |
| C | 4 | 3 | 2 | -1 |
| N | 5 | 4 | 0 | +1 |
Scelta della struttura di Lewis più plausibile per HCN
Calcolo cariche formali: HCN Come si procede? Quale struttura di Lewis scegliere tra le due?
La struttura piu plausibile deve: 1- Presentare le cariche formali piu basse (meglio se nulle). 2- Evitare di attribuire una carica formale di segno positivo all'atomo piu elettronegativo. 3- Evitare la contemporanea presenza di cariche formali di segno opposto su atomi adiacenti.
Quindi nel caso di HCN la prima struttura è piu plausibile anche se la seconda è comunque possibile! H-C=N: H-N=C:
Calcolo cariche formali: CO2
Calcolo cariche formali: CO 2 A: 0 = c = 0 B: :0=0 -0: .. C 0 = 0 = C :
A:
| Elemento | Elettroni valenza | Numero legami | Numero elettroni solitari | Carica formale |
|---|---|---|---|---|
| C | 4 | 4 | 0 | 0 |
| O | 6 | 2 | 4 | 0 |
| O | 6 | 2 | 4 | 0 |
A:
| Elemento | Elettroni valenza | Numero legami | Numero elettroni solitari | Carica formale |
|---|---|---|---|---|
| C | 4 | 3 | 2 | -2 |
| O | 6 | 1 | 6 | +2 |
| o | 6 | 1 | 6 | 0 |
A:
| Elemento | Elettroni valenza | Numero legami | Numero elettroni solitari | Carica formale |
|---|---|---|---|---|
| C | 4 | 2 | 0 | 0 |
| o | 6 | 4 | 0 | +1 |
| o | 6 | 2 | 4 | -1 |
Fondamento concettuale: Fase 1 e 2
Il fondamento concettuale Fase 1: Si contano gli elettroni di valenza di ciascun atomo; per gli ioni si aggiungono o si tolgono elettroni in funzione della carica.
Fase 2: Si formula la disposizione piu probabile degli atomi servendosi della semplicissima regola di scegliere come atomo centrale l'atomo con minore elettronegatività. Es. H2CO3 -> l'atomo centrale è il carbonio, l'idrogeno è sempre esterno.
Fase 3: Si colloca una coppia di elettroni nello spazio tra gli atomi legati. H 0: ·C· · Ö: .
Fondamento concettuale: Fase 4 e 5
Il fondamento concettuale Fase 4: Si completa l'ottetto (il doppietto per H) di ciascun atomo disponendo intorno all'atomo gli elettroni eventualmente rimasti. Si INIZIA con gli atomi periferici per poi passare all'atomo centrale. Se non vi sono abbastanza elettroni, si formano legami multipli.
Fase 5: Nel caso di presenza di più possibili strutture di Lewis, se queste differiscono nella posizione di un doppio legame tra coppie identiche si tratta di risonanza, se invece la differenza consiste in una disposizione alternativa degli atomi, utilizzare il calcolo della carica formale per stabilire qual'è la struttura di Lewis piu probabile. Se si tratta di uno ione menzionare sulla molecola la carica.
Primo esempio: ione clorito (ClO2)-
Primo esempio: ione clorito (CIO2)- Fase 1: Si contano gli elettroni di valenza di ciascun atomo; per gli ioni si aggiungono o si tolgono elettroni in funzione della carica. In questo caso: 7 (Cl) + 6 (O) + 6 (O) + 1 (ione) = 20, quindi 10 coppie di elettroni (leganti e solitarie).
Fase 2: Si formula la disposizione piu probabile degli atomi servendosi della semplicissima regola di scegliere l'atomo centrale come l'atomo con minore elettronegatività. In questo caso: O CI O
Fase 3: Si colloca una coppia di elettroni nello spazio tra gli atomi legati. In questo caso: O-Cl-O Si identificano le coppie di elettroni non ancora collocate: In questo caso: 10 coppie di elettroni totali- 2 coppie collocate nello spazio = 8 coppie di elettroni non ancora collocate
Ione clorito: Fase 4/5 e possibilità
Primo esempio: ione clorito (CIO2)- Fase 4/5: Si completano gli ottetti prima provando con i soli doppietti solitari, se non bastano anche con i doppi legami. Si valutano le varie possibilità.
Prima possibilità: .. 0-çı-0 0 =- 1 Cl = +1 0 =- 1
Terza possibilità: 0Çı=0 0 =- 1 + CI= 0 + 0=0
Seconda possibilità: @_@1 - 0:
Quarta possibilità: 0= 0 + CI=0 + 0 =- 1 0=0 + CI =- 1 + 0=0
7 (Cl) + 6 (O) + 6 (O) + 1 (ione) = 20, quindi 10 coppie di elettroni (leganti e solitarie).
Ione clorito: Risonanza
Primo esempio: ione clorito (CIO2)" Quindi:
Nel caso di presenza di più possibili strutture di Lewis, se queste differiscono nella posizione di un doppio legame tra coppie identiche si tratta di risonanza, se invece la differenza consiste in una disposizione alternativa degli atomi, utilizzare il calcolo della carica formale per stabilire qual'è la struttura di Lewis piu probabile.
Se si tratta di uno ione menzionare sulla molecola la carica.
Qual è il nostro caso? La risonanza !! [ö -- ö] - [ö=@-ö.]
Conclusione
Alla prossima lezione! Chimica