Reazioni di sostituzione nucleofila: meccanismi SN1 e SN2 in Chimica
Documento sulle reazioni di sostituzione nucleofila. Il Pdf esplora i meccanismi SN1 e SN2, l'ingombro sterico e la stabilità dei carbocationi intermedi, con esempi e diagrammi per la Chimica universitaria.
Mostra di più10 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Reazioni di sostituzione nucleofila
Le reazioni di sostituzione nucleofila sono reazioni nelle quali una specie nucleofila legata ad un atomo di carbonio del substrato viene sostituita da un'altra specie nucleofila Nella figura il nucleofilo che viene sostituito, che si chiama gruppo uscente, è disegnato in viola, mentre il nucleofilo che prende il suo posto è disegnato in rosso.
induced dipole set up 8- 8+ approaching negative ion electrons repelled towards the iodine end of the bond
Le specie nucleofile sono normalmente più elettronegative dell'atomo di carbonio; per questo motivo l'atomo di carbonio legato al gruppo uscente assume una parziale carica positiva, quindi ha caratteristiche elettrofile e costituisce un buon punto di attacco per il nucleofilo entrante. I substrati che più comunemente sono coinvolti nelle reazioni di sostituzione nucleofila sono gli alogenuri alchilici, in quanto gli alogeni (in particolare cloro, bromo e iodio, non il fluoro per ragioni che vedremo più avanti) sono buoni gruppi uscenti. I reattivi nucleofili che possono fungere da gruppi entranti sono invece molti. Possono essere ioni negativi o specie neutre. Le tabelle in fondo a pagina 136 del vostro libro di testo e quella qui a fianco ne riportano alcuni.
Nucleofilia
Nucleofili
+ I", HS", RS" Br, HO". RO", CN", N3 NH3, CI-, F. RCOO" I H2O. ROH RCOOH
La probabilità che avvenga la reazione di sostituzione nucleofila, non è però solo legata alla carica parziale dell'atomo di carbonio, ma dipende da molti fattori, tra i quali:
- la forza del nucleofilo entrante
- la facilità con cui il nucleofilo uscente tende a lasciare il carbonio al quale è legato (in questo caso si parla di buon o cattivo gruppo uscente a seconda dei casi)
- dalle caratteristiche del substrato
Fattori che influenzano la forza del nucleofilo (nucleofilia)
Un nucleofilo è una specie che presenta una coppia di elettroni non condivisa da poter mettere in gioco per formare un legame chimico con una specie elettrofila Un nucleofilo è tanto più forte quanto maggiore è la sua tendenza a mettere a disposizione la coppia di elettroni liberi I principali fattori influenzano la nucleofilia sono:
a) carica elettrica: gli ioni negativi sono più nucleofili, delle molecole neutre corrispondenti (a parità di atomo che mette a disposizione la coppia di elettroni). Ad esempio:
- OH- è più nucleofilo di H2O;
- RS- è più nucleofilo di RSH,
- RO è più nucleofilo di ROH
b) elettronegatività/polarizzabilità: confrontando atomi che portano la coppia di elettroni, sono più nucleofili quelli meno elettronegativi di quelli più elettronegativi e quelli che hanno dimensioni maggiori rispetto a quelli che hanno dimensioni minori: entrambi i fattori infatti influenzano la capacità di tali atomi di trattenere o meno i propri elettroni, ad esempio:
- NH3 è più nucleofilo di H2O che è più nucleofilo di HF;
- HS- è più nucleofilo di OH ;
- I- è più nucleofilo di Br che è più nucleofilo di Cl- che è più nucleofilo di F-
Nucleofilia e basicità
Sappiamo che le specie nucleofile sono basi di Lewis. Questo significa che un nucleofilo più forte è anche una base più forte? In molti casi si, ma non sempre. Ad esempio, considerando gli esempi forniti in precedenza, per quelli scritti in blu, la specie più nucleofila è anche quella più basica, mentre per quelli mostrati in rosso è il contrario: la specie più nucleofila è quella meno basica. IQuesto perché la basicità di una specie chimica dipende dall'equilibrio acido-base con l'acido coniugato: più una base è stabile, meno è forte, in quanto avrà bassa tendenza a protonarsi. Per questo lo ione I-, di grandi dimensioni, potendo distribuire la carica negativa in uno spazio grande è meno basico, in quanto più stabile, dello ione F- che invece ha piccole dimensioni quindi una elevata densità di carica negativa. Di conseguenza lo ione F- tenderà maggiormente a protonarsi (maggiore basicità), dello ione I -. Viceversa la nucleofilia è una proprietà cinetica, legata alla capacità di una specie chimica di mettere a disposizione una coppia di elettroni non condivisi per reagire velocemente con una specie carente di elettroni (elettrofila). È evidente che tale capacità è maggiore se tali coppie di elettroni liberi sono debolmente trattenute dalla specie nucleofila. Per questo motivo lo ione I- è più nucleofilo dello ione F-, pur essendo meno basico Carica elettrica ed elettronegatività non sono però gli unici fattori che influenzano la nucleofilia, ne esistono anche altri che rivestono un ruolo importante a livello di reattività chimica. In generale, tutti gli aspetti che in qualche modo ostacolano la disponibilità di un nucleofilo a cedere la coppia di elettroni liberi incidono sulla nucleofilia. Di seguito ne vediamo altri due: l'ingombro sterico del nucleofilo le caratteristiche del solvente.
Ingombro sterico del nucleofilo
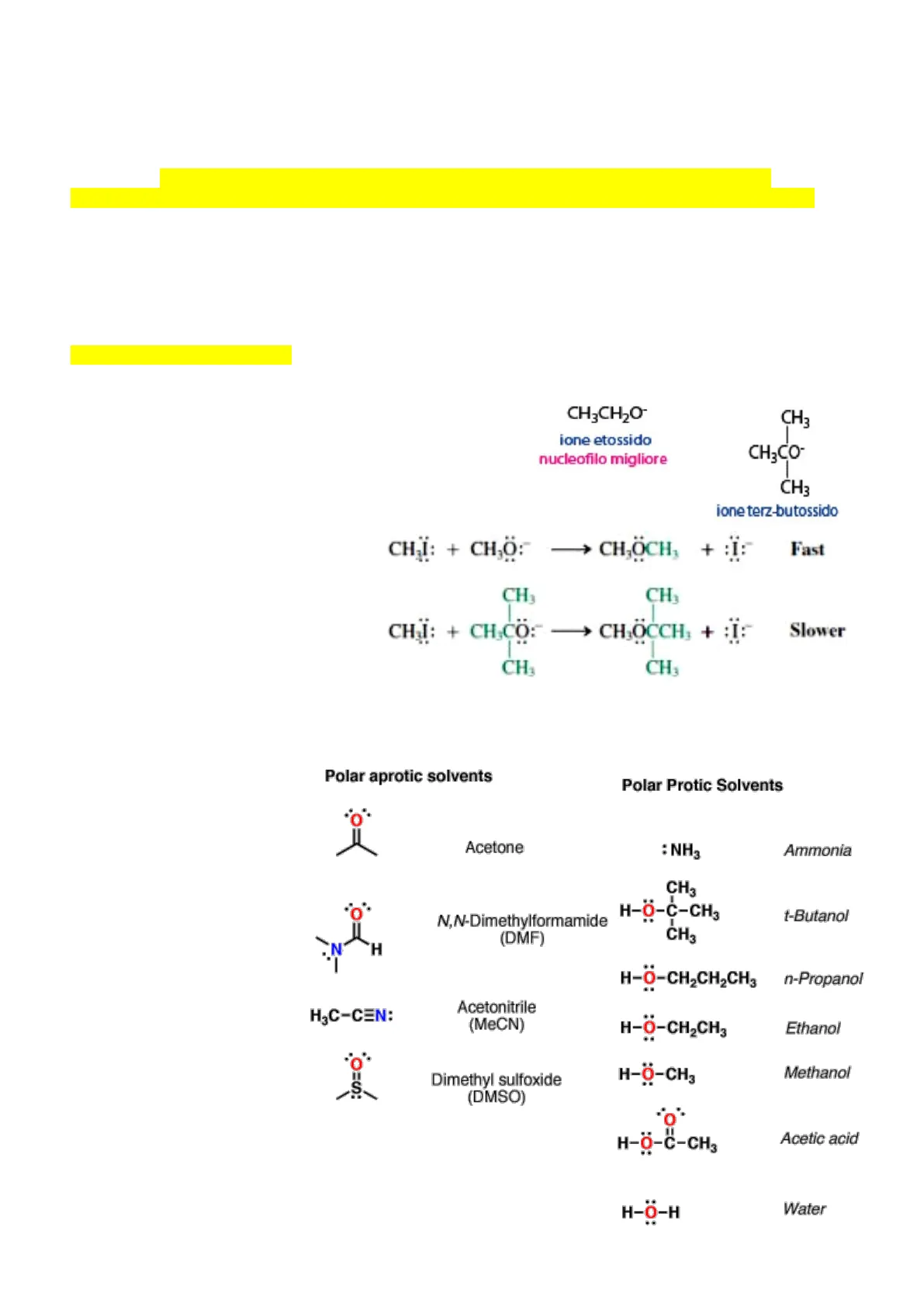
Se in un nucleofilo, l'atomo che porta la coppia di elettroni si trova legato ad un carbonio fortemente ingombrato, cioè con molti sostituenti intorno, la specie chimica nel suo complesso faticherà ad avvicinarsi al centro elettrofilo del substrato. Ad esempio, come mostra la figura a fianco, lo ione etossido è un nucleofilo migliore dello ione terz-butossido, semplicemente perché ha meno difficoltà ad avvicinarsi al centro elettrofilo. La conseguenza è quella mostrata nella figura seguente che mostra due reazioni di sostituzione nucleofila dei due reattivi con lo stesso substrato: la reazione con il terz- butossido è più lenta, perché il reattivo fatica ad avvicinarsi al substrato
CH3CH2O- ione etossido nucleofilo migliore CH3 CH3CO- CH3 ione terz-butossido CHI: + CH,O: ·CH,OCH, + I: Fast CH CH3 CH CHI: + CH.CO: - > CHOCCH, + :I: Slower CH
Solvente
In questa parte vedremo che la forza di un nucleofilo dipende anche dal solvente nel quale avviene la reazione, cioè una stessa specie nucleofila può avere forza diversa in solventi diversi. I solventi possono essere distinti in apolari e polari. Quelli polari a Polar aprotic solvents loro volta si possono distinguere Polar Protic Solvents in solventi polari protici e solventi polari aprotici. I solventi polari aprotici sono solventi polari che non hanno la possibilità di mettere a disposizione protoni per formare legami a idrogeno con la specie chimica in essi disciolta. Non possiedono quindi legami N-H, O-H o F-H N H H3C-CEN: Acetonitrile (MeCN) H-O-CH2CH3 Ethanol H-Ö-CH3 Methanol N-H o F-H. Le due tabelle a fianco riportano un elenco dei più comuni solventi protici e aprotici Acetone : NH3 Ammonia CH3 N,N-Dimethylformamide (DMF) H-O-C-CH3 CH3 t-Butanol H-Ö-CH2CH2CH3 n-Propanol I solventi polari protici sono solventi polari in grado di mettere a disposizione protoni per formare legami a idrogeno con la specie chimica in essi disciolta. Devono dunque possedere legami O-H, Dimethyl sulfoxide (DMSO) H-O-C-CH3 Acetic acid H-O-H WaterI solventi protici, a causa della loro capacità di formare legami a idrogeno, sono in grado di solvatare gli ioni presenti in soluzione molto efficacemente, meglio dei solventi aprotici e decisamente meglio dei solventi apolari Cosa significa solvatare? Gli ioni che si liberano dalla dissociazione o ionizzazione di una sostanza, vengono circondati dalle molecole di solvente e possono formare con esse legami intermolecolari anche molto forti; si possono così creare degli ioni solvatati, costituiti dallo ione e dalle molecole che gli stanno intorno, abbastanza stabili da muoversi come un unico aggregato nella soluzione. 8 La figura a lato e quella sottostante mostrano in modo chiaro la differenza di solvatazione che sono in grado di generare solventi protici e aprotici. Immaginiamo di sciogliere in acqua, un solvente protico, la sostanza NaBr. Entrambi gli ioni formatisi vengono ben solvatati dall'acqua attraverso forti legami ione-dipolo e ione-idrogeno. 8+ Br" 8+ Na+ is solvated by ion-dipole interactions with H2O. Br- is solvated by hydrogen bonding with H2O. Se la stessa sostanza viene sciolta in acetone, solvente aprotico, vediamo che lo ione positivo viene ben solvatato attraverso forti legami ione-dipolo, mentre lo ione bromuro non è così ben solvatato perché i legami che si generano sono di tipo ione-dipolo, più deboli. Ovviamente un solvente apolare produrrebbe una solvatazione decisamente inferiore, quasi nulla. 8 8 Na+ 8 18 (CH3)2C=O solvates Na+ well by ion-dipole interactions. Br Br- Br Br Branions are surrounded by solvent but not well solvated by the (CH3)2C=O molecules. Ora, lo ione bromuro è una specie nucleofila; appare chiaro dalle figure che in presenza di un solvente protico lo ione è ben stabilizzato e completamente circondato, quasi intrappolato, dalle molecole del solvente; di conseguenza la sua capacità di fornire una coppia di elettroni ad una specie elettrofila risulterà ridotta. Nel caso di un solvente aprotico invece lo ione negativo è meno stabile è più libero quindi potrà mettere più facilmente a disposizione la coppia di elettroni. Se lo ione negativo si trova infine in un solvente apolare sarà poco stabilizzato, quindi più reattivo e il suo potere nucleofilo risulterà enfatizzato, il problema in questo caso è che lo ione non si solubilizzi affatto. Possiamo concludere quindi che lo ione bromuro e tutte le specie nucleofile ioniche in genere, hanno maggiore forza nucleofila in solventi apolari e tra i polari hanno maggiore forza nucleofila in solventi polari aprotici che in solventi polari protici 8 Na+
Buoni e cattivi gruppi uscenti
Il gruppo uscente, in una reazione di sostituzione nucleofila è il nucleofilo che lascia il substrato. (vedi figura a fianco) Maggiore è la tendenza ad abbandonare il substrato del gruppo uscente, più probabile è che avvenga la reazione di sostituzione nucleofila. R-L Nu-R + L: L = leaving group Nu = nucleophile Dato che il gruppo uscente, al termine della reazione è solo, non è legato con altre specie chimiche, il criterio per valutare la qualità del gruppo uscente è semplicemente la sua stabilità: più è stabile, più facilmente esce dal substrato. Essendo una specie carica negativamente, il gruppo uscente è una base e le basi sono tanto più stabili quanto più sono deboli (infatti non tendono a protonarsi), quindi i gruppi uscenti migliori sono basi deboli. La tabella a fianco classifica i gruppi uscenti in funzione del pKa del loro acido coniugato. Le basi coniugate degli acidi più forti sono i migliori gruppi uscenti. L'unica eccezione è lo ione F- che come segnalato nella figura è un gruppo uscente peggiore di quanto prevedibile dalla sua basicità, ma ciò è dovuto alla particolare forza del legame sigma che forma con gli atomi di carbonio. In alcuni casi si può migliorare la qualità del gruppo uscente agendo con catalizzatori; ad esempio lo ione OH- è un pessimo gruppo uscente, infatti è una base forte, quindi è difficile effettuare una sostituzione nucleofila su un alcol. Uno stratagemma è quello di protonare il gruppo alcolico in ambiente acido in modo che diventi OH2+. In questo modo il gruppo uscente diventa l'acqua che è un migliore gruppo uscente dello ione OH-
Tabella pKa per gruppi uscenti
A pKa table is a handy guide to leaving groups Functional group / Example pKa Conjugate base Hydroiodic acid HI -10 0 Hydrobromic acid HBr -9 Br Hydrochloric acid HCI -8 CI 0 Sulfuric acid H2SO4 -3 HSOA O= Os Sulfonic acids 1 OH -3 Me Me (tosic acid) Hydronium ion H3O -1.7 H2O Hydrofluoric acid H-F 3.2 F Exception: FO is typically a poor leaving group (forms strong bonds) O Carboxylic acids H3C OH H3C Moderate leaving groups (weak bases) Protonated amines + NHÀ CI 9-11 NH3 Water HO-H 16 HOO 1 Poor leaving groups (atrong bases) Alcohols CH3O-H 16-18 Amine NH3 ~35 NH Hydrogen H-H 42 HO Extremely poor leaving groups (very strong bases) Alkane HO .CH3 ~50 H3C CH2O Excellent leaving groups (extremely weak bases) 0 Sin + 0 4 0 0 ℮ Nu: CH:00