Technology Transfer nell'industria farmaceutica: evoluzione e requisiti
Documento universitario sul Technology Transfer nell'industria farmaceutica. Il Pdf esplora l'evoluzione storica, i requisiti regolatori e i fattori chiave di successo e fallimento, con un case study pratico. Utile per lo studio autonomo, presenta schemi e diagrammi per facilitare la comprensione dei concetti.
Mostra di più12 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Evoluzione dell'Industria Farmaceutica
L'industria farmaceutica è cambiata notevolmente negli ultimi anni. Inizialmente, negli anni 80, tutti i servizi si trovavano all'interno della stessa azienda: lavanderie, asilo nido e così via. In questi ultimi anni, invece, sono stati introdotti più requisiti regolatori, pressioni governative per abbassare i prezzi, la competizione da parte dei generici, i costi di sviluppo in aumento, la crescita dell'industria farmaceutica nei mercati emergenti come l'India e la Cina e soprattutto le attività di outsourcing.
Passato e Presente nel Settore Farmaceutico
Passato Presente 1970 1980 1990 2000 2010 2020 Fully integrated Larger but fewer FIPCOs • Even larger and even Pharmaceutical • Specialized Drug Discovery fewer FIPCOs Companies (FIPCOs) Companies • Specialized Drug Discovery • Specialized Drug Delivery Companies Companies Specialized Drug Delivery Contract Research • Companies Organizations (CROs) • CROS, CMOs, Generic Companies • Virtual Companies
Infatti, il mercato globale è in continuo cambiamento e, di conseguenza, le Ditte Farmaceutiche devono rivalutare costantemente le loro funzioni ed operazioni in merito a:
- Globalizzazione
Fusioni e acquisizioni ® -> Creazione di "centri di eccellenza" e siti produttivi di "prima classe" Riallocazione degli impianti produttivi in aree che offrono vantaggi di tasse ® -> Aumento dell'outsourcing
Il Technology Transfer nei Processi Farmaceutici
Le aziende più grosse hanno quindi sviluppato dei modelli di Technology Transfer: i Technology Transfer sono diventati una parte integrante dei processi farmaceutici, sempre più importanti, sempre più internazionali e sempre più complessi, coinvolgendo siti differenti, culture differenti, procedure differenti, apparecchiature e tecnologie produttive differenti, e così via. Le ditte tendono ad accelerare i loro processi, ed è quindi critico lo sviluppo ed il trasferimento di formulazioni e processi robusti. Molte industrie farmaceutiche hanno sviluppato dei propri modelli di Technology Transfer.
Definizione e Tipi di TT
Il Technology Transfer può essere definito come il trasferimento della conoscenza, dell'esperienza e della tecnologia relative ad un processo e ai controlli ad esso correlati, da un sito "Donatore" ad uno "Ricevente": il Technology Transfer è una esperienza di insegnamento e apprendimento per entrambe le parti.
Il TT può essere di due tipi:
- TT primario: da R&D a produzione in house o conto terzi.
- TT secondario: da un sito ad un altro sito.
Fasi del Technology Transfer
Le principali fasi del TT cominciano con l'identificazione della formulazione che andrà trasferita; i materiali di confezionamento primario non necessariamente devono subito essere identificati, perché magari saranno scelti in funzione della preferenza del sito produttivo, per quanto debbano comunque essere simili a quelli originari. Inoltre, è meglio interagire subito appena possibile con il sito di produzione finale, perché in questo modo si evitano problemi con il trasferimento: di solito si fa un kick off, ovvero una riunione con il sito produttivo. Devono essere poi prodotti dei lotti dimostrativi e dei lotti per la stabilità regolatoria, sui quali i dati devono essere inseriti nel dossier. I lotti per la stabilità regolatoria non devono necessariamente essere in scala commerciale (la scala è indicata nella linea guida ICH sulla stabilità), mentre quando si passa alla convalida devono essere prodotti lotti sulla scala commerciale finale.
122
-
•Formulazione Finale
-
Decisione di Sourcing, Conferenza del Technology Transfer + Piano Tech Transfer
-
Lotti di prova al Sito Finale (Lotti "Dimostrativi")
-
Completamento del Tech Transfer
-
Convalida (scala finale)
-
Lotti per stabilità regolatoria (Pronti per la PAI)
La Piramide del TT
La piramide del TT, mostrata in figura, ha senso perché il TT deve sicuramente essere in primis economicamente fattibile: se non si ha un ritorno economico finale, non ha alcun senso fare un TT. Sia gli investimenti sia i tempi impattano sul ritorno economico. Poi, si deve garantire la compliance ai requisiti regolatori: anche il TT deve rispettare i requisiti regolatori. Infine, il TT deve essere tecnicamente valido.
Il TT di un processo produttivo o di un metodo analitico è un processo ispezionabile, che deve avvenire in un ambito regolamentato.
Economicamente fattibile
"Compliance" con i requisiti regolatori
P. Thompson, Tech Transfer, London, 2002
Tecnicamente valido
Occorre stabilire una relazione efficace per ogni livello prima di iniziare il processo
Linee Guida e Regolamentazioni del TT
Al momento non esistono delle linee guida formali FDA, ICH o EMA che ricomprendano nell'insieme tutto il TT: sono disponibili delle linee guida tecniche (technical guidance) della WHO e della PDA, che contengono elementi del QbD e del QRM, che si trovano nelle ICH Q8, Q9 e Q10, e una linea guida ISPE, anch'essa contenente elementi del QbD e del QRM. Anche se non esistono linee guida specifiche, di fatto il metodo deve essere convalidato nel sito ricevente. Le raccomandazioni regolatorie che si applicano durante lo sviluppo o dopo l'approvazione di un prodotto si applicano appropriatamente anche al processo di TT.
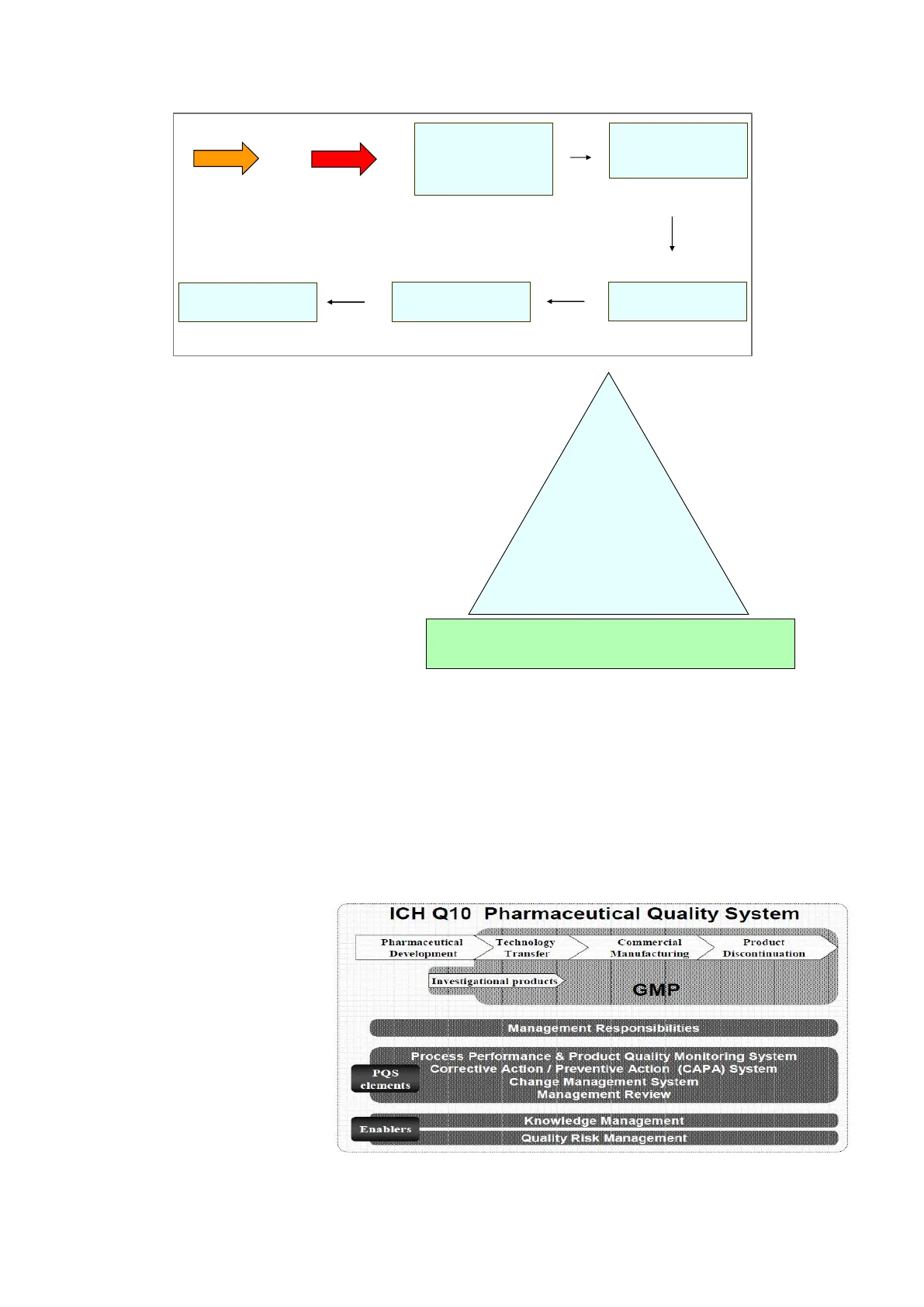
Ruolo del TT nella ICH Q10
La ICH Q10 richiama il ruolo chiave del TT per il suo porsi tra lo Sviluppo Farmaceutico (dove si crea la conoscenza) o tra il Sito Donor (che già produce in una situazione di controllo) e, passando attraverso la convalida di processo, la produzione per il mercato presso il Sito Ricevente (che deve realizzarsi in una situazione di controllo). In questa linea guida, il TT viene citato all'interno del PQS (Pharmaceutical Quality System). Il PQS copre ICH Q10 Pharmaceutical Quality System l'intero lifecycle di un prodotto, includendo lo sviluppo Pharmaceutical Product Discontinuation Development Technology Transfer Commercial Manufacturing farmaceutico, il technology transfer, la produzione GMP Investigational products commerciale e la sospensione del prodotto. Il PQS incrementa le GMP regionali Management Responsibilities come mostrato nel diagramma, che Process Performance & Product Quality Monitoring System Change Management System Management Review Corrective Action / Preventive Action (CAPA) System mostra anche che le GMP POS elements regionali si applicano alla produzione degli IMPs.
Knowledge Management Enablers Quality Risk Management
Strategie di Controllo nella Produzione Farmaceutica
Lo schema sottostante, invece, mostra una panoramica delle strategie di controllo di tutte le fasi di produzione, sempre sotto il PQS:
-
• ‒Pharmaceutical Development Create Knowledge
-
Technology Transfer Prepare to Execute
-
Manufacturing Execute
Product and Process Knowledge Understand CQAs and CPPs to enable a Control Strategy to be developed
Provide sufficient details of Controls to enable technology transfer
Execute in a State of Control with Efficient Operations & Continuous Improvement
-Drug Substance -Scale-Up Patient Business -Formulation -Initial Validation (PQ) Continuous -Clinical Supplies Patient Business 2 -Drug Delivery -Analytical Methods 2 Verify -Packaging -Etc. Patient Business Development 3 Pharmaceutical Quality System
Quando si trasferisce un processo, le autorità regolatorie richiedono:
- Un alto grado di conoscenza del prodotto, del processo e dei relativi controlli, tramite l'identificazione delle variabili critiche e dei possibili effetti sul prodotto finito, gli intermedi e i diversi passaggi del processo.
- L'equivalenza tra le caratteristiche chimico-fisiche e biofarmaceutiche dei lotti di sviluppo (clinici, stabilità primaria) e dei lotti prodotti al sito finale.
- L'accesso a tutti i dati e le informazioni relativi allo sviluppo e al Technology Transfer: Report di Sviluppo del Prodotto, ovvero dati scientifici che giustificano la formulazione, il processo e i controlli di processo, e Protocolli e report relativi al Technology Transfer.
Trasferimenti di Siti Produttivi Post-Approvazione negli USA
Parlando di trasferimenti di siti produttivi dopo l'approvazione negli USA, esiste una linea guida della FDA del 2004 che indica quali sono le categorie con le quali è possibile introdurre un cambio e comunicarlo alla FDA. Se il cambiamento è meno importante e ha un rischio minore sulla qualità, sicurezza e efficacia del prodotto, è possibile produrre il prodotto e poi introdurre un annual report: non è necessario aspettare un'approvazione dell'autorità regolatoria. Questa linea guida individua categorie di reporting: nel caso della categoria CBE-0, si hanno 0 giorni di attesa per l'autorizzazione, nel caso della categoria CBE-30 30 giorni e nel caso della categoria PA, è necessario aspettare l'approvazione dell'autorità regolatoria. Non ci sono indicazioni su informazioni specifiche da sviluppare per valutare l'effetto del cambio.
La linea guida del 2014 è più dettagliata e dice quali sono i cambiamenti che possono essere fatti dal punto di vista chimico e tecnologico che possono essere documentati negli annual reports. Questo è utile per cercare di snellire la comunicazione con l'ente regolatorio.
Linee Guida SUPAC della FDA
Le SUPAC (Scale-up and Post Approval Changes) sono linee guida per l'industria redatte dal CDER della FDA nel 1995 e nel 1997. Esse comprendono:
- SUPAC-IR: compresse a rilascio immediato, compresse masticabili, capsule di gelatina dura e molle.
- SUPAC-MR: forme solide orali a rilascio modificato.
- SUPAC-SS: preparazioni semi-solide non sterili ad uso topico (creme, gel, lozioni, unguenti).
- SUPAC: Manufacturing Equipment Addendum (2014).
Lo scopo di queste linee guida è ridurre il carico regolatorio per industria e FDA in seguito a variazioni dopo l'approvazione di un prodotto, continuando a garantirne sicurezza, efficacia e qualità. Le categorie di reporting raccomandate nella linea guida "Changes to an Approved NDA or ANDA" sostituiscono quelle SUPAC, quando inconsistenti. Le definizioni di manufacturing site nella linea guida "Changes to an Approved NDA or ANDA" sostituiscono quelle SUPAC, quando inconsistenti.
Le linee guida SUPAC definiscono:
- Livelli di cambio 124 Improvement-> Test CMC raccomandati per ogni livello di cambio
- Test di dissoluzione in vitro o studi di bioequivalenza in vivo
- Documentazione a supporto del cambio
- Livelli di reporting
- La documentazione da generare e presentare alla FDA a supporto di uno dei seguenti cambi per un prodotto già registrato: § Componenti o composizioni § Sito di produzione § Scala di produzione § Produzione (processo e apparecchiature)
Trasferimento di Sito Post-Approvazione nell'Unione Europea
Invece, per quanto riguarda il trasferimento di sito dopo approvazione del prodotto in Unione Europea, la prima linea guida è stata del 2008 e riguardava l'esame delle variazioni ai termini dell'AIC per prodotti medicinali per uso umano e veterinario. Questo regolamento è entrato in vigore nel 2010 ed è stato modificato con il regolamento 712/2012. Nel 2013 infine è uscita una linea guida riguardo i dettagli delle varie categorie di modifica dei termini dell'AIC per prodotti medicinali ad uso umano e veterinario.
Variazione Numero B.II.b.1 REPLACEMENT OR ADDITION OF A MANUFACTURING SITE FOR PART OR ALL OF THE MANUFACTURING PROCESS OF THE FINISHED PRODUCT
- Secondary packaging site - Procedura Tipo IAIN
- Primary packaging site - Procedura Tipo IAIN
- Site where any manufacturing operation(s) take place, except batch release, batch control and secondary packaging, for biological/immunological medicinal products - Procedura Tipo II
- Site which requires an initial or product specific inspection - Procedura Tipo II
- Site where any manufacturing operation(s) take place, except batch release, batch control, primary and secondary packaging, for non-sterile medicinal products - Procedura Tipo IB
- Site where any manufacturing operation(s) take place, except batch release, batch control, and secondary packaging for sterile medicinal products manufactured using an aseptic method excluding biological/immunological medicinal products - Procedura Tipo IB
Types of variations Changes not requiring Any prior approval
Changes requiring prior approval
Design Space
Type IA Type IB Type II Extension Do and Tell Variations
Evaluation Procedure adapted to the level of risk
Criteri Tecnici e Fattori di Complessità del TT
I criteri tecnici per stabilire la robustezza derivano da questi quesiti:
- Quanto simili sono le apparecchiature? (Fasi I, II, scale-up, sito finale)
- Fonte delle materie prime (Sito Donor versus Sito Ricevente): la fonte è la stessa
- I metodi analitici funzionano bene o sono operatore-dipendenti?
- I componenti del confezionamento primario sono stati ben specificati?
- Il prodotto finito è sufficientemente caratterizzato da poter capire quando il processo non funziona bene?
I criteri tecnici per stabilire i fattori di complessità sono:
- Forma farmaceutica: tipo e formulazione.
- Processo di produzione: livello del cambio di scala e tipo e principio operativo di apparecchiature e impianti.
- Caratteristiche dei Siti Donatore e Ricevente: flussi di lavoro, esperienza del personale, sistema di qualità.
- Intra- vs Extra-aziendale.
- Pre- vs Post-registrativo.
Scale-up e Fattori di Scala
Lo scale-up prevede diverse entità dei lotti:
- Scala di laboratorio: 0.2-2 Kg, pari a 100-1000 volte meno della scala di produzione. ® Scala intermedia: 5-30 Kg. ® Scala pilota: 30-100 Kg, pari al 10% della scala di produzione o a 100000 unità.
- Scala commerciale: 300-1000 Kg, nello stabilimento di produzione.
I fattori di scala riguardano l'incapacità di prevedere i problemi nel passaggio dallo Sviluppo alla Produzione. Il "commento preferito" del personale di Sviluppo in presenza di problemi in Produzione è normalmente "Non abbiamo mai avuto problemi di processo durante le prove di formulazione e di scale- up!". Nell'analisi delle cause spesso risulta invece che la formulazione è inappropriata per il processo di 125