Geochimica degli isotopi dei gas nobili: focus sull'elio e applicazioni
Slide da Uni-Milano Bicocca sulla Geochimica degli isotopi dei gas nobili (prima parte). Il Pdf, utile per studenti universitari di Scienze, esplora le proprietà dei gas nobili e l'uso degli isotopi dell'elio come traccianti nei processi del mantello, con grafici esplicativi.
Mostra di più12 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Geochimica degli isotopi dei gas nobili
LEZIONE N.26B Geochimica degli isotopi dei gas nobili (prima parte) Corso di GEOCHIMICA (8 CFU) Scienze e Tecnologie Geologiche (Uni-Milano Bicocca, DISAT) AA 2024-2025 - II semestre Prof. Andrea L. Rizzo: andrealuca.rizzo@unimib.itProprietà dei gas nobili
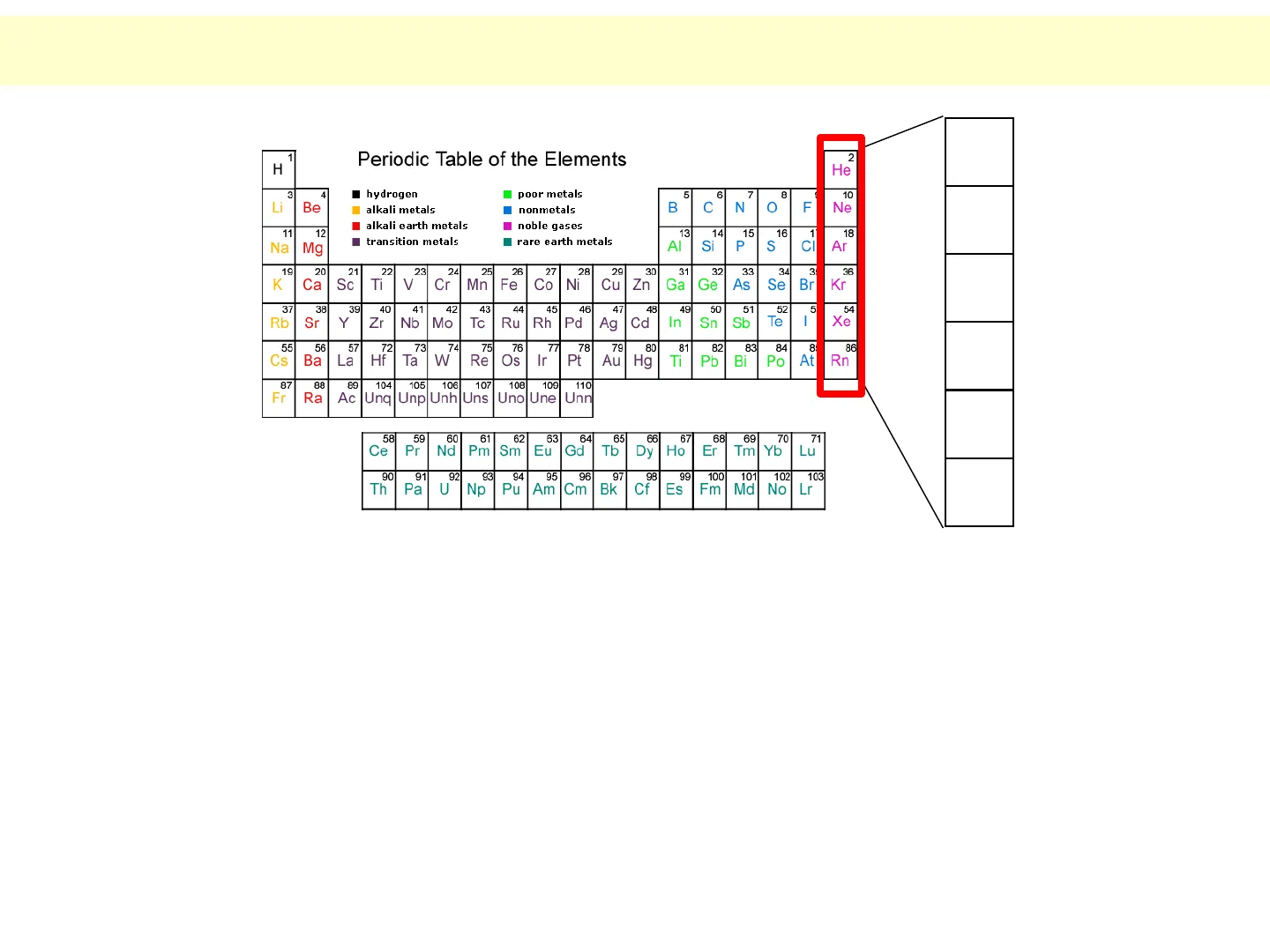
2 H He 3 4 hydrogen I poor metals 5 6 7 8 Li Be alkali metals nonmetals B C N O F 10 Ne 10 Ne 11 Na 12 Mg transition metals rare earth metals AI 14 Si 15 P S 1 CI Ar 19 21 22 23 24 25 26 Fe 27 Co 28 29 30 31 32 33 As 34 Se Br Kr Ar 37 Rb 38 39 40 42 43 44 Ru 45 Rh Pd 47 Ag 48 Cd 49 In 50 Sn 51 Sb Te I Xe 55 Cs 56 Ba 57 La 72 Hf 73 74 75 Re 76 Os Ir 78 Pt 79 Au 80 Hg 81 Ti 82 Pb 83 Bi 84 Po 8 At 86 Rn 87 Fr 88 Ra 89 Ac 104 Ung 105 Unp 106 Unh 107 Uns 108 Uno 109 Une 110 Unn 54 Xe 58 Ce 59 Pr 60 Nd 61 Pm 62 Sm 63 Eu 64 65 Tb 66 Dy 67 Ho 68 Er 69 Tm 70 Yb Lu 90 Th 91 Pa 92 U 93 Np 94 Pu 95 Am 96 Cm 97 Bk Cf 99 Es 100 Fm 101 Md 102 No Lr Rn 3 36 K 20 Ca Sc Ti V Cr Mn Ni Cu Zn Ga Ge 52 5 54 Sr Y Zr 41 Nb Mo Tc 36 Kr 71 86 103 1 Periodic Table of the Elements 2 He alkali earth metals noble gases 13 16 18 18 46 77 Gd 98 Ta W
Proprietà dei gas nobili
- I gas nobili, noti anche come gas inerti o gas rari, si trovano nel gruppo VIII della tavola periodica.
- Gli elementi hanno una configurazione elettronica con un ottetto completo.
- Sono gli elementi più piccoli nei rispettivi periodi, con le più alte energie di ionizzazione. La loro configurazione elettronica a guscio chiuso fa sì che abbiano una reattività e un'inerzia chimica molto basse.
- I gas nobili hanno punti di fusione e di ebollizione molto bassi
- In natura i gas nobili si presentano sotto forma di singoli atomi e non formano composti
- Bassa solubilità nei fusi silicatici (saturazione già nel mantello), paragonabile o addirittura inferiore a quella della CO2
- Si comportano come elementi incompatibili durante la fusione e la differenziazione del mantello
- Gli isotopi dello stesso elemento non si frazionano durante la partizione (cioè cristallo/fusione, fusione/gas, gas/acqua)
- Tra i gas nobili, l'elio, il neon e l'argon sono più comunemente usati nelle applicazioni alle geoscienze.
Storia dei gas nobili
1868: L'elio è stato identificato per la prima volta come un elemento semplicemente dal suo spettro di assorbimento nella cromosfera solare da Lockyer. 1895: Rayleigh ha identificato la presenza di un gas sconosciuto di bassa densità nell'atmosfera (poi rivelato essere argon). 1898 Questa osservazione ha portato a esperimenti di distillazione più raffinati da parte di Ramsey, che ha identificato Ar e ha portato anche all'isolamento di Kr, Ne e Xe (per i quali Ramsey e Rayleigh avrebbero ricevuto premi nobili). 1905 La scoperta che una particella alfa prodotta dal decadimento di U era in realtà un nucleo di elio permise a Rutherford e Strutt di effettuare le prime misurazioni radiometriche dell'età. Ciò ha portato a suggerire che l'età della Terra fosse essere maggiore di 400 Ma, invece di 20 Ma come si pensava fino ad allora. 1913 La prima separazione isotopica utilizzando il primo spettrometro di massa è stata effettuata da Thomson e Aston per separare 20Ne da 22Ne. Questo sviluppo ha aperto le porte alla ricerca sugli isotopi dei gas nobili. 1939 3He è stato identificato per la prima volta in spettrometria di massa presso i Lawrence Berkely Labs (CA) 1942 Il progresso nella spettrometria di massa ha portato a nuove opportunità di ricerca in geo e cosmochimica
Carta dei nuclidi dei gas nobili
6Li + n > a +3H; 3HS; 3He ß - 6Li 7Li (a) 3He 1.7×10-4 4He =1 20 Ne 13.6 21Ne 0.033 22Ne =1 36 Ar 5.6 37 Ar 35 d 38 Ar 39 Ar 269 yr 40 Ar Element 1H 2H 3H 12.3 yr 19F 35℃1 36C1 301 ka 37Cl Unstable isotopes (d) .78Kr 0.00637 80 Kr 0.0409 81 Kr 229 ka 82Kr 0.2048 83Kr 0.2029 Kr =1 86Kr 0.3024 Atomic weight A (=Z+N) 79Br 81Br Solar isotope ratios 133 Cs (e) 124 Xe 0.0294 126Xe 0.0255 128 Xe 0.510 129Xe 6.27 130xe =1 131Xe 4.98 132Xe 6.02 134 Xe 2.207 136xe 1.797 127] 1291 16 Ma Neutron number (N) = 39K 40K (1.28 Ga) 41 K (b) 22Na 2.6 yr 23Na (c) =1 < 0.02 85Rb 87Rb Proton number (Z)
Gas nobili in atmosfera
N2 = 78.084 %, O2 = 20.948%, CO2 ~ 0.0400% He Ne Atmosphere Ar, Kr, Xe Highly degassed upper mantle Little degassed lower mantle L'atmosfera attuale è il risultato dell'evoluzione temporale dalla formazione della Terra ad oggi. I gas nobili vengono degassati dal mantello e in parte sfuggono dall'atmosfera, creando uno stato stazionario di breve durata Source: Ozima and Podosek (2002); Brennwald et al. (2013), The Noble Gases as Geochemical Tracers, Springer
Composizione dei gas nobili in atmosfera
N2 = 78.084 %, O2 = 20.948%, CO2 ~ 0.0400% Element Vi di (Å) Isotope Ri (%) He (5.24 ± 0.05)· 10-6 2.55 3He 0.000140 4 He ~100 Ne (1.818 ± 0.004) . 10-5 2.82 20Ne 90.50 21 Ne 0.268 22 Ne 9.23 Ar (9.34 ± 0.01)·10-3 3.45 36 Ar 0.3364 38 Ar 0.0632 40 Ar 99.60 Kr (1.14 ± 0.01)·10-6 3.65 78 Kr 0.347 80 Kr 2.257 82 Kr 11.52 83 Kr 11.48 84 Kr 57.00 86 Kr 17.40 Xe (8.7 ± 0.1)· 10-8 4.04 124 Xe 0.0951 126Xe 0.0887 128 Xe 1.919 129 Xe 26.44 130Xe 4.070 131 Xe 21.22 132Xe 26.89 134 Xe 10.430 136 Xe 8.857
Ripartizione dei gas nobili: liquido e vapore
Ripartizione tra liquido (acqua come solvente) e vapore, regolata dalla costante di solubilità della legge di Henry: Si=C/P 200 \ Xe -He Ne Ar -1) 150 1 - Kr 1 - - Xe -1 . O2 100 Kr N2 0 5 10 15 20 25 30 0 10 20 30 40 T (C) S (g/kg) L 1 50 Ar , O2 4.3×10-5 2300 Abraham and Matteoli (1988) L 9.1×10-5 2900 Abraham and Matteoli (1988) L 9.2×10-5 2600 Wilhelm et al. (1977) L 3.3×10-4 2400 Sander et al. (2011) L 3.3×10-4 2400 Sander et al. (2006) L 1.4×10-5 1900 Warneck and Williams (2012) L Temperature (C) 1.4×10-5 1600 Sander et al. (2011) L 100% 80% * c;/c, 60% He Ne Ar Kr T Xe N2 Ne , He 0 10 20 30 T.TAIV 1 WWWWEZ-Tillm Ul ti. (4vvJ) Bunsen (ml Kg 1 atm . 40%
Geochimica degli isotopi dell'elio
- Due isotopi: 3He e 4He
- 3He è primordiale, non rinnovato e immagazzinato all'interno della Terra
- 4He è radiogenico e prodotto continuamente dal decadimento radioattivo di U e Th He 3He, 4He
- Gli isotopi dell'elio sono riportati come 3He/4He, espresso come R/Ra, dove R è il rapporto isotopico del campione mentre Ra è il rapporto in atmosfera (Ra=1,39×10-6).
- L'elio non è riciclato nel mantello durante la subduzione (viene deidratato dallo slab nelle prime centinaia di km), quindi elevati 3He/4He implicano la presenza di materiale poco degassato dal mantello inferirore
- È sensibile alla miscelazione tra diversi serbatoi, fornendo informazioni sulla composizione e la storia della Terra
3He/4He dei serbatoi geochimici
Solar (Primordial) 3He/4He > 120 RA + Radiogenic (from U, Th) 3He/4He ~ 0.01 RA Mid Ocean Ridge Basalts (MORB) 8 RA Hotspot 5~50 RA Atmosphere 3He/4He = 1 RA (1.4x10-6) 10-3 Solar Solar Wind Meteorites Planetary 100 10-4 Crust ~0.01 RA Upwelling "Plume" MORB source 8 RA Mantle Plume source ≥ 50 RA Lower mantle or core-mantle boundary ? 10- 100000 Cosmogenic 10-2 1000 3He/4He OIB 10-5 MORB Arcs Atmosphere 1 10-6 - 0.1 10-7 Crustal Rocks 0.01 10-8 Element Stable isotopes 10000 R/RA 10
Geochimica degli isotopi dell'elio in ambienti marini
- In studi in ambienti marini e paleoclimatici, l'elio è spesso ripotato come anomalia di 3He 83He = 100 -1) RA Rx 0 10 1000 20 2000 30 Depth (m) 3000 20 4000 5000 P4 (10 N) 6000 140 160 180 200 220 240 260 0 40.0 1000 27.5 Depth (m) 2000 130 22.5 3000 17.5 4000 12.5 5000 P21 (18 S) 160 180 200 220 240 260 280 0 -2.5 25 1000 10 2000 Depth (m) 3000 4000 5000 6000 P6 (32 S) 160 180 200 220 240 260 280 Longitude Distribuzione dell'eccesso di 3He nell'acqua di mare sopra l'Oceano Pacifico in prossimità di pennacchi idrotermali dal fondo marino. 700 600 500 400 300 200 Depth (m) 100 0 Age (y) 5 40 10 15 35 20 25 : 20 35 G 35 25 i 30 25. 20 15 15 10 10 5 5 0 Distribuzione dell'età dell'acqua sulla base di trizio-3He nell'Oceano Pacifico (1980-1990) Il Sistema 3H/3He è molto utile per datare l'acqua che è stata in contatto con l'atmosfera negli ultimi 50 anni t = 2 3He* 1 3H + 1 3H=12.31 anni t-dimezzamento 8(3He)% 32.5 30 20 7.5 2.5 20
Isotopi dell'elio come traccianti nei processi di mantello
Evoluzione temporale di 3He/4He
OIB CUMULATES 4 magmas Degassing Time (Ga) 3 He Primordial mantle 1 10 30 3He/4He (R/R2) Evoluzione temporale di 3He/4He dalla formazione della Terra ad oggi
Variabilità di 3He/4He nei vulcanismi
OIB 7.9 CUMULATES MORB depth > 3.5 km (n = 82) a 4 gmas Degassing Reunion (n = 76) He Iceland (n = 416) 3 Primordial mantle Hawaii (n = 472) 2 MORB Galapagos (n = 61) 1 10 30 100 120 3He/4He (R/Ra) Variabilità di 3He/4He nei vulcanismi di tipo MORB e OIB 2 MORB Probability density Time (Ga)
Isotopi dell'elio come traccianti nei processi di mantello: nomenclatura
Mantle domains nomenclature Plate boundary MORB (DMM)=Mid-Ocean Ridge Basalt Atlantic, Pacific, and Indian oceans Within plate OIB = Ocean Island Basalt HIMU = high 238U/204Pb (high u) EM1 = Enriched mantle 1 EM2 = Enriched mantle 2 10-1 Cosmogenic 10000 10-2 10-3 Solar Solar Wind Meteorites Planetary 100 10-4 R/RA OIB 10-5 MORB Arcs 1 10-6 - Atmosphere 206 Pb/204 Pb 15.3 17 18 19 20 21 22 23 (b) 10-8 Crustal Rocks 0.01 10 Iblean Ustica Linosa Etna Pantelleria® HIMU 6 Vulture R/Ra -Panarea Ischia-Procida Salina 4 Stromboli Vulcano Lipari Roccamonfina Phlegrean Fields Vesuvius 2 Albani Vulsini Crust 0 - 17 18 19 20 21 22 3He/4He 10 0.1 10-7 206ph / 204ph 8 DM - Alicudi Filicudi 100000 1000
Geochimica degli isotopi dei gas nobili (seconda parte)
LEZIONE N.27 Geochimica degli isotopi dei gas nobili (seconda parte) Prossime lezioni 04/06/2025 ore 08:30-10:30 - U9-15