L'acqua: proprietà, legami a idrogeno e scala del pH
Documento dall'Università sull'acqua, le sue proprietà e il pH. Il Pdf esplora la struttura molecolare dell'acqua, i legami a idrogeno, le interazioni deboli e la ionizzazione, argomenti fondamentali per la Chimica a livello universitario.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
L'acqua e le sue proprietà
l'acqua è la sostanza più abbondante in tutti gli esseri viventi e rappresenta più del 70% del peso della maggior parte degli organismi la dimensione della molecola d'acqua è circa un millesimo dello spessore di un capello umano 0,1 mm contro 0,1nm=1Å i primi organismi comparvero senza dubbio negli oceani primordiali e la loro evoluzione fu influenzata dalle proprietà del mezzo acquoso le forze di attrazione tra le molecole d'acqua e la sua scarsa tendenza a ionizzarsi sono caratteristiche fondamentali per la struttura e funzione delle biomolecole le molecole d'acqua e i loro prodotti di ionizzazione influenzano profondamente la struttura, il modo di combinarsi insieme e le proprietà di tutti i componenti cellulari: proteine, acidi nucleici e lipidi le interazioni responsabili del riconoscimento tra le biomolecole sono influenzate in modo determinante dalla proprietà dell'acqua come solvente quale la sua capacità di formare LEGAMI A IDROGENO con se stessa e con i suoi soluti proprietà particolari che permettono che diventi il solvente adatto per la vita
Interazioni deboli nei sistemi acquosi
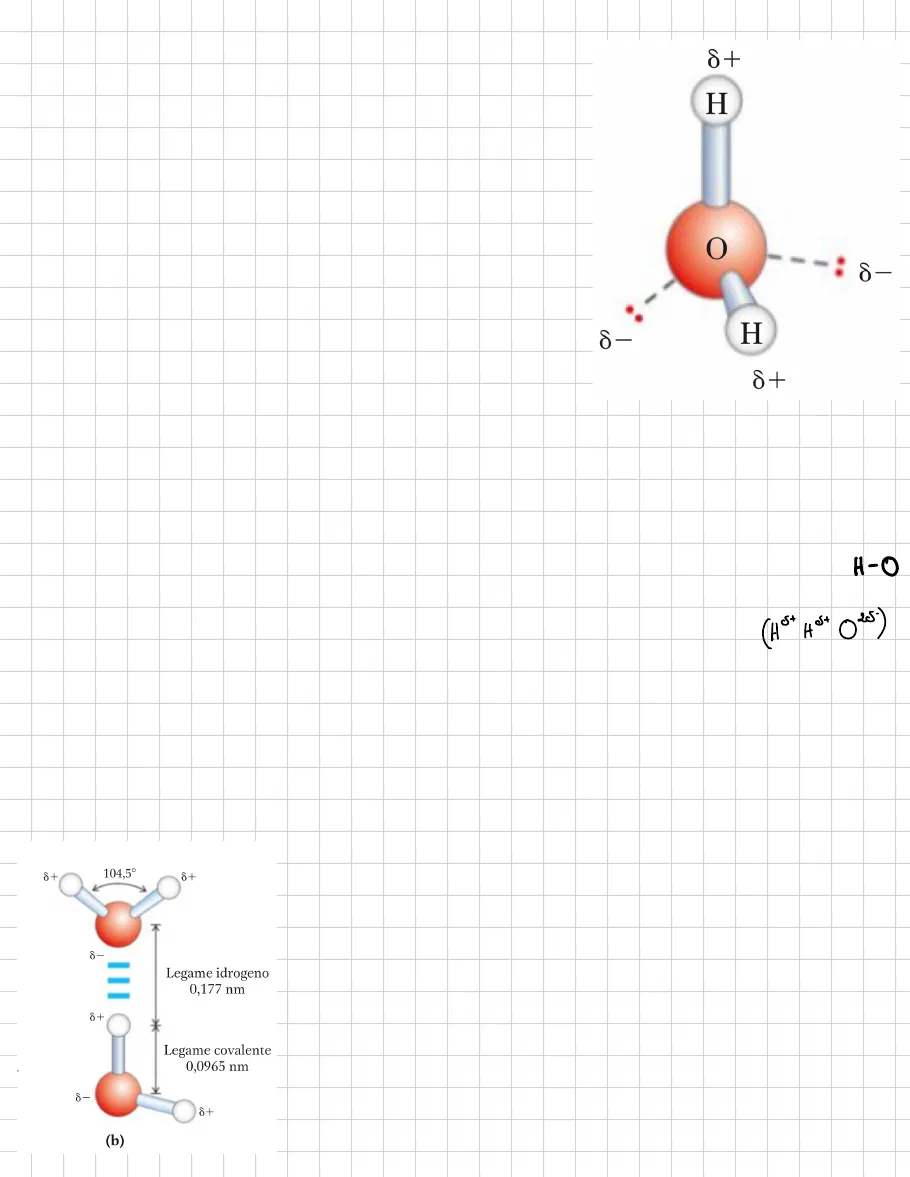
i legami a idrogeno tra le molecole di acqua rappresentano la forza di coesione che rende l'acqua un liquido a temperatura ambiente è un cristallo a basse temperatura con disposizione delle molecole ordinata le biomolecole polari si dissolvono facilmente nell'acqua in quanto possono sostituire le interazioni favorevoli acqua-acqua con altre interazioni ancora più favorevoli acqua-soluto al contrario le molecole non polari sono scarsamente solubili in acqua poiché interferiscono con le interazioni favorevoli acqua-acqua ma non sono in grado di formare interazioni acqua soluto i legami a idrogeno e ionici, le interazioni di van der walls sono legami deboli se presi singolarmente, ma essendo numerosi nelle macromolecole, le complesso sono significativi nel determinare la struttura tridimensionale delle proteine, degli acidi nucleici, dei polisaccaridi e dei lipidi di membrana l'acqua ha un punto di fusione, ebollizione e un calore di evaporazione più elevati rispetto agli altri liquidi che conosciamo: proprietà che sono conseguenza delle ATTRAZIONI tra MOLECOLE DI ACQUA ADIACENTI che conferiscono all'acqua allo stato liquidò una coesione internaogni atomo di H di una molecola d'acqua condivide una coppia di elettroni con l'atomo centrale di O si dispongono con gli orbitali secondo un TETRAEDRO lunghezza del legame covalente= 0,095 nm ossia 1Armstrong legame corto perchè H è molto piccolo l'angolo di legame tra le molecole è di 104,5° il nucleo dell'ossigeno attrae gli elettroni in modo molto più forte del nucleo dell' idrogeno: l'OSSIGENO È PIÙ ELETTRONEGATIVO 8+ H O 8- 8- H 8+ la distribuzione degli elettroni che sono in compartecipazione tra H e O non è quindi simmetrica: gli elettroni si trovano molto più spesso nelle vicinanze dell'atomo di ossigeno che di idrogeno il risultato è l'INEGUALE DISTRIBUZIONE degli ELETTRONI e la FORMAZIONE DI DUE DIPOLI ELETTRICI NELLA MOLECOLA D'ACQUA uno lungo ciascuno dei legami H-O ogni atomo di idrogeno porta una l'attuale carica positiva e ogni tomo di ossigeno una parziale carica negativa uguale alla somma delle sue cariche parziali positive (H++ +++ O25) 25- raggio di van der walls dell'O è di 0,14 nm grosso della molecola d'acqua corrisponde al volume dell'ossigeno si viene a generare un'ATTRAZIONE ELETTROSTATICA tra molecole d'acqua vicine in una soluzione d'acqua pura osservo che semplicemente tdall'apparenza dell'acqua si vede che non è una sostanza simile alle altre ma vi sono forze che tengono insieme le molecole d'acqua che sono legami deboli esempio plastico: cade goccia d'acqua su superficie impermeabile forma delle gocce semisferiche 8+ 8+ 8- Legame idrogeno 0,177 nm 8+ * Legame covalente 0,0965 nm 8- 8+ (b) vi sono delle forze di coesione interne: alcune le troviamo in tutte le molecole (interazioni di Van der Walls) altre sono interazioni deboli prese singolarmente ma se moltiplicate all'interno di una soluzione diventano significative l'interazione tra l'atomo di ossigeno e l'atomo di idrogeno di un'alta molecola viene detta LEGAME A IDROGENO 104,5°i legami a idrogeno sono relativamente deboli e nell'acqua allo stato puro hanno un'ENERGIA DI DISSOCIAZIONE di circa 23KJ/mol rispetto alla 470 Kj/mol del legame covalente C-C legame covalente 20 volte più forte di quello a idrogeno il legame a idrogeno è per il 10% COVALENTE e per la sovrapposizione degli orbitali di legame e per il 90% ELETTROSTATICO a temperatura ambiente l'energia termica di una soluzione acquosa è dello stesso ordine di grandezza di quella necessaria per rompere i legami a idrogeno quando l'acqua viene riscaldata l'aumento di temperatura è dovuto al movimento più veloce delle molecole d'acqua energia cinetica è proporzionale alla velocità delle molecole: più è alta energia più è alta la velocità si muovono in maniera casuale e velocemente 토 2mv2 -1-8 ogni legame ha vita media da 1 a 20 picosecondi; quando si rompe un legame se ne riforma uno nuovo o con la stessa molecola o con un'altra FLICKERING CLUSTERS= gruppi di molecole di acqua unite da legami a idrogeno con una vita media così breve gran numero di legami idrogeno che si forma tra le molecole conferisce all'acqua allo stato liquido una GRANDE COESIONE INTERNA La disposizione quasi tetraedrica degli orbitali attorno all'ossigeno consente a ogni molecola di acqua di formare legami idrogeno con altre quattro molecole vicine ma allo stato liquidò le molecole sono in uno stato disordinato e in continuo movimento, cosicchè ogni molecola in media fa solo 3,4 legami a idrogeno con le altre molecole IIIO OIII OI !! DIII DIII IIIO C IIIC - nel ghiaccio invece ogni molecola d'acqua è bloccata nello spazio e forma 4 legami a idrogeno con molecole vicine determinando una STRUTTURA LINEARE A RETICOLO ghiaccio ha una densità inferiore all'acqua P =M V i legami a idrogeno sono responsabili del valore alto del punto di fusione dell'acqua= necessaria un'elevata quantità di energia termica per rompere i legami a idrogeno necessari per stabilizzare la struttura cristallina del ghiaccioquando il ghiaccio fonde o evapora, l'entropia del sistema acquoso aumenta perchè la disposizione ordinata delle molecole di acqua ne, ghiaccio passa a quella meno ordinata dello stato liquido o gassoso AG = DH-TAS- entropia 1. entalpia fusione e evaporazione a temperatura ambiente avvengono spontaneamente AG negativo i legami a idrogeno si formano anche tra un atomo elettronegativo, accettore di idrogeno come ossigeno o azoto con una coppia di elettroni non condivisa, è un atomo di idrogeno legato covalentemente a un altro atomo elettronegativo 1 Accettore C di idrogeno O H ZINE-O- N H O ONIE-O- H O H H H N N. N 1 es. metano non formano legami a H perche il legame non è polarizzato e l'H non ha una sufficiente quantità di carica positiva H legato a molecole con alta elettrinegatività: fluoro, azoto, zolfo legame più forte tra H e F in una soluzione di acido fluoridrico Es, carbossile l'H è legato all'O carbossile è un gruppo polare il gruppo chetonico ha un O con lone pair ,iberi quindi può formare un legame a H con atomo poco elettronegativo il legame a idrogeno ha anche una natura DIREZIONALE= dipende dalla geometria in cui i 3 atomi sono disposti i legami a idrogeno sono più forti quando le molecole legate sono orientate in modo da rendere MASSIMA L'INTERAZIONE ELETTROSTATICA avviene quando l'atomo di idrogeno e gli altri due atomi che partecipano al legame sono su una linea retta: accettore è in linea con il legame covalente tra l'atomo donatore e l'H O Legame idrogeno forte P=OWH Legame idrogeno debole la carica positiva dello ione H è posta tra le due cariche parzialmente negative H - -P O R 1 - 1 -C 1 1 O N Donatore di idrogeno -0- / questa proprietà determina la formazione di strutture tridimensionali ben precise sia nelle proteine sia negli acidi nucleici in cui vi sono moltissimi legami a idrogeno intra molecolari
L'acqua come solvente
l'acqua è un solvente polare quindi dissolve la maggior parte delle molecole cariche o polari dette IDROFILICHE al contrario i solventi non polari solubilizzano bene le molecole IDROFOBICHE ossia composti non polari come i lipidi e le cere l'acqua scioglie i sali e stabilizza gli ioni indebolendo le loro interazioni elettrostatiche e quindi si oppone alla tendenza ad associarsi in una struttura cristallina Ione CI- idratato H2O CI- CI- Na+ + + + Si noti l'orientazione non casuale delle molecole d'acqua + Na+ Ione Na+ idratato l'acqua scioglie facilmente anche le biomolecole contenenti gruppi funzionali carichi come carbossilici di acidi ionizzati, amminici protonati, esteri fosforici, anidridi fosforiche l'acqua dissolve tali composti SOSTITUENDO I LEGAMI A IDROGENO SOLUTO-SOLUTO che uniscono queste biomolecole l'una all'altra con LEGAMI A IDROGENO ACQUA- SOLUTO annullando le interazioni elettrostatiche tra le molecole di soluto è efficace nel rompere le interazioni tra gli ioni perchè la sua costante dielettrica è ELEVATA a 25°℃ è 785 F= Q1 Q2 la dipendenza da r fa sì che le attrazioni o repulsioni ioniche agiscano solo in ambienti molto limitati: tra 10 e 40 nm quando il solvente è l'acqua le interazioni con gli ioni sono importanti per la nostra fisiologia quando un sale si discioglie gli ioni che lasciano i reticolo cristallino acquisiscono una maggiore libertà di movimento= tale AUMENTO DI ENTROPIA è responsabile della facilità con cui i sali si disciolgono in acqua ioni SOLVATATI in acqua le interazioni con le molecole d'acqua sono più forti di quelle che hanno tra di loro Ione Cl- idratato CI- se ho membrana con ioni ai due lati della membrana non la attraversano perchè devono rompere delle interazioni elettrostatiche, processo che richiede energia, le membrane biologiche sono una barriera al passaggio degli ioni Si noti l'orientazione non casuale delle molecole d'acqua Na+ Ione Na+ idratato proprietà di solvatazione è fondamentale per la propagazione dell'impulso nervoso: se non vi è una differenza di potenziale non si ha la propagazione dell'impulso nervoso