Legami sigma, pi greco e ibridazioni in chimica
Slide di Università sui legami sigma, pi greco e ibridazioni. Il Pdf esplora la formazione dei legami attraverso la sovrapposizione degli orbitali atomici e introduce l'ibridazione, un concetto fondamentale in Chimica per gli studenti universitari.
Mostra di più14 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Legami e Ibridazioni
Legami o legami a e ibridazioniLegame sigma o
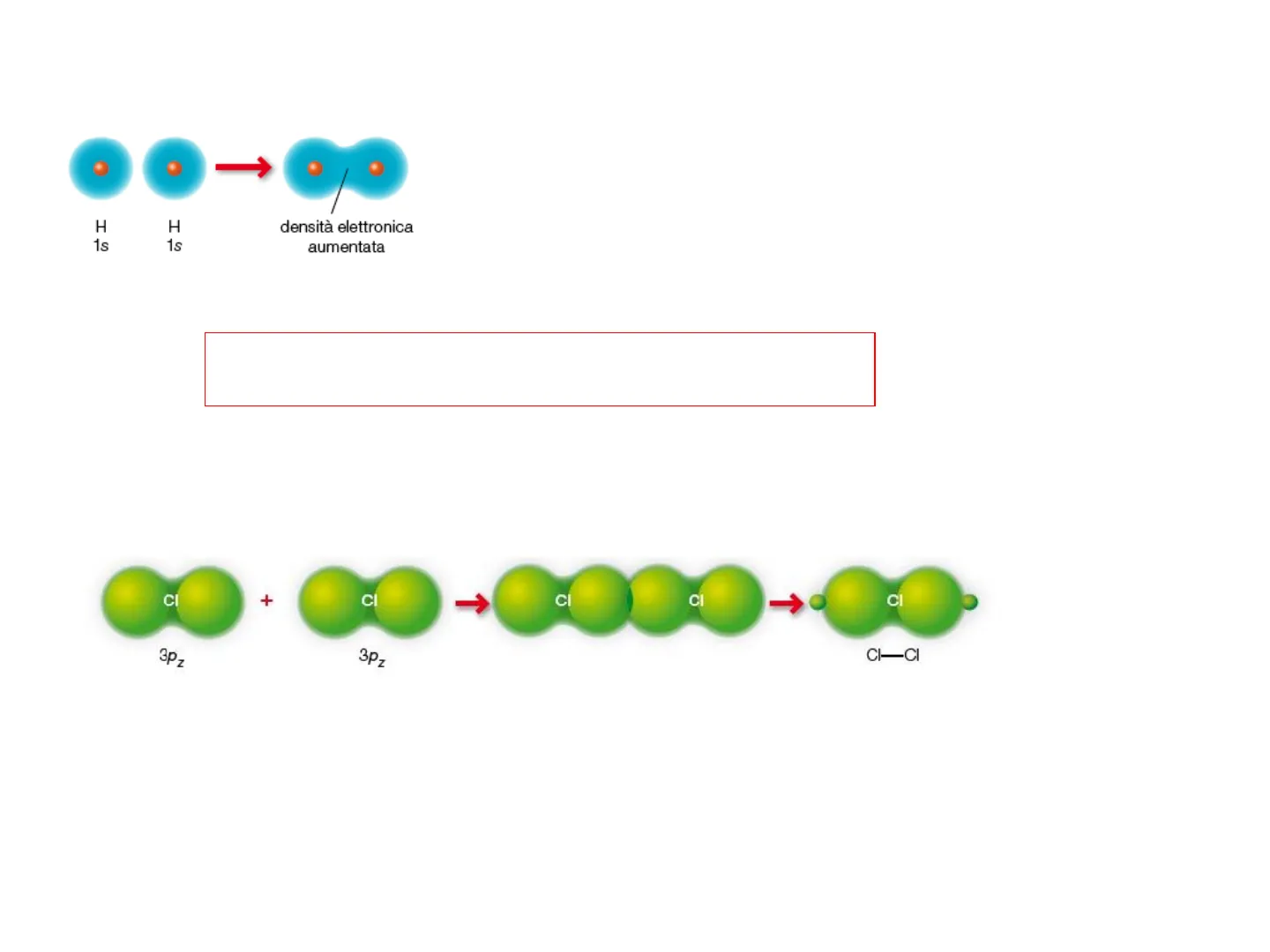
H 1s H 1s densità elettronica aumentata Se due atomi di idrogeno si avvicinano, gli orbitali s di entrambi gli atomi si fondono a formare un'unica nuvola elettronica, che avvolge entrambi i nuclei ed è più stabile. La massima densità di carica è localizzata nella zona internucleare
Legame sigma (o) = legame covalente in cui la sovrapposizione degli orbitali atomici è concentrata lungo l'asse di legame
CI + CI 1 cl CI 1 CI 3p, 3Pz CI-CI Nel caso della molecola di cloro Cl2, che ha una configurazione elettronica esterna 3s23p5, i due elettroni che vengono messi in compartecipazione per realizzare l'ottetto appartengono a orbitali p, per cui l'orbitale molecolare che ne risulta avrà una forma diversa da quello della molecola di idrogeno.Legame pi greco a
+ T S S σ (s) + S p σ (ps) + 1 -- p p σ (pp) + 1 p p Sia nella molecola di idrogeno che in quella di cloro la retta che collega idealmente i due nuclei (asse di legame) è avvolta completamente dalla nuvola elettronica dell'orbitale molecolare, che viene chiamato legame sigma (o). Nelle molecole in cui si formano legami doppi o tripli, la sovrapposizione delle nuvole elettroniche del secondo e terzo legame, lungo rette perpendicolari al primo, determina la formazione di orbitali molecolari che non includono l'asse di legame. Questi legami sono chiamati legami pi greco (7).
simmetria simile rispetto all'asse di legame simmetria simile rispetto all'asse di legame si forma il legame o non si forma il legame o sovrapposizione sovrapposizione
Legame Pi Greco
Legame pi greco (I) = legame covalente formato dalla sovrapposizione di orbitali p parallelio
+ - 0 TT 0 - π 0=0 O2 Esempi: ossigeno molecolare O2 i due atomi (O = 8e-) formano un doppio legame, mettendo in comune due coppie di elettroni per raggiungere l'ottetto; solo uno dei due legami è di tipo sigma (o), mentre l'altro è lungo una retta perpendicolare al legame sigma, per cui la nuvola elettronica non può avvolgere completamente l'asse di legame. La molecola di azoto, N2, (N=7e-) forma un legame triplo, con tre coppie di elettroni, appartenenti a orbitali p e quindi disposti lungo rette tra loro perpendicolari: solo un legame è di tipo o, mentre il secondo e il terzo legame tra i due atomi di azoto sono di tipo I, perché gli orbitali molecolari che si vengono a formare non includono la retta che collega i due nuclei.
1 Pz P Px t 1 Py Py Py Py Legame It IN. ·NI IN=NI Riassumendo: Uno dei due legami tra i due atomi di ossigeno (nella molecola di O2) è lungo la retta che congiunge i due nuclei ed è quindi un legame sigma. L'altro legame, invece, non coincide con la retta che collega i due nuclei ed è perciò un legame pi greco. Nella molecola di N2, si realizzano un legame sigma e due legami pi greco.
Legame At Pz
Ibridazione
GIbridazione Ibridazione: combinazione di due o più orbitali atomici per formare un nuovo set di orbitali definiti orbitali ibridi L'ibridizzazione (o ibridazione) è un procedimento di combinazione di un certo numero di orbitali con contenuto energetico poco diverso di uno stesso atomo che permette di ottenere nuovi orbitali ibridi equivalenti (isoenergetici) con i lobi orientati lungo le direzioni dei possibili legami che l'atomo centrale di una molecola può formare con altri atomi. Il numero di orbitali ibridi ottenuti è uguale al numero di quelli che vengono combinati, cosicché il numero totale di orbitali di valenza dell'atomo non cambia. Il processo di ibridazione può essere accompagnato dalla promozione di uno o più elettroni in orbitali più alti; ciò comporta una spesa energetica iniziale da parte dell'atomo che è tuttavia largamente compensata nel momento in cui esso va a legarsi con altri atomi a formare una molecola2p2 Î E sp3 Î - 252 152 N.B. L'ibridazione di orbitali atomici è un processo che richiede ENERGIA, ma aumentando il numero di elettroni "spaiati" su altrettanti orbitali ibridi, aumenta il numero dei legami covalenti che quell'atomo può formare. Quindi l'energia spesa inizialmente viene recuperataIL NUMERO DI ORBITALI IBRIDI DEVE ESSERE UGUALE AL NUMERO DEGLI ORBITALI ATOMICI DI PARTENZA
1 orbitale S 3 orbitali P 4 orbitali ibrid sp3 + Copyright 1998 Jian Shen NB 1 orbitale s 3 orbitali p Non confondere l'apice con quello usato per scrivere la configurazione elettronica in cui indica il numero di e- presenti negli orbitali
1 orbitale S 2 orbitali P 3 orbitali ibridi sp2 + right 1998 Jian She Copyright 1998 Jian Shen NON IBRIDATO
1 orbitale P 2 orbitali ibridi sp 1 orbitale S + NON IBRIDATI Copyright 1998 Jian ShenIbridazione degli orbitali del carbonio nella molecola del metano
Ibridazione del Carbonio nel Metano
+ 25 +2px + 2py + 2p= y ibridizzazione 2s e 2p. e 2py e 2pz + CH 4 orbitali di partenza orbitali ibridi 2sp3 (C=6 e- 1s22s22p2) C non ibridizzato 2s DOO 2p H e H HHHH 0 tetraedrica H C 1s 1s 1s 1s 2sp2 H CH 4 ibridizzato C DOOD 2sp3 CIbridazione degli orbitali del carbonio nella molecola del metano
E T - 2p (C=6 e- 1s22s22p2) 2s A FIGURA 12-4 Modello "ball-and-stick" del metano, CH4 La molecola ha struttura tetrae- drica e gli angoli di legame H-C-H sono di 109.5°
E sp3 Is H Sp3 109°28' 1s 1.s + H H -Is H sp3 FIGURA 12-6 Legami e struttura in CHA I quattro orbitali del carbonio sono ibridi sp3 (in violetto). Quelli dell'idrogeno (rossi) sono 1s. La struttura è tetraedrica con angoli di legame H-C-H di 109.5° (più precisamente 109°28'). ibridizzazione: CH 4Ibridazione degli orbitali dell'azoto nella molecola dell' ammoniaca e dell'ossigeno nella molecola d'acqua
Ibridazione in Ammoniaca e Acqua
ibridizzazione: NH3, H2O
E E (N=7 e- 1s22s22p3) + - - (O=8 e- 1s22s22p4) 2p 2p 2s 2s
E E - Sp3 Sp3 sp 15 H H -15 H 503 FIGURA 12-7 Orbitali ibridi sp3 e legami in NH3 Uno schema di ibridizzazione sp3 dà una geome- tria molecolare in ottimo accordo con le osserva- zioni sperimentali. Tranne la parte della figura occupato dalla coppia solitaria si tratta di una pi- ramide trigonale.Orbitali ibridi sp2
Orbitali Ibridi sp2
ibridizzazione 2 2 V V x S Py Combinati generano tre orbitali sp2 120° 2 2 Y + + x - x Rappresentati come gruppo + A FIGURA 12-8 Schema di ibridizzazione sp2 Ciascun orbitale ibrido sp2 è formato da due lobi, uno più grande l'altro più piccolo; giacciono in un piano e sono diretti verso i vertici di un triangolo equilatero, gli angoli sono di 120° N-Ibridazione degli orbitali del carbonio nella molecola dell'etene (C2H4) formazione di legami rt y H HO C 0 H Il gruppo di orbitali sp2 + p Legami sigma (o) TT H H H H C C H H H H TT Sovrapposizione di orbitali p che porta a legami TT
1 1 2p E E 14 2 Pz - orbital I - bond Pz - orbital o - bond plane of the SP2 - orbitals T - bond A FIGURA 12-13 Modello "Ball-and-Stick" FIGURA 12-12 Legami sigma (o) e pi greco (1) in C2H4 Gli orbitali in rosso violetto sono ibridi sp2, quelli blu orbitali 2p. Gli orbitali ibridi sp2 si sovrappongono lungo la linea che collega gli atomi legati - legami o . Gli orbitali 2p si sovrappongono di lato e formano legame T. 20 -3111 Dopo promozione di un e- 2s all'orbitale 2p vuoto si ha ibridazione dell'orbitale 2s e di due dei tre orbitali p Il terzo orbitale p è ortogonale al piano su cui giacciono gli orbitali sp2. la molecola è planare, tutti gli atomi giacciono sullo stesso piano. Tra i due C si instaura un legame o per sovrapposizione di due orbitali sp2. Gli orbitali pz non ibridati si sovrappongono originando un legame z. I restanti orbitali sp2 sono utilizzati per la formazione di legami con 4 atomi di HOrbitali ibridi sp
Orbitali Ibridi sp
ibridizzazione 2 Z y -x x P. 1 Combinati generano due orbitali sp Z 180º V * Che sono rappresentati come gruppo + + r A FIGURA 12-9 Schema di ibridizzazione sp Nell' ibridazione sp sono coinvolti l'orbitale s ed uno soltanto degli orbitali p. Sono orientati in modo da formare un angolo di 180°Ibridazione degli orbitali del carbonio nella molecola dell'etino - o acetilene (C2H2)
Ibridazione del Carbonio nell'Etino
H H H H Formazione di legami o Formazione di legami Modello a riempimento spaziale A FIGURA 12-14 Legami sigma (or) e pi greco (#) in C2H2 Uno scheletro di legami o collega gli atomi H-C-C-H con un orbitale Is degli atomi H e gli orbitali sp degli atomi C. Ci sono due legami 7. Ogni legame 7 consiste di due segmenti paralleli a forma di sigaro. I quattro segmenti in realtà si fondono dando un guscio cilindrico cavo che circonda l'asse del legame o carbonio-carbonio.
11 11 20 2p 11 E E sp 11 2 (C=6 e- 1s22s22p2) Un triplo legame C=C consiste di un legame o formato per sovrapposizione di orbitali ibridi sp (uno per ciascun atomo di C. L'altro sp forma legami o con H) e di due legami T. Un legame « si forma per sovrapposizione di una coppia di orbitali atomici 2p paralleli; il secondo legame « per sovrapposizione di una seconda coppia di orbitali 2p paralleli b b TO