Le Proteine: struttura e proprietà degli amminoacidi in Biologia
Documento di Università sulle Proteine, gli amminoacidi e le loro proprietà. Il Pdf esplora le strutture comuni degli amminoacidi, il legame peptidico e le proprietà chimico-fisiche, con tabelle e diagrammi esplicativi per la Biologia.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
LE PROTEINE
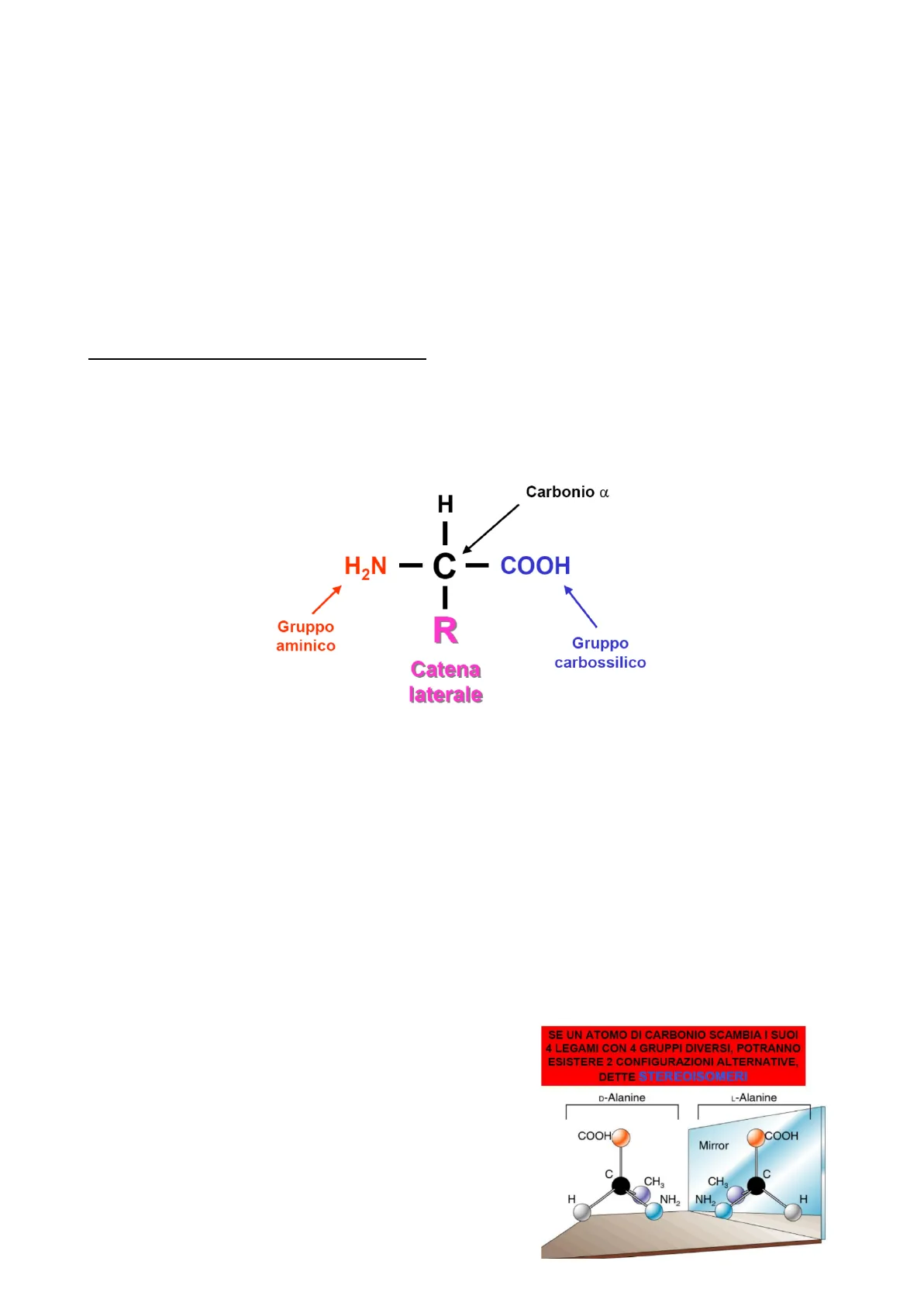
GENERALITÀ SUGLI AMMINOACIDI
Terminati gli acidi nucleici, si può cominciare con le proteine, che sono polimeri di amminoacidi. Di conseguenza si partirà con la spiegazione dagli amminoacidi: tutti gli amminoacidi possiedono una struttura comune, che viene codificata a partire dall'informazione nel genoma.
Carbonio a H I HON C -COOH I R Gruppo aminico Gruppo carbossilico Catena laterale
Il legame peptidico è fatto dal ribosoma, che è un enzima principalmente costituito da RNA e da una componente proteica, che sa catalizzare solo la formazione di un legame peptidico tra il gruppo carbossilico di un amminoacido e il gruppo amminico di un altro amminoacido. Questo è il motivo per cui, nonostante molecole con un gruppo carbossilico e un gruppo amminico si possano trovare anche al di fuori degli amminoacidi classici, solo quelli fatti in questa maniera vengono utilizzati per fare proteine: infatti il ribosoma è in grado di portare avanti la reazione solo tra amminoacidi con questa struttura comune. Per entrare nel ribosoma inoltre, gli amminoacidi devono essere legati ad un tRNA, tanto che qualora si voglia trarre in inganno a scopi medici il sistema di produzione delle proteine, si deve caricare sul tRNA un elemento che possieda un carbonio-alfa, un gruppo amminico e un gruppo carbossilico. Anche se non fa parte dei 20 amminoacidi canonici, finché abbia questa struttura comune, l'elemento introdotto verrà sempre utilizzato dal ribosoma per polimerizzare una proteina. È necessario anche usare una delle triplette di STOP per poter proseguire con l'amminoacido sintetico. Siccome il carbonio-alfa è legato a 4 componenti diverse (tranne che nella glicina) tutti gli amminoacidi hanno un centro chirale in corrispondenza di questo carbonio.
Di conseguenza, esisteranno gli L-amminoacidi e gli SE UN ATOMO DI CARBONIO SCAMBIA I SUOI 4 LEGAMI CON 4 GRUPPI DIVERSI, POTRANNO ESISTERE 2 CONFIGURAZIONI ALTERNATIVE, DETTE STEREOISOMERI D-amminoacidi: nelle proteine si trovano gli L-amminoacidi. Gli D-amminoacidi invece si trovano solitamente nel peptidoglicano (zuccheri e amminoacidi) della spessa parete dei D-Alanine L-Alanine batteri, soprattutto Gram+. Questa struttura però non viene realizzata dai ribosomi, bensì da enzimi specifici della parete COOH COOH che possono usare anche i D-amminoacidi per formare legami Mirror peptidici. C C Dunque questi D-amminoacidi possono trovarsi anche negli alimenti ma possono essere comunque eliminati dal nostro organismo con meccanismi specifici, purché non siano presenti CH3 CH3 H NH2 NH2 Hin quantità eccessive.
CLASSIFICAZIONE DEGLI AMMINOACIDI IN BASE A CARICA E POLARITÀ
Gruppi R alifatici, non polari Gruppi R aromatici COO H3Ň-C-H H3N-C-H H3N-C-H CH- CH2 CH C CH NH ÓH Fenilalanina Tirosina Triptofano Gruppi R carichi positivamente ÇOO" COO" H3N-C-H H3N-C-H H3N-C-H CH CH2 CH2 1 CH- CH C-NH CH2 CH2 CH2 NH - +NHg C=NH2 NH2 Lisina Arginina Istidina Gruppi R carichi negativamente H3N-C-H H3N-C-H CH CH COO CH COO- Aspartato Glutammato
- amminoacidi non polari
- glicina: possiede come catena laterale un semplice H, che dunque non le permette di avere un centro chirale e quindi una D-glicina e una L-glicina, ma solo un'unica struttura; la rotazione attorno al legame attorno al legame è libera, quindi nel contesto di una struttura proteica la presenza di glicina rappresenterà un punto di flessibilità; si deve però ricordare che la glicina è una molecola piccola, estremamente solubile in acqua. NOTA BENE: si devono immaginare le proteine come una catenella di amminoacidi: la proprietà della catena è il risultato delle singole proprietà degli amminoacidi.
- alanina: ha come catena laterale un metile; ha una struttura sempre piuttosto flessibile ma di maggiori dimensioni
- prolina: possiede una struttura ad anello, il che la rende non solo più grande ma anche molto meno flessibile, in quanto non può girare liberamente attorno al legame N -- C
- valina: non è rigida, ma la sua struttura diventa leggermente più idrofobica perché possiede una coda idrofobica NOTA BENE: in generale, tutti gli amminoacidi sono solubili in acqua e cristallizzabili in solidi cristallini bianchi.
- leucina: presenta una struttura più lunga
- isoleucina: è un isomero della leucina, con il metile collocato più vicino alla catena (sul C beta)
- metionina: presenta nella sua struttura un atomo di zolfo; è molto lunga e apolare perché la tendenza ad instaurare legami a H è bassa
- amminoacidi aromatici, presentano una componente aromatica all'interno della catena laterale Gruppi R polari, non carichi ÇO0 COO- 000- H3N-C-H H3N-C-H H3N-C-H CH2OH H-C-OH CH2 CH3 SH Serina Treonina Cisteina H3N-C-H H3N-C-H CH CH2 HON 0-9 HAN 0,00 Asparagina COO" COO" HgŇ- -C-H H3N-C-H C H3N-C-H I CH 3 CH - CH HỌC-CHO CH3 CH3 Glicina Alanina Prolina Valina C00 H3N-C-H H3N-C-H H3N-C-H CH- H-C-CH3 ÇH2 CH2 CH2 CH3 CH3 CH3 S CH3 Leucina Isoleucina Metionina COO" HON Glutammina `CH C-N- fenilalanina: presenta un grande gruppo R, leggermente flessibile perché non è direttamente attaccato alla catena, molto idrofobico
- tirosina: molto simile alla fenilalanina, ma con un gruppo ossidrile al fondo della struttura, che gli permette di formare un legame H singolo
- triptofano: presenta un doppio anello con una struttura di grandi dimensioni e molto idrofobica
- amminoacidi polari non carichi
- serina: presenta la stessa struttura dell'alanina, con aggiunto un gruppo OH
- treonina: ha una catena laterale più grande
- cisteina: presenta un gruppo solfidrilico non acido ma decisamente polare, che si può ridurre/ossidare
- asparagina e glutammina: sono le ammidi rispettivamente dell'acido aspartico e del glutammato, con annessi gruppi carbossilici
- amminoacidi basici carichi positivamente
- lisina: possiede un gruppo amminico molto lontano dalla catena laterale
- arginina: possiede un gruppo amminico anch'esso abbastanza lontano, che la rende ancora più polare e con 2 gruppi basici in grado di reagire
- istidina: presenta una struttura ad anello, il gruppo imidazolico, in cui l'azoto può dissociarsi ad un pH abbastanza fisiologico; di conseguenza può agire da tampone in alcune condizioni e può anche agire da catalizzatore acido-base in molti siti catalitici di enzimi
Gli amminoacidi hanno tutti un nome, una sigla a 3 lettere (sovrascritta sulla base delle triplette codificanti) e una lettera: tutti questi tipi di nomenclature vanno sapute.
Tabella 3.I Abbreviazioni degli amminoacidi.
| Amminoacidi | tre lettere (*) | una lettera |
|---|---|---|
| Alanina | Ala | A |
| Arginina | Arg | R |
| Asparagina | Asn | N |
| Aspartato | Asp | D |
| Cisteina | Cys | C |
| Glicina | Gly | G |
| Glutamina | Gin | Q |
| Glutammato | Glu | E |
| Istidina | His | H |
| Isoleucina | lle | I |
| Leucina | Leu | L |
| Lisina | Lys | K |
| Metionina | Me | M |
| Fenilalanina | Phe | F |
| Prolina | Pro | P |
| Sering | Ser | S |
PROPRIETÀ DEGLI AMMINOACIDI
TABLE 3-1 Properties and Conventions Associated with the Common Amino Acids Found in Proteins
| Amino acid | Abbreviation/ symbol | Mr | pK1 (-COOH) | pK2 (-NH3) | pK_ values (R group) | pl | Hydropathy index* | Occurrence in proteins (%)+ |
|---|---|---|---|---|---|---|---|---|
| Nonpolar, aliphatic R groups | ||||||||
| Glycine | Gly G | 75 | 2.34 | 9.60 | 5.97 | -0.4 | 7.2 | |
| Alanine | Ala A | 89 | 2.34 | 9.69 | 6.01 | 1.8 | 7.8 | |
| Proline | Pro P | 115 | 1.99 | 10.96 | 6.48 | 1.6 | 5.2 | |
| Valine | Val V | 117 | 2.32 | 9.62 | 5.97 | 4.2 | 6.6 | |
| Leucine | Leu L | 131 | 2.36 | 9.60 | 5.98 | 3.8 | 9.1 | |
| Isoleucine | lle 1 | 131 | 2.36 | 9.68 | 6.02 | 4.5 | 5.3 | |
| Methionine | Met M | 149 | 2.28 | 9.21 | 5.74 | 1.9 | 2.3 | |
| Aromatic R groups | ||||||||
| Phenylalanine | Phe F | 165 | 1.83 | 9.13 | 5.48 | 2.8 | 3.9 | |
| Tyrosine | Tyr Y | 181 | 2.20 | 9.11 | 10.07 | 5.66 | -1.3 | 3.2 |
| Tryptophan | Trp W | 204 | 2.38 | 9.39 | 5.89 | -0.9 | 1.4 | |
| Polar, uncharged R groups | ||||||||
| Serine | Ser S | 105 | 2.21 | 9.15 | 5.68 | -0.8 | 6.8 | |
| Threonine | Thr T | 119 | 2.11 | 9.62 | 5.87 | -0.7 | 5.9 | |
| Cysteine | Cys C | 121 | 1.96 | 10.28 | 8.18 | 5.07 | 2.5 | 1.9 |
| Asparagine | Asn N | 132 | 2.02 | 8.80 | 5.41 | -3.5 | 4.3 | |
| Glutamine | Gin Q | 146 | 2.17 | 9.13 | 5.65 | -3.5 | 4.2 | |
| Positively charged R groups | ||||||||
| Lysine | Lys K | 146 | 2.18 | 8.95 | 10.53 | 9.74 | -3.9 | 5.9 |
| Histidine | His H | 155 | 1.82 | 9.17 | 6.00 | 7.59 | -3.2 | 2.3 |
| Arginine | Arg R | 174 | 2.17 | 9.04 | 12.48 | 10.76 | -4.5 | 5.1 |
| Negatively charged R groups | ||||||||
| Aspartate | Asp D | 133 | 1.88 | 9.60 | 3.65 | 2.77 | -3.5 | 5.3 |
| Glutamate | Glu E | 147 | 2.19 | 9.67 | 4.25 | 3.22 | -3.5 | 6.3 |
*A scale combining hydrophobicity and hydrophilicity of R groups; It can be used to measure the tendency of an amino acid to seek an aqueous environment (- values) or a hydrophobic environment (+ values). See Chapter 11. From Kyte, J. & Doolittle, R.F. (1982) A simple method for displaying the hydropathic character of a protein. J. Mol. Biol. 157, 105-132. "Average occurrence In more than 1,150 proteins. From Doolittle, R.E. (1989) Redundancies In protein sequences. In Prediction of Protein Struc- ture and the Principles of Protein Conformation (Fasman, G.D., ed.), pp. 599-623, Plenum Press, New York. Hanno tutti una massa: il più pesante è il triptofano, con una massa di 204 dalton. Questo deve far capire l'impressionante dimensione delle proteine: per esempio, se si dovesse considerare una proteina non di grandissime dimensioni formata da 100 amminoacidi, essendo il peso medio di un amminoacido di 110 dalton, peserà 110.000 dalton. Tutte le proteine sono caratterizzate dall'avere un gruppo amminico e un gruppo carbossilico: questo fa sì che il gruppo carbossilico si dissoci ad un pH intorno al 2. Quindi a pH fisiologico i gruppi carbossilici sono tutti dissociati. Il gruppo amminico si dissocia quando va oltre un pH 9.5-10: di conseguenza a pH fisiologico di 7-7.4 sono sempre protonati. Nel caso delle catene laterali:
- tirosina, che presenta nella catena laterale un fenolo (acido debole) si dissocia a pKa 10-11, quindi fisiologicamente la tirosina non agisce come acido, a meno che non sia all'interno del sito attivo di una proteina, vicino ad un metallo che favorisca la dissociazione e la donazione di un protone;
- nel caso della cisteina, il suo gruppo solfidrilico oltre pH di 8 può dissociarsi: esistono enzimi specifici che portano avanti proprio questa dissociazione;
- la lisina ha la catena laterale che si dissocia a pH 10-11, quindi sarà praticamente sempre protonata
- arginina: ha la catena laterale che si dissocia a 12.5, quindi anch'essa sarà praticamente sempre protonata
- l'istidina possiede invece una catena laterale che a pH fisiologico di 7 rilascia il protone, di conseguenza può protonarsi in determinate condizioni (soprattutto in presenza di un donatore forte)