Mioglobina ed emoglobina: struttura, funzione e patologie correlate
Slide su mioglobina e emoglobina: struttura, funzione e patologie. Il Pdf, adatto a studenti universitari di Chimica, esplora la struttura e la funzione di queste proteine, gli effettori allosterici e le patologie legate alle mutazioni, come l'anemia falciforme.
Mostra di più17 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Mioglobina ed emoglobina: struttura e funzione
Mioglobina e emoglobina
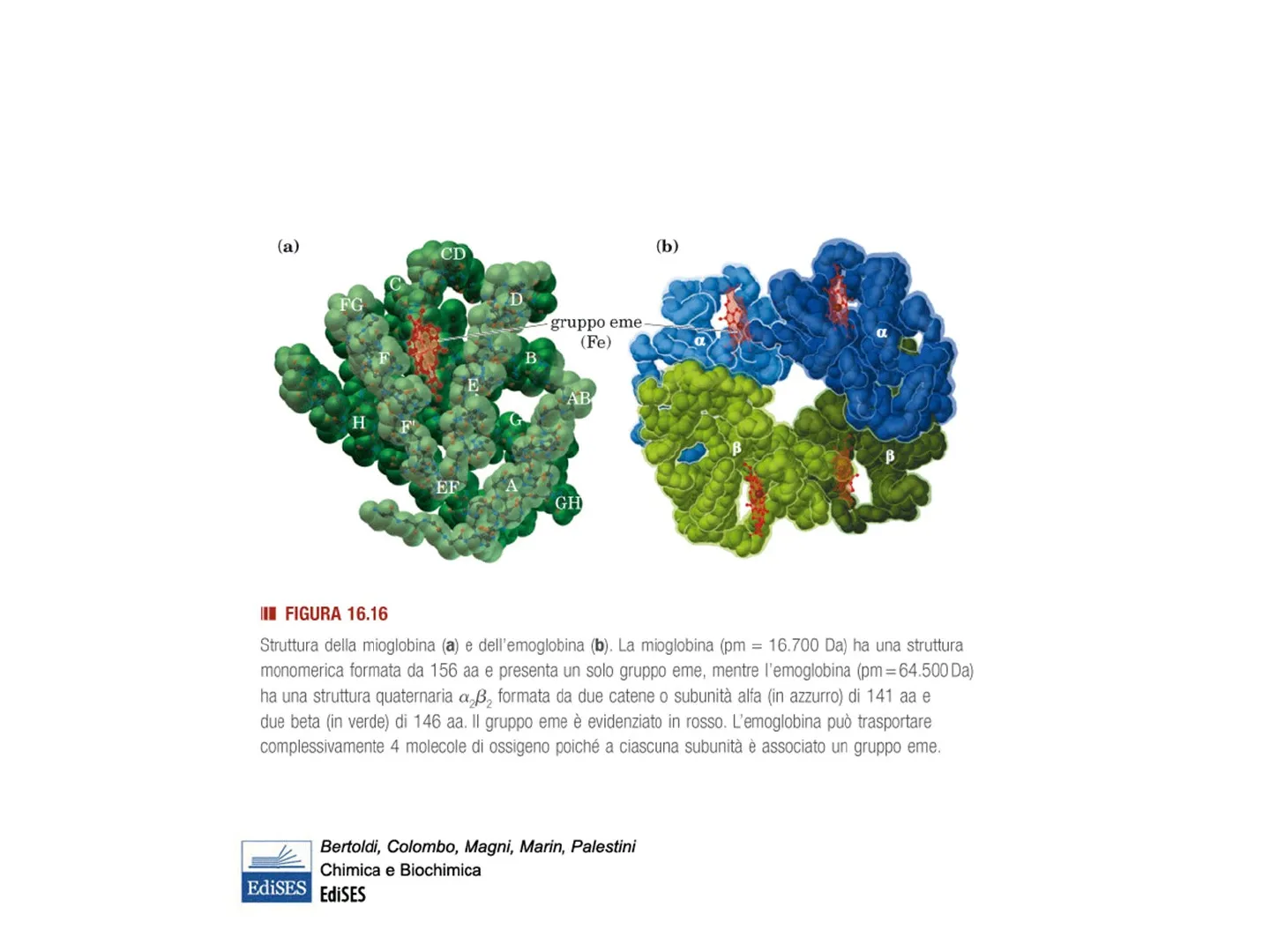
(a) (b) CD C D FG gruppo eme (Fe) F B E AB H F B B EF A GH I FIGURA 16.16 Struttura della mioglobina (a) e dell'emoglobina (b). La mioglobina (pm = 16.700 Da) ha una struttura monomerica formata da 156 aa e presenta un solo gruppo eme, mentre l'emoglobina (pm=64.500 Da) ha una struttura quaternaria «2ß2 formata da due catene o subunità alfa (in azzurro) di 141 aa e due beta (in verde) di 146 aa. Il gruppo eme è evidenziato in rosso. L'emoglobina può trasportare complessivamente 4 molecole di ossigeno poiché a ciascuna subunità è associato un gruppo eme. EdiSES Bertoldi, Colombo, Magni, Marin, Palestini Chimica e Biochimica EdiSES
Struttura dell'emoglobina
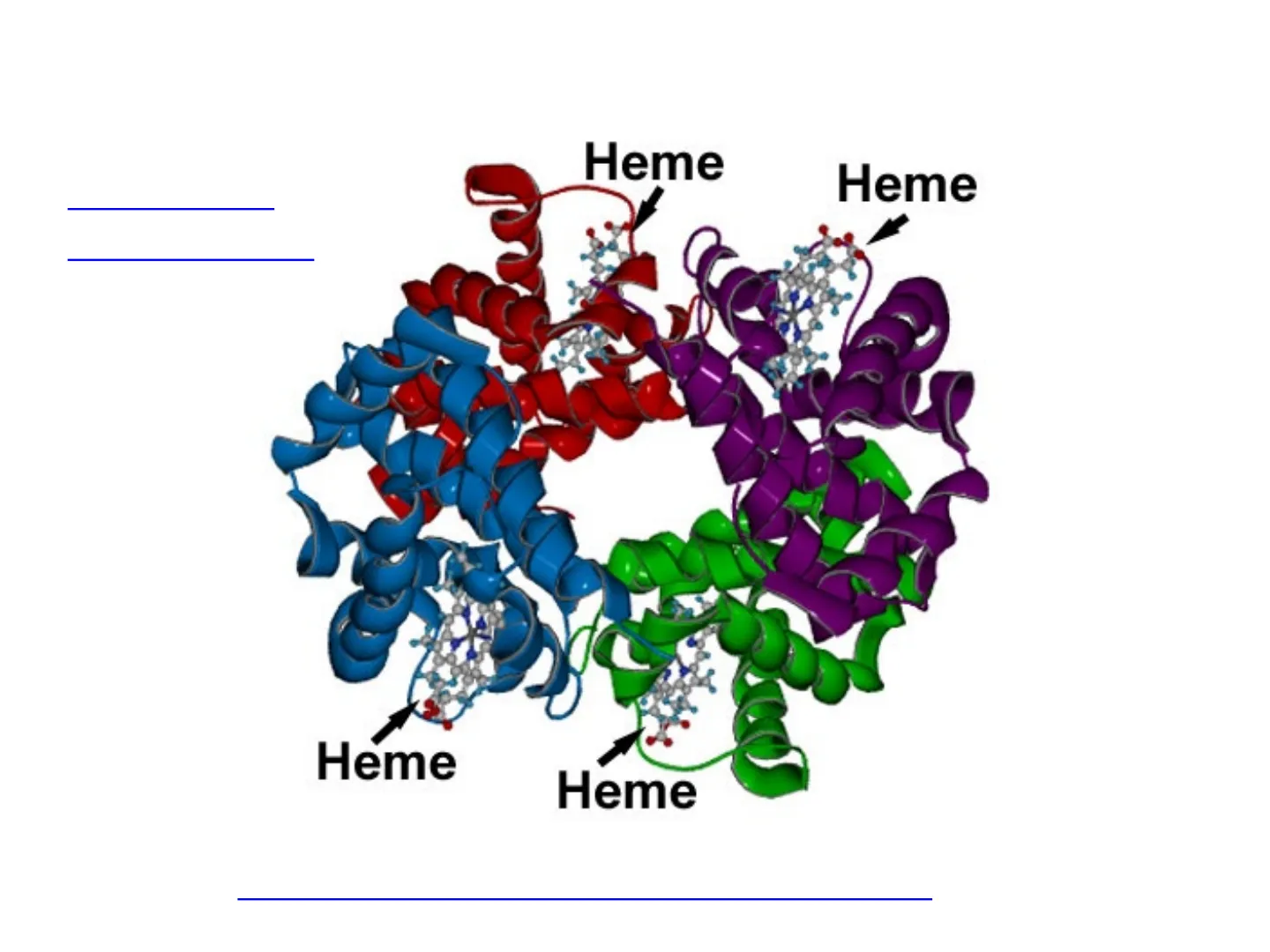
1la struttura dell'emoglobina Animazione conformazioni Heme Heme Heme Heme http://en.wikipedia.org/wiki/Hemoglobin
Emoproteine e legami del ferro
2• L'eme è legato covalentemente alla proteina in una tasca idrofobica Emoproteine A Gris's B Il ferro può formare sei legami: quattro con gli atomi d'azoto della porfirina e due ulteriori legami, disposti uno sopra e uno sotto il piano in cui giace l'anello porfirinico. COO E7 (His 64) F8 (His 93) CH2 Az CH H H2 C H3C- C-C CH3 C N- C HC Fe C C=N"A `N- C H2C C C. C C C H CH3 H 0-0 Elica F Elica E H CH2 Molecola di, ossigeno (O2) Eme F 0-0 11 - C-CH3 ,0-0 C-N. V
Struttura dell'Eme e legame con l'ossigeno
3Struttura dell'Eme Legame reversibile, debole Con O2 (si ossigena, non si ossida) Tramite Fe++ Fe++ chelato in un anello tetrapirrolico: protoporfirina IX Protoporfirina IX + Fe++ = eme Il Fe++ può fare 6 legami: 4 con protoprofirina IX 1 con His della globina ( catena E) 1 con: H2O -- > deossiglobina O2 -- > ossiglobina CO -- > carbossiglobina 0 0 H2C=CH CH3 01 Af 1 CH2 II H3C A B CH N 1 N Fe(II) N N H3C D C CH3 - OOC-CH2-CH2 CH2-CH2-COO N HN CH2 1 C- -N H C=0 H 1 1
Deossi- e ossi-globine
4Deossi- e ossi-globine H H - c- -N Histidine C C- H H- H N Fe Heme is planar. 0 O Deoxygenated Oxygenated Sangue venoso Sangue arterioso Rosso cupo deossi Hb C-N Histidine -C H MSH Fe Heme is domed (nonplanar). Rosso brillante ossiHb
Trasporto di ossigeno e anidride carbonica
5Hb nel trasporto dell'ossigeno e anidride carbonica Hemoglobin + 4 02 -> Hb(02) (Hb) Arterial circulation Î Venous circulation Lungs Heart Tissue Hemoglobin + 4 02 <- Hb(02) (Hb) POLMONI Il CO2 si libera dall'emoglobina L'O2 si lega all'emoglobina O CO 2 NHCOO" 02 02 Fe2+ Fe2+ Fe2+ Fe2+ Fe2+ Fe2+ I Fe2+ Fe2+ NHCOO- Carbamminoemoglobina Ossiemoglobina CO2 O2 Il CO2 si lega all'emoglobina L'O2 si libera dall'emoglobina TESSUTI
Effetto Bohr
02Effetto di Bohr Polmoni SANGUE Muscolo HCO3+ H+ - H CO3 H2O+CO2 RESPIRAZIONE Mb O2 2 Hb-HbH+Hb ) INSPIRAZIONE O2 2 Hb 4O2 Hb 4O2 MbO2 pO2= 100 torr pO2= 30 torr
Meccanismo dell'effetto Bohr
7Effetto di Bohr Polmoni SANGUE Muscolo ESPIRAZIONE RESPIRAZIONE Anidrasi carbonica Anidrasi carbonica H2O+ CO2 H CO3 HCO3+ H+ H CO3 H2O+ CO2 Mb O2 H++ Hb-HbH++Hb INSPIRAZIONE 2 Hb 4O2 Hb 4O2 Mb O2 La CO2 prodotta da lavoro fisiologico dei tessuti deve essere efficientemente allontanata. L'accumulo di CO2 abbassa il pH nei tessuti e nei capillari
Effetto del pH sull'affinità per l'O2 dell'emoglobina
8Effetto del pH sull'affinità per l'O2 dell'emoglobina: effetto di bohr L'effetto Bohr: pH bassa -> bassa affinità -> rilascio di O2 Tissues Lungs 100 Mb 80 7.6 7.2 6.8 pH % Saturation 60 Hb 40 20 0 40 80 120 Po2 (mm Hg) -His-H+ Terminal-NH3+ L'ABBASSAMENTO DI pH conseguente alla PRODUZIONE DI CO2 favorisce il rilascio di ossigeno in quanto diminuisce l'affinità dell'Hb per esso Quando si verifica un INTENSA ATTIVITÀ MUSCOLARE si accumula acido lattico (scarsa ossigenazione) favorendo un ulteriore rilascio di O2 Effetto del pH sull'emoglobina comporta uno spostamento della curva di trasporto a DESTRA
Trasporto di CO2 nel sangue
9Trasporto di CO, nel sangue L'anidride carbonica reagisce con l'Hb formando Carbammati (CO2 + aminogruppi N-terminali di Hb) Nel sangue si forma Bicarbonato CO2+H2O HCO3 + H+ (anidrasi carbonica ) Il sangue venoso ritorna ai polmoni, l'ossigeno provoca il rilascio di protoni e favorisce il rilascio di CO2
Curva di saturazione
10100 - mioglobina saturazione (%) emoglobina 50 - pO2 tessuto pO. polmone > 0 0 20 40 60 80 100 pressione O2 (pO2 in torr) FIGURA 16.19 Curva di saturazione della mioglobina e dell'emoglobina. La curva di saturazione con l'ossigeno della mioglobina descrive un'iperbole, mentre quella dell'emoglobina mostra un andamento ad S o sigmoide. La concentrazione dell'ossigeno (un gas) viene espressa come pressione parziale e misurata in torr nell'atmosfera che si trova in contatto con la soluzione contenente la proteina. La pressione parziale dell'ossigeno alla quale si raggiunge il 50% di saturazione indica l'affinità per l'ossigeno. La mioglobina raggiunge il 50% di saturazione già ad 1 torr, l'emoglobina a 26 torr perché ha un'affinità minore.
Effettori allosterici
2,3-bisfosfoglicerato
11COO- H-C-O-PO_2- I H-C-O-PO32- I H 2,3 bisfosfoglicerato Effettore allosterico negativo (a) 2,3-Bisphosphoglycerate (37 $84 D C ₿, 5 B2 + 81 B F E B 2 H N BPG + 70 G G 1 A F H 79 2 80 o O E ₿2 D + 81 35 82 ₿2 143 83 35 143 C E 80 A +2 N B E B C 02,3-BPG = 0 'Hemoglobin stripped of 2,3-BPG) % Saturation with O2 (Y) 100г 2,3-BPG = 5 mmol/L Normal blood) 2,3-BPG = 8 mmol/L (Blood from individual adapted to high altitudes) 40 80 120 Partial pressure of oxygen (mm Hg)
Monossido di carbonio come effettore allosterico
13Effettori allosterici positivi: Monossido di carbonio (CO) Il monossido di carbonio si lega all'eme con affinità 300x superiore a quella dell'O2 diminuisce la quantità di Hb disponibile per O2 E' UN EFFETTORE ALLOSTERICO POSITIVO: impedisce la dissociazione di H Avvelenamento da CO Terapia: ventilazione con 100% O2
Fattori che regolano il comportamento allosterico
14Effettori allosterici sull'emoglobina Fattori che regolano il comportamento allosterico dell'emoglobina sono: - H+ e CO, (strettamente associati) - 2,3-Bifosfoglicerato (2,3-BPG) - temperatura Sono tutti effettori negativi: Promuovono la forma deossi Inibiscono la reazione Hb + O2 Spostano la curva di dissociazione a destra Aumentano P50
Patologie legate alle mutazioni dell'emoglobina
Anemia falciforme
15Patologie legate alla mutazioni dell'emoglobina Normal Missense Mutation Partial DNA Sequence CCT GAG GAG of Beta Globin Gene: GGA CTC CTC CCT GTG GAG GGA CAC CTC Partial RNA Sequence:CCU GAG GAG CCU GUG GAG Partial Amino Acid Sequence for Beta Globin: Pro Glu Glu Pro Val Glu Hemoglobin Molecule: Red Blood Cell: Anemia falciforme o drepanocitica http://evolution.berkeley.edu/evol ibrary/article/mutations 06 Articolo in Italiano sulla malattia NORMAL HEMOGLOBIN CLUMPED HEMOGLOBIN Video
Talassemie
16Patologie legate alla mutazioni dell'emoglobina Sostituzioni di residui in superficie es. anemia falciforme (sicke cell anemia Sostituzioni di residui interni alla catena globinica es. lisi e anemia emolitica Sostituzioni nell'interfaccia fra le catene a e B TALASSEMIE: Beta-talassemie Alfa-talassemie Video per ulteriori approfondimento Beta Thalassemia - causes, symptoms, diagnosis, treatment, pathology 2019 17