Virologia molecolare: organizzazione del genoma HIV-1 e espressione genica
Documento di Università su Virologia Molecolare 18/03/2024. Il Pdf esplora l'organizzazione del genoma di HIV-1 e i meccanismi di espressione genica, con un focus sulle proteine Tat e Rev, per la materia Biologia.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
VIROLOGIA MOLECOLARE 18/03/2024
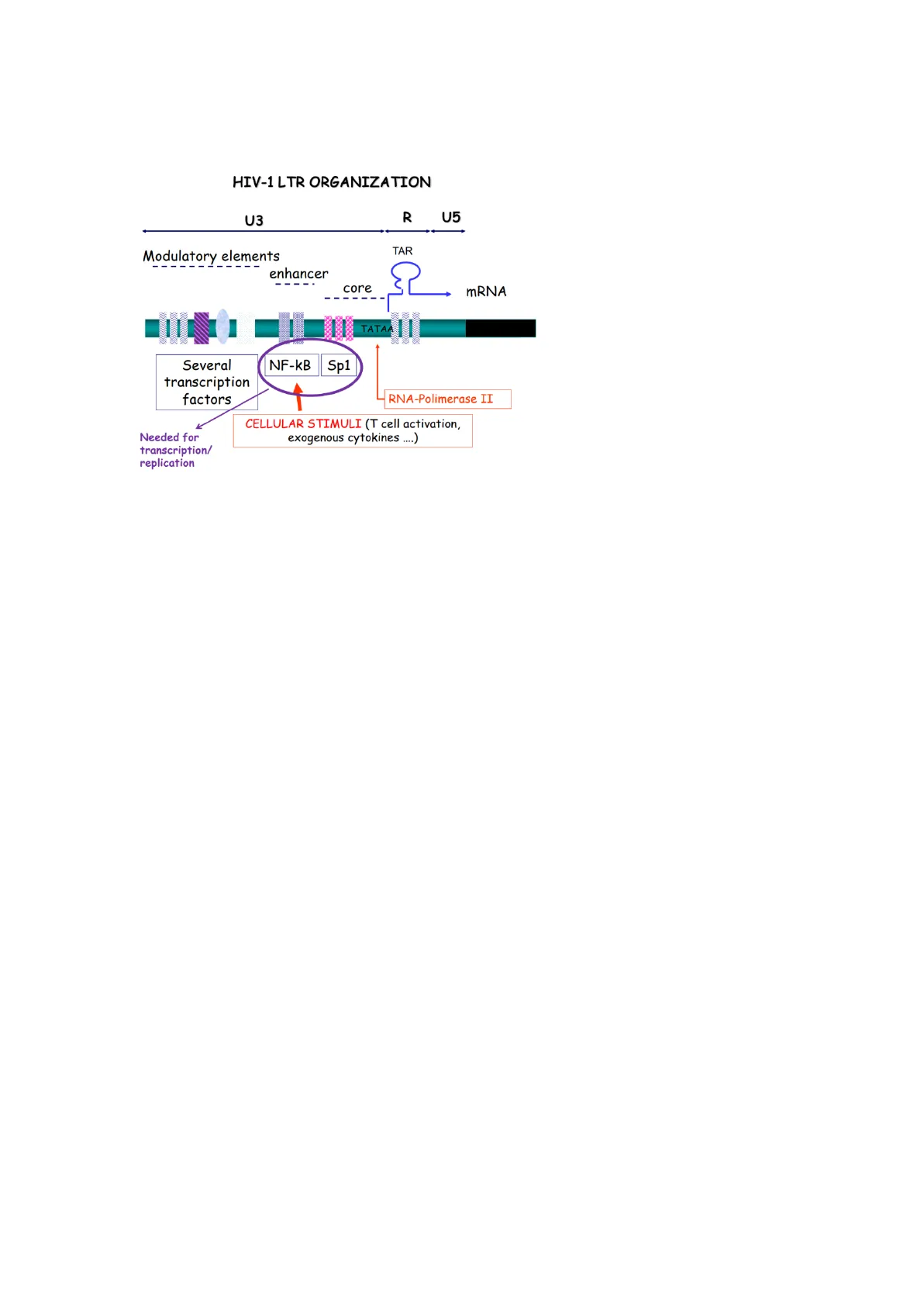
HIV-1 LTR ORGANIZATION
U3 R U5 TAR Modulatory elements enhancer core MRNA TATAA NF-KB Sp1 Several transcription factors RNA-Polimerase II CELLULAR STIMULI (T cell activation, exogenous cytokines .... ) Needed for transcription/ replication
Nella scorsa lezione abbiamo parlato del virus dell'immunodeficienza umana, della biologia del virus e ripercorrendo il ciclo vitale di HIV siamo arrivati al momento in cui il DNA provirale del virus viene integrato all'interno del genoma della cellula ospite. Il DNA provirale, come tutti i retrovirus, una volta che ha raggiunto il comparto nucleare e nel caso del virus dell'HIV esso viene raggiunto in maniera attiva, grazie al complesso di pre integrazione, passa attraverso il poro nucleare grazie all'interazione dovuta a una serie di fattori cellulari fino a contattare il genoma cellulare e ad essere integrato grazie all'integrasi virale nel genoma cellulare. Se le condizioni dello stato della cellula sono favorevoli questo DNA provirale viene espresso. Affinché esso sia espresso deve necessariamente essere attivata la trascrizione e per come tutti i retrovirus gioca un ruolo importante una delle tre regioni dell'LTR, ossia U3, dove risiedono l'enhancer e il promotore. La trascrizione è schematizzata nella diapositiva: U3 è la porzione più grande di LTR; U3 è seguita da R, quest'ultima è il punto dove inizia la trascrizione e a valle di esso ci sta U5, che farà parte del trascritto genomico. La regione U3 di HIV è particolare. Il tropismo di questo virus è molto ristretto e tale restrizione è dovuta in primis al suo anti-recettore che in maniera specifica deve legare il suo recettore, che è la proteina CD4 che è espressa solo su alcuni tipi cellulari. Anche l'organizzazione della sua LTR stessa contribuisce alla restrizione del virus: i retrovirus in generale, una volta integrato il DNA provirale nel genoma della cellula ospite, l'espressione di esso parte in automatico perché U3 nella maggioranza dei retrovirus contiene sequenze consensus per fattori di trascrizione cellulari ubiquitari e costitutivi, quindi non c'è richiesta di particolari condizioni cellulari perché venga attivata la trascrizione. Nel caso di HIV ci sono almeno due limitazioni: una è il fatto che uno dei fattori di trascrizione fondamentali per attivare la trascrizione di questo pro-virus è il fattore di trascrizione NF-KB. Esso è presente nella cellula in forma inattiva, suscettibile ad essere attivato a seconda dei segnali che arrivano dall'esterno che possono essere svariati (es. Interferone) e sicuramente per quanto riguarda la cellula T,un segnale per l'attivazione di NF-KB è l'attivazione della stessa cellula T, che presenta l'antigene. Se questa cellula è in uno stato di riposo senza particolari stimoli, il fattore NF-KB si trova in forma inattiva. Questo significa che la trascrizione del DNA provirale avviene solo in una cellula in cui NF-KB è nella sua forma attiva; quindi, lo stato della cellula deve essere attivato. L'altro fattore trascrizionale è sp1. Inoltre NF-KB è un complesso trascrizionale ubiquitario, lo troviamo in tutte le cellule.
HIV-1 Gene Expression
DNA provirus RNA transcription RNA nuclear export RNA splicing Early regulatory mRNAs (doubly spliced) Late structural mRNAs (unspliced, singly spliced) + Gag-pol (unspliced mRNA) Tat Env (singly spliced mRNA) also: Vpr, Vpu, Vif encoded by singly spliced mRNAs Rev also: Nef encoded by doubly spliced mRNA Callen. J. Virol. 65:1053, 1991
Un altro fattore di trascrizione necessario per l'attivazione della trascrizione del DNA provirale (anche se è meno penetrante come dipendenza rispetto a NFKB, anche se è più cell-specific) è nFAT. Esso si trova in uno stato inattivato nella cellula inattiva e si trova solo in alcuni tipi cellulari del sistema immunitario. Ci sono anche altri fattori di trascrizione che si legano, ma quelli appena citati sono quelli limitanti, ossia fanno la differenza sullo stato di attivazione della LTR. Tat plays a crucial role in synthesis of full-length HIV-1 mRNA transcripts. Poniamo il caso che il virus abbia infettato una cellula che si trovava in uno stato di attivazione ideale per l'espressione del pro-virus, vediamo cosa succede: inizia la trascrizione del pro-virus che si è integrato. Nella fase precoce dell'infezione della cellula il DNA provirale viene trascritto in RNA genomico che avrà più destini; tuttavia, all'inizio dell'infezione esso viene,di default, completamente maturato; infatti, ci sono più siti accettori di splicing, per cui l'RNA genomico subirà splicing multipli da cui si formeranno messaggeri da cui verranno tradotte soltanto tre proteine virali quali Tat, Rev e Nef. Soltanto in una fase più tardiva, e questo dipende dall'accumulo della proteina Rev, l'RNA genomico trascritto potrà lui stesso essere trasportato dal nucleo al citoplasma e qui andare incontro a traduzione e poi, in una fase successiva, ad impacchettamento nel nucleocapside, oppure può subire solo un evento di splicing per cui si forma il messaggero che viene anch'esso trasportato dal nucleo al citoplasma ed esso è il messaggero da cui verrà prodotta la poliproteina env insieme ad altre proteine accessorie del virus.
Model for the stimulation of elongation by Tat
A Nf-kb Sp1 Sp1 Sp1 Tflld Tat +Tat, pTefb Nf-kb Sp1 Sp1 Sp1 Tflld Tat In the absence of Tat, transcription complexes are poorly processive, and the great majority (9 of 10) terminate within 60 bp of the initiation site, releasing transcription components and short transcripts. Production of the Tat protein upon translation of mRNAs spliced from rare, full-length transcripts and its recruitment of p-Tefb and other regulators of elongation to nascent RNA allow transcriptional complexes to pass through the elongation block and synthesis of full-length viral RNA. From Flint et al. Principles of Virology (2015), ASM Press
Tat e Rev sono definiti in maniera impropria "fattori di trascrizione" del virus, poiché sono coinvolti nell'espressione genica del virus ed in particolare Tat è fondamentale per la trascrizione dell'RNA genomico. Quando il virus infetta de novo una cellula il DNA provirale viene integrato e la sua trascrizione comincia, ma soltanto un inizio su dieci viene terminato, e dà origine ad un trascritto genomico, tutti gli altri inizi di trascrizione abortiscono, cioè vi è una terminazione prematura della trascrizione e per questo sono assolutamente non funzionali all'espressione genica del virus, quindi la trascrizione è molto inefficiente.
Tat - Trans-Activator of Transcription (14-16kDa)
C N terminal Cysteine rich Core Basic C terminal K ------- RGD RNA binding in vitro Stimulation of transcription "activation domain" ₭ NLS The Tat protein is made from several different, multiply spliced mRNAs and therefore varies in length at its C terminus. The regions of the protein are named for the nature of their sequences (basic, cysteine rich) or greatest conservation among lentiviral Tat proteins (core). Experiments with fusion proteins containing various segments of Tat and a heterologous RNA-binding domain identified the N-terminal segment as sufficient to stimulate transcription. The basic region, which contains the nuclear localization signal (NLS), can bind specifically to RNA containing the bulge characteristic of TAR RNA. However, high-affinity binding, effective discrimination of wild-type TAR from mutated sequences in vitro, and RNA-dependent stimulation of transcription within cells require additional N-terminal regions of the protein, shown by the dashed arrow. TAT interacts with the ciclina T1/cdk9 complex through the cysteine rich domain. From Flint et al. Principles of Virology (2015), ASM Press
Quindi siamo in una cellula che dal punto di vista proteico-virale contiene la proteina Nef (proteina accessoria trasportata nel virione), la trascrittasi inversa e l'integrasi hanno già svolto la loro funzione, la proteasi contenuta nel virione non ha, in questa fase, alcuna funzione (e sicuramente non è la proteasi del virione che ha questa funzione), altre proteine virali presenti all'inizio sono la vpr (proteina accessoria fondamentale per la formazione del complesso di pre-integrazione). Per il resto non ci sono altre proteine virali all'inizio; quindi, la trascrizione del DNA provirale è molto inefficiente. Quando viene trascritta una molecola di RNA genomico completa, essa андrà incontro a completa maturazione e darà origine ai messaggeri che verranno poi maturati e daranno le proteine tat, rev e nef. È fondamentale che venga prodotta la proteina tat, essa ha un ruolo fondamentale nell'assicurare un'efficiente trascrizione del DNA provirale, tanto che la proteina tat, una volta prodotta, essa fa sì che a ogni inizio di trascrizione poi di fatto corrisponda a una trascrizione di rna genomico completo.
Model for the stimulation of elongation by Tat and p-Tefb
CycT1 Super elongation complex Čdk9 pTefb CycTT Ćdk9 Tat Tat Nelf RNA pol Il Tar RNA Spt5 P C-terminal domain Cooperative binding to TAR of Tat and p-Tefb (via its cyclin T1 subunit) leads to phosphorylation (P) of the C-terminal domain of the largest subunit of RNA polymerase Il by the Cdk9 kinase subunit of p-Tefb. This enzyme also phosphorylates and inactivates negative regulators of transcriptional elongation (e.g., transcription elongation factor [Spt5] and negative elongator factor complex [Nelf]). Positive regulators of elongation, such as RNA polymerase Il elongation factor 2 (Ell2), are also recruited to form a super elongation complex. The net result is that transcriptional complexes become competent to carry out highly processive transcription. Adapted from M. Ott et al., Cell Host Microbe 10:426-435, 2011, with permission. From Flint et al. Principles of Virology (2015), ASM Press
Cosa è Tat? È una piccola proteina che possiede una serie di domini: un dominio N-terminale di trans-attivazione che attraverso alla generazione di mutanti puntiformi e/o delezioni è stato stabilito perchè abbia un'attività trans-attivante altamente efficiente e che discrimini le sequenze di RNA a cui si lega la proteina Tat. Tale dominio è seguito dal dominio di cisteine e il dominio core (il più stabile). Inoltre, è presente un dominio basico, in quanto Tat ha la capacità di legarsi a sequenze nucleotidiche (in particolare all'RNA). Attraverso il dominio basico si lega alla sequenza di RNA (mostrata in diapositiva) che è la prima sequenza che viene trascritta dall'RNA polimerasi II della cellula ospite. Una volta trascritta la proteina Tat, essa si lega alla sequenza Tar. Inoltre, verso il C-terminale c'è il dominio Rgd che è quello attraverso cui Tat è in grado di legarsi alle integrine.