Adsorbimento e scambio ionico nel suolo, Presentazione
Slide di Università su adsorbimento e scambio. La Pdf esplora i meccanismi di adsorbimento e scambio ionico nel suolo, analizzando l'influenza delle dimensioni delle particelle e delle cariche superficiali, utile per studenti universitari di Scienze.
Mostra di più18 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Adsorbimento e Scambio Ionico
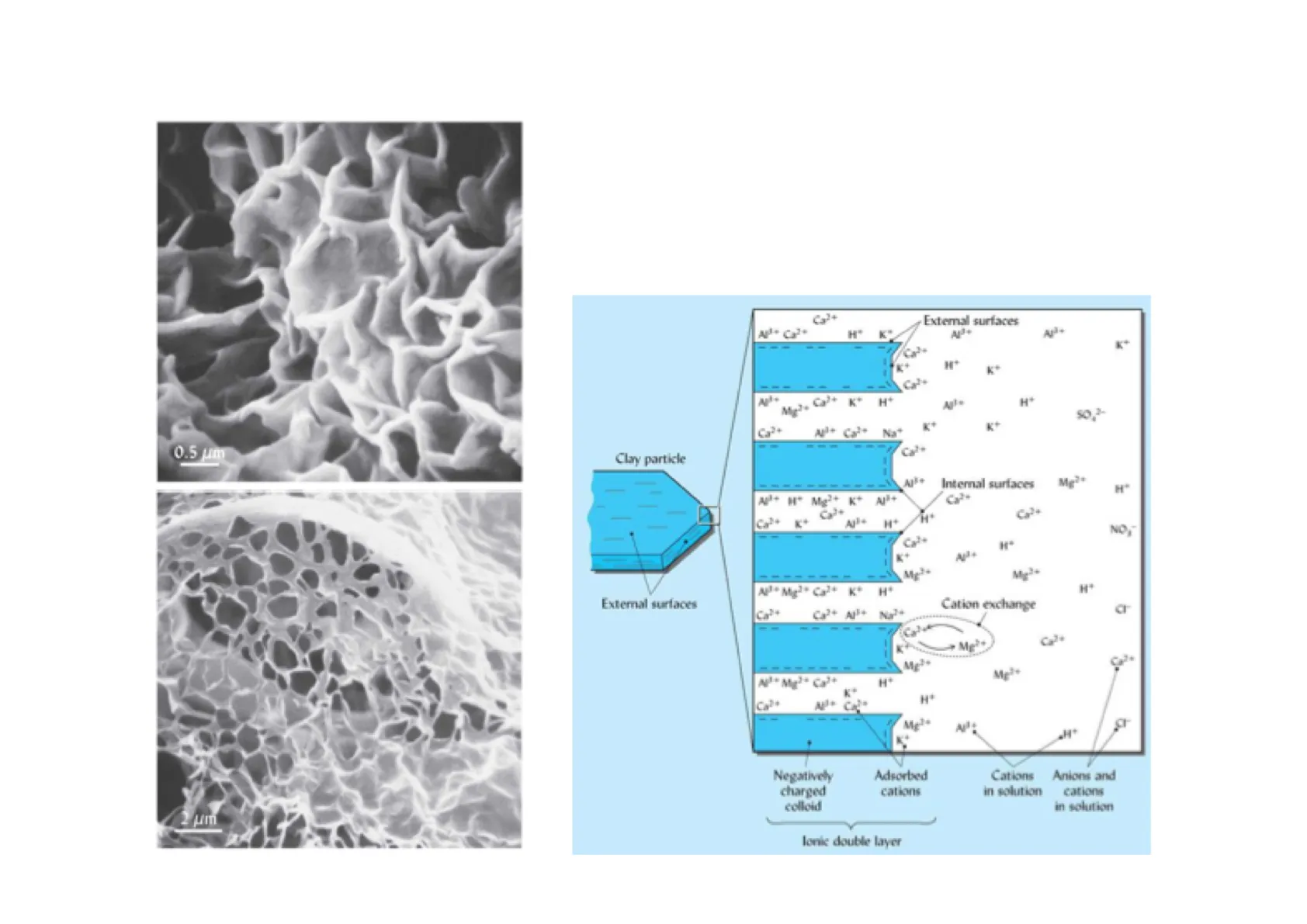
ADSORBIMENTO E SCAMBIO Ca2+ External surfaces NA* Ca2* H" All+ 1 - - -- K* --- Muže Ca2+ K* H+ H* Ca2+ A+ Ca2+ Na+ K+ K+ Clay particle Internal surfaces Mg2+ H" A+ H* Mg2+ ** All+ Ca2+ Ca2+ K+ H+ NO, - -- - H+ -- AJ+ Mg++ Mg2+ AP+ Mg2+ Ca2+ K* H* External surfaces Ca2+ Ca2+ All+ Na2+ Cation exchange 9 1 1 Cal* -------- Mg2+ A* Mg2* Ca2+ H* Ca2+ H* - Negatively charged colloid Adsorbed cations Cations in solution Anions and cations in solution lonie double layer . - - -- - H+ Ca2+ Mg++ Cal+ Cal 3 0.5 umIl suolo è un sistema eterogeneo con la fase solida formata da particelle minerali ed organiche.
Le dimensioni delle particelle influiscono significativamente sulle proprietà dei suoli: Suoli costituiti in maggioranza da particelle molto piccole (< 2 um) sono generalmente compatti e poco permeabili, con elevata ritenzione di acqua e di cationi Suoli costituiti in maggioranza da particelle > 50 um sono generalmente poco compatti e molto permeabili, con bassa capacità di ritenzione di acqua e di cationi.
L'estensione della zona di contatto tra la fase liquida e la fase solida del suolo è determinata dalla quantità di particelle con dimensioni minori ed è quindi condizionata dalla composizione granulometrica.
Dalla natura dei minerali presenti dipendono invece le cariche sulle superfici solide.
A seguito dell' interazione tra le due fasi, e a seconda delle caratteristiche della fase solida, quest'ultima è in grado di trattenere cationi (Ca2+, Mg2+, K+, Na+) ed anioni (H2PO3 ,HPO32-) presenti nella soluzione del suolo.I fenomeni fisico-chimici che avvengono nel sistemo solido-soluzione sono regolati dalle proprietà di superficie delle particelle di dimensioni inferiori a 1 um (alcuni autori pongono il limite a 2 um, limite dimensionale della frazione argillosa) che costituiscono la frazione colloidale del suolo.
Dimensioni delle Particelle e Proprietà del Suolo
Dispersione grossolana Dispersione colloidale Soluzione Dimensione delle particelle > 1000 nm 10-1000 nm < 10 nm Nº di atomi o molecole per particella > 109 103-109 1-103 Filtrabilità sempre solo con ultrafiltri mai Visibilità microscopio ottico microscopio elettronico mai nm = nanometri (10-9 mm)La frazione colloidale del suolo è costituita dai minerali argillosi (secondari) e dalle sostanze umiche, entrambi caratterizzati da dimensioni assai piccole.
Nel processo di formazione del suolo, i processi di alterazione fisica riducono la taglia dei minerali primari (da 2 - 0,2 mm a 50 - 2 um) che poi, grazie ai processi di alterazione chimica, verranno distrutti e/o trasformati in minerali secondari Le piccole dimensioni delle particelle fanno si che il rapporto superficie/massa sia particolarmente alto e, quindi, grande sia l'area superficiale esposta a fenomeni di adsorbimento, catalisi, precipitazione, colonizzazione microbica, ed altri fenomeni di superficie che avvengono nel suolo.
Tutti i colloidi del suolo posseggono una grande superficie specifica esterna (1000 volte superiore a quella delle particelle sabbiose). Alcuni minerali argillosi possiedono anche un'ampia area superficiale interna agli strati che costituiscono i cristalli (minerali 2:1).
La superficie specifica dei colloidi del suolo varia tra 10 m2/g e 800 m2/g.0.5 um 0.5 pm [a] [b] 0.5 um 2 um (c) Crystals of three silicate clay minerals and a photomicrograph of humic acid found in soils. (a) Kaolinite from Illinois (note hexagonal crystal at upper right). (b) A fine-grained mica from Wisconsin. (c) Montmorillonite (a smectite group mineral) from Wyoming. (d) Fulvic acid (a humic acid) from Georgia.Le particelle colloidali sono cariche elettricamente e possono attrarre, a secondo della loro carica, cationi o anioni, sottraendoli dalla soluzione del suolo.
Cariche Elettriche delle Particelle Colloidali
Le particelle del suolo hanno generalmente carica di superficie negativa a causa della presenza di ossigeno ed ossidrili sulla superficie dei costituenti minerali ed organici.
Le cariche negative attraggono le molecole di H2O presente nel suolo che tende a formare strati di spessore variabile sulle particelle, determinando una costante idratazione dei colloidi.
L'affinità tra l'acqua ed i colloidi è dovuta alla distribuzione asimmetrica degli elettroni nella molecola dell'acqua: l'atomo di ossigeno, fortemente elettronegativo, attrae gli elettroni degli atomi di idrogeno lasciandone parzialmente scoperti i nuclei e generando una molecola con una parziale carica negativa sull'ossigeno ed una parziale carica positiva sugli idrogeni. La carica positiva dell'acqua interagisce con la carica negativa dei colloidi.
La carica di superficie delle particelle del suolo è normalmente negativa e può modificarsi in relazione alle variazione del pH.
Carica negativa permanente: indipendente dal pH e determinata dalle caratteristiche del reticolo cristallino Carica variabile: subisce modificazioni al variare del pHCarica negativa permanente Non è influenzata dal pH, ma è funzione della natura e della struttura cristallina del minerale del suolo. Nei fillosilicati la carica negativa è dovuta alle sostituzioni isomorfe di ioni Si4+ con ioni Al3+, che avvengono nei reticoli cristallini dello strato tetraedrico, e di ioni Al3+ con ioni Fe2+ e Mg2+, che avvengono nello strato ottaedrico.
Le sostituzioni isomorfe comportano la diminuzione della carica positiva all'interno degli strati ed un aumento della carica netta della superficie dei fillosilicati.
- Sostituzioni isomorfe O 6 o o O O O Si AI Si Si AI Si HO 0 O. HO 0 Q HO O OH Al. Al Mg Al Fe Al: - OH o O OH O O HO O OH Al Si Si Al Si Si O C O O O O - - - - -- AIL'origine di tali cariche è riconducibile, nei minerali argillosi - a scompensi di carica determinati dalle sostituzioni isomorfe e, in misura minore, alla dissociazione dei gruppi -OH di bordo. nell'humus - alla dissociazione dei gruppi carbossilici e, in misura minore, dei gruppi fenolici.
La densità delle cariche elettriche negative dipende essenzialmente da due fattori: natura delle cariche e pH.
In relazione alla natura delle cariche, la densità è relativamente bassa se queste sono originate prevalentemente dall'interruzione dei reticoli cristallini (es. caolinite), è mediamente alta se sono originate da un elevato numero di sostituzioni isomorfe silicio- alluminio (es. montmorillonite), è molto alta se sono originate dalla dissociazione ionica di gruppi funzionali organici (es. humus).Carica variabile o pH dipendente Presente nei fillosilicati, ossidi di Fe, Al e Mn, silicati a scarso ordine cristallino (allofane e imogolite) e nelle sostanze umiche.
La carica variabile è influenzata da pH con meccanismi diversi: 1) Nei fillosilicati, la carica variabile è dovuta alla dissociazione o protonazione degli ossidrili che si trovano agli spigoli dei fogli tetraedrici ed ottaedrici. Solo il 5-10% della carica negativa nei fillosilicati 2:1 è pH-dipendente (maggior numero di sostituzioni isomorfe), mentre raggiunge il 50% nei fillosilicati 1:1 (Kaolinite) 2)Nei minerali non silicatici la carica è influenzata dalla dissociazione o protonazione degli ossidrili coordinati direttamente con i metalli. Gli ossidi di Al e Fe hanno carica negativa a pH basici, molto bassa o nulla a pH prossimi alla neutralità, e positiva a pH acidi. 3) Nelle sostanze umiche la carica negativa è dovuta soprattutto alla dissociazione o alla protonazione dei gruppi funzionali acidi (carbossilici e fenolici). A valori normali di pH (4-9) presentano solo cariche negative.
0 Large complex organic humus molecule consisting of chains and rings of mainly carbon and hydrogen atoms O OH OH Carboxylic group OH C O OH,+ O C Phenolic hydroxyl group Alcoholic hydroxyl groupLa carica netta di una particella soggetta a cariche pH dipendenti può cambiare, da positiva a negativa, all'aumentare del pH. Vi sarà un valore di pH in cui la carica netta della particella sarà pari a zero. Questo valore di pH è indicato come PUNTO DI CARICA ZERO (PZC).
+ -OH2+ PZC -OH- - € - - - PH acido PH alcalino - In generale, i silicati hanno una carica netta negativa anche in soluzioni molto acide ed attraggono quindi i cationi, mentre gli ossidi ed ossidi idrati di alluminio e di ferro, possono essere carichi sia positivamente che negativamente.
Punto di Carica Zero (PZC) e Ioni
PZC Quarzo 2-3 Smectite 2.5 Caolinite 4.6 Ossidrossidi di Fe 7-10 Ossidrossidi di Al 6-7.5 Sostanze umiche <4.5 Range di pH del suolo: 4-9La presenza nel suolo di colloidi con carica principalmente negativa comporta che gli ioni di segno opposto presenti nella fase liquida vengano attratti dalla fase solida e si dispongano nella zona di interfaccia solido-liquido.
L'interazione tra ioni in soluzione e superfici comporta che la concentrazione degli ioni rispetto alla superficie del colloide vari in dipendenza di due parametri: Densità di carica della superficie del colloide Densità di carica dello ione idrato (che dipende dal rapporto tra carica dello ione e raggio ionico).
Da non dimenticare che le cariche superficiali dei colloidi attirano anche le molecole d'acqua e quindi i colloidi tendono ad essere fortemente idratati e circondati da vari strati di molecole d'acqua.
lone Raggio ionico (pm) Energia di idratazione (Kcal/mol) Li+ 68 120 Na+ 97 100 K+ 133 85 Mg2+ 66 430 Ca2+ 99 373 Ba2+ 134 320Come si dispongono i diversi cationi rispetto alla superficie del colloide?
Modello del Doppio Strato Diffuso
- + + + - + + + - + + - + + - - + - + - - + - + + + + + + - - + + + - + - - + + - + - - + - + W+ 0 Strato di Stern Strato diffuso di Gouy distanza Modello del doppio strato diffuso E' formato da due strati: il primo è costituito da uno strato di controioni "adsorbiti" sulla superficie del solido (strato di Stern) ed il secondo dallo strato diffuso della soluzione (Strato di Gouy). Nel primo strato, il potenziale elettrico della superficie decresce linearmente con l'aumentare della distanza, mentre nello strato diffuso il potenziale ha valori più bassi e si riduce in modo esponenziale fino a coincidere con quello della soluzione (\ = 0).
Questo modello tiene in considerazione che gli ioni possano interagire con le superfici dei colloidi con diversi gradi di affinità in relazione al loro grado di idratazione. Cationi con elevata densità di carica e poco ingombranti (meno idratati) tendono a disporsi nello strato di Stern, mentre cationi con minore densità di carica e più idratati tendono ad occupare lo strato diffuso.
- + + + + + - + - - + + - - + - - +