Traffico vescicolare e controllo qualità proteine in Biologia
Documento di Università sul Traffico Vescicolare. Il Pdf, un approfondimento di Biologia, descrive il traffico vescicolare, la glicosilazione e il controllo di qualità delle proteine, con un focus sul meccanismo di selezione e trasporto tramite il complesso COP II.
Mostra di più15 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Traffico Vescicolare
Precedentemente:
- Abbiamo iniziato a parlare della via secretoria;
- Abbiamo visto il ruolo che ha il reticolo endoplasmatico nelle regioni ruvide nell'ambito della via secretoria;
- Abbiamo capito che se guardiamo dalla prospettiva delle proteine che devono raggiungere gli organelli della via secretoria che maturano all'esterno della cellula, il punto di partenza è il proprio reticolo.
Il 90-95% delle proteine della via secretoria entrano co-traduzionalmente, grazie alla presenza di un segnale idrofobico all'Nterminale. La particella SRP, aiutata da un complesso traslocatore (anche noto come traslocone sec61) permette questo passaggio.
Il ruolo del reticolo non è solo quello di compiere la sintesi e la traslocazione di queste proteine, ma rappresenta proprio l'ambiente cellulare in cui queste proteine dovranno acquisire la propria conformazione matura. Questo processo è favorito dal fatto che nel reticolo endoplasmatico abbiamo tanti chaperon e anche tante attività enzimatiche, come quella compiuta dell'enzima disolfuro isomerasi, che favorisce la formazione dei ponti disolfuro, che serviranno proprio a stabilizzare la struttura tridimensionale di alcune proteine.
Quindi, nel reticolo queste proteine prima acquisiscono la loro conformazione matura, poi si ripiegano, si formano legami tra diverse catene polipeptidiche e poi vanno incontro a diverse modifiche post-traduzionali. Tra le più importanti, troviamo la N-glicosilazione, che consiste nell'aggiunta di un oligosaccaride composto da 14 zuccheri, che verranno però rimossi all'interno del reticolo. Precisamente, il 3-glucosio viene rimosso da enzimi come le glucosidasi, e il mannosio da parte di enzimi mannossidasi. Sono proprio queste due modifiche a carico di questo modellamento della catena N-oligosaccaridica che permettono l'uscita dal reticolo endoplasmatico.
Dopo che le proteine sono state sintetizzate e hanno acquisito il loro giusto ripiegamento, possono uscire dal reticolo se il loro ruolo deve essere svolto in altri ambienti cellulari.
In realtà la glicosilazione ha un ruolo fondamentale e non è solo una modifica post-traduzionale, in quanto, analizzando le proteine della via secretoria, quasi tutte risulteranno glicosilate. I ruoli più importanti di questo processo sono quelli di riconoscimento, segnale antigenico e protezione, con una funzione diretta. La glicosilazione oltre al suo ruolo diretto ne ha anche un altro, che è quello di fare il controllo di qualità.
La N-glicosilazione avviene nel reticolo endoplasmatico a carico delle proteine della via secretoria e ha un ruolo cruciale nel controllo qualità delle proteine stesse. Il termina "quality control", significa proprio controllare la qualità delle proteine, e quindi il loro ripiegamento. È stato sperimentalmente evidenziato in una serie di prove che soltanto le proteine ben ripiegate riescono a muoversi all'interno della cellula, ed entrare quindi in quella vescicola che deve gemmare dal reticolo endoplasmatico per raggiungere il Golgi. La via secretoria rappresenta un quarto di tutto il proteoma cellulare.
Fondamentali nel controllo qualità sono appunto gli chaperon, che non solo servono proprio ad aiutare il ripiegamento, ma hanno un altro ruolo fondamentale: sono i primi sensori di un cattivo ripiegamento. Quando si legano alla proteina perché riconoscono il cattivo ripiegamento, la vanno a bloccare nel reticolo e le danno il tempo di ripiegarsi.Ogni chaperon riconosce il cattivo ripiegamento, chiaramente sempre sulla base di interazioni chimiche.
Chaperon Importanti
Alcuni chaperon importanti: calreticulina, calnexina e Herp57.
Herp57 è una proteina chaperon che riconosce i punti disolfuro. Ognuna va a riconoscere parte della proteina che serve poi a determinare il corretto ripiegamento. Calreticulina e calnexina possono fare il loro controllo di qualità solo se i tre glucosi terminali sono stati eliminati. Quindi, la glicosilazione che avviene nel reticolo può essere utilizzata da questi chaperon per capire se la proteina è correttamente ripiegata.
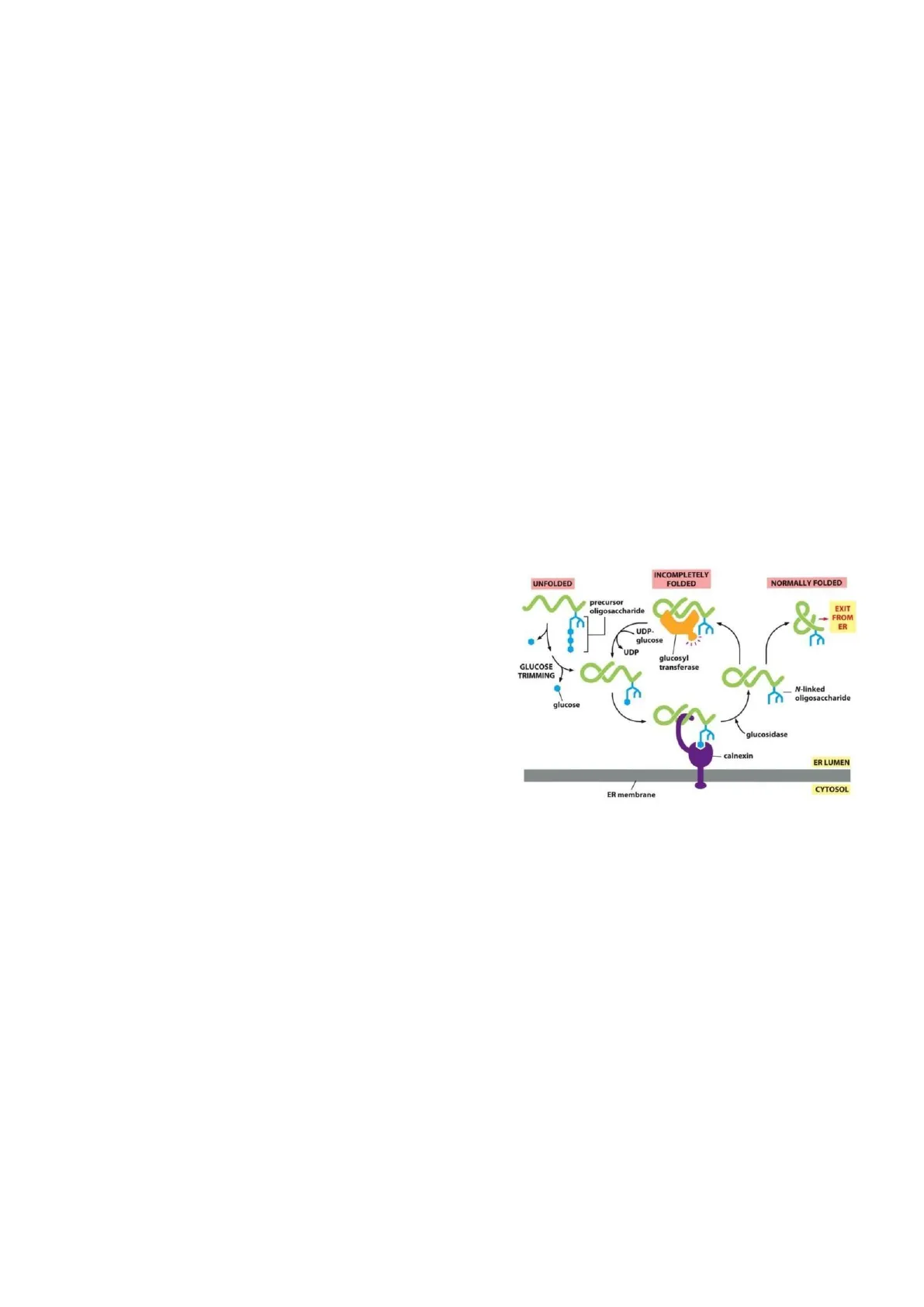
Quando l'oligosaccaride si aggiunge alla proteina, prima ci sono le glucosidasi che tagliano il glucosio e se la proteina si è ripiegata bene, avverrà anche il taglio del mannosio. Successivamente viene impacchettata ed esce dal reticolo per entrare nelle vescicole di gemmazione.
Se invece è mal ripiegata, subentra un altro enzima, il glucosil-trasferasi, che trasferisce un glucosio: questa proteina trasferisce un glucosio solo alle proteine mal ripiegate, perché quella catena oligosaccaridica è più accessibile e riconosce regioni della proteina che non dovrebbero essere esposte. L'aggiunta di questo glucosio forma uno stato intermedio della proteina ancora non ben ripiegata, che avrà questo però un glucosio legato, così che possa essere riconosciuto da Calnexina, e Calreticulina.
Differenza tra Calnexina e Calreticulina
Qual è la differenza tra Calnexina e Calreticulina? Calnexina è una proteina transmembrana, mentre calreticulina è una proteina chaperon solubile, quindi luminale, non ancorata alla membrana. Entrambe hanno un dominio, detto lectimico, capace di riconoscere le proteine mal ripiegate legate al glucosio.
Inoltre, sono proteine calcio-dipendenti: il legame di queste proteine al calcio le rende efficienti.
Riconoscono quel glucosio terminale che è presente nelle proteine mal ripiegate, e così riescono a legarsi ad esse. Successivamente, la bloccano nel reticolo grazie ad una porzione di regione proteica, la Calnexina ne aiuta il ripiegamento.
INCOMPLETELY FOLDED NORMALLY FOLDED precursor oligosaccharide & EXIT FROM ER UDP- glucose UDP glucosyl transferase GLUCOSE TRIMMING N-linked oligosaccharide glucose glucosidase calnexin ER LUMEN ER membrane CYTOSOL
Se la proteina, grazie all'aiuto di Calnexina o Calreticulina, si ripiega bene, allora può uscire dal reticolo perché ha ormai superato il controllo di qualità. Se invece non si riesce a ripiegare, potrà essere un potenziale prodotto del glucosil-transferasi e quindi il ciclo potrebbe ricominciare. Si è scoperto e si è capito che quella N-glicosilazione ha un ruolo importante come controllo di qualità, proprio perché l'aggiunta di quel glucosio è fondamentale per l'assunzione della giusta conformazione.
Portare avanti proteine mal ripiegate non solo non è utile per la cellula, ma può portare a gravi danni. Ad esempio, se un trasportatore di membrana non funziona, può causare la fibrosi cistica (che è dovuta a una delezione della fenilalanina). Nel caso del CFTR, la proteina non si conforma bene e rimane bloccata nel reticolo; non arriva proprio in membrana perché il reticolo, grazie al controllo di qualità, non la fa uscire.
UNFOLDED
Controllo Qualità nel Reticolo
Quando il reticolo è impegnato nel controllo qualità, come fa la cellula a capire quali sono le proteine mal ripiegate?
Nel passaggio da proteina non ripiegata a quella ripiegata, ci sono una serie di stati intermedi di ripiegamento, oltre a quelle che non si ripiegheranno più.
In inglese si utilizza il termine unfolded protein response, cioè la risposta alla proteina mal ripiegata, che può essere causata da un mal ripiegamento o da stress cellulare. In condizioni di stress, la cellula può attivare una serie di meccanismi di risoluzione, attivando quella che viene chiamata la UPR.
Se la proteina non si è ripiegata, non viene smaltita e non esce dal reticolo, ma viene attivato un meccanismo che la porta a sconfiggere questi mal ripiegamenti eccessivi. Se l'errore non può essere corretto, la cellula attiva un sistema di protezione per evitare l'accumulo di questa proteina, inducendo la sua morte tramite un processo di autofagia.
Ricapitolando: gli oligosaccaridi sono usati come etichette per indicare lo stato di ripiegamento delle proteine. Nel reticolo endoplasmatico, questo corretto ripiegamento è garantito da alcuni sistemi di controllo:
- Glicosilazione: le proteine neosintetizzate ricevono una catena di zuccheri tramite l'enzima glicosiltransferasi, che aggiunge residui di glucosio. Questi residui vengono poi riconosciuti dai chaperoni calnexina e calreticulina, che stabilizzano le proteine parzialmente ripiegate, favorendone il corretto ripiegamento.
- Rimozione mannosio: molte proteine traslocate nel RE non riescono a raggiungere il loro corretto stato ripiegato e vengono "retrotraslocate" indietro dal reticolo endoplasmatico al citosol, dove vengono riconosciute e distrutte. Dopo la glicosilazione, se la proteina non è correttamente ripiegata, intervengono le mannossidasi, che sono enzimi che rimuovono il mannosio residuo della proteina mal ripiegata. La rimozione del mannosio crea una nuova struttura oligosaccaridica che è riconosciuta da lectine del lume del RE appartenenti all'apparato della retrotraslocazione. Questo processo è un segnale che indica alla cellula che la proteina non è pronta per essere trasportata. Il mannosio rimosso serve quindi come indicatore per il sistema di qualità, favorendo il successivo riconoscimento della proteina da parte degli chaperoni e dei meccanismi di degradazione.
Stress del RE
Un accumulo di proteine ripiegate male nel reticolo endoplasmatico (RE) scatena un fenomeno noto come stress del reticolo endoplasmatico, che può avere gravi conseguenze per la cellula. Questo può verificarsi, ad esempio, in presenza di mutazioni nei geni che codificano i retrotraslocatori o componenti molecolari dei processi di controllo qualità. Tali situazioni portano a un aumento eccessivo di proteine mal ripiegate.
Questo accumulo attiva una risposta alle proteine non ripiegate (UPR: Unfolded Protein Response), che comprende:
- Un aumento della trascrizione di geni che codificano proteine coinvolte nella retrotraslocazione e nella degradazione proteica nel citosol.
- L'induzione di molecole chaperone e altre proteine che contribuiscono ad aumentare la capacità di ripiegamento delle proteine.
- Un'attenuazione della sintesi proteica tramite il blocco della traduzione.
Vie di Segnalazione tra RE e Nucleo
Le proteine ripiegate male nel citosol o nel RE mandano segnali al nucleo tramite tre vie parallele: IRE1, PERK e ATF6.
Via IRE1
Quando nel RE si accumulano proteine mal ripiegate, una proteina chinasi chiamata IRE1 si attiva tramite oligomerizzazione e autofosforilazione. Questa attivazione permette al suo dominio endoribonucleasico di eliminare un introne specifico da un RNA. Questo rappresenta un caso particolare di splicing che avviene nel citosol, invece che nel nucleo. I due frammenti di RNA vengono poi riuniti da una ligasi, creando un mRNA tradotto in una proteina attiva. Tale proteina stimola la trascrizione di geni coinvolti nella risposta allo stress del RE.
Via PERK
Anche una seconda chinasi transmembrana del RE, PERK, viene attivata dalle proteine mal ripiegate. Una volta attivata, PERK inibisce un fattore di inizio della traduzione tramite fosforilazione, riducendo così la produzione di nuove proteine in tutta la cellula.
Parallelamente, PERK fosforila alcuni fattori di trascrizione che promuovono la trascrizione di geni codificanti chaperoni molecolari e altre proteine necessarie per affrontare lo stress del RE.
Via ATF6
ATF6 è inizialmente una proteina di membrana del RE. Quando si accumulano proteine ripiegate male, ATF6 viene trasportata nell'apparato del Golgi, dove specifiche proteasi tagliano il suo dominio citosolico. Questo dominio libero migra nel nucleo e attiva la trascrizione di geni che codificano proteine utili per affrontare lo stress del RE.
Equilibrio e Apoptosi
L'importanza relativa di ciascuna delle tre vie di risposta allo stress (IRE1, PERK e ATF6) varia a seconda del tipo cellulare, consentendo un adattamento specifico alla situazione. Tuttavia, se lo stress persiste e l'equilibrio fisiologico non viene ripristinato, la cellula può attivare segnali di apoptosi, portando alla propria morte.
Implicazioni Generali
La ridondanza dei meccanismi di risposta (la presenza di più proteine con funzioni simili) è fondamentale per affrontare lo stress e ripristinare l'omeostasi cellulare. Tuttavia, il mal ripiegamento delle proteine compromette gravemente la funzionalità cellulare, causando potenziali danni a livello dell'intero organismo. Ad esempio, nei tumori, l'organismo può entrare in uno stato di cachessia, in cui le cellule muscolari perdono proteine e diventano incapaci di contrarsi.
Traffico dal RE al Golgi
Le proteine ben ripiegate, che non devono svolgere la loro funzione nel RE, proseguono lungo una via che comprende come seconda tappa obbligata il Golgi. Per arrivarci, devono essere impacchettate in vescicole che gemmano dal RE.