I derivati degli acidi carbossilici, alogenuri acilici e anidridi
Slide dall'Università San Raffaele sui derivati degli acidi carbossilici, alogenuri acilici e anidridi. Il Pdf illustra reazioni chiave come alcolisi, amminolisi e riduzione, con dettagli su formule chimiche e reagenti, per lo studio della chimica organica a livello universitario.
Mostra di più19 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Università San Raffaele Roma
Professore Gilda Aiello
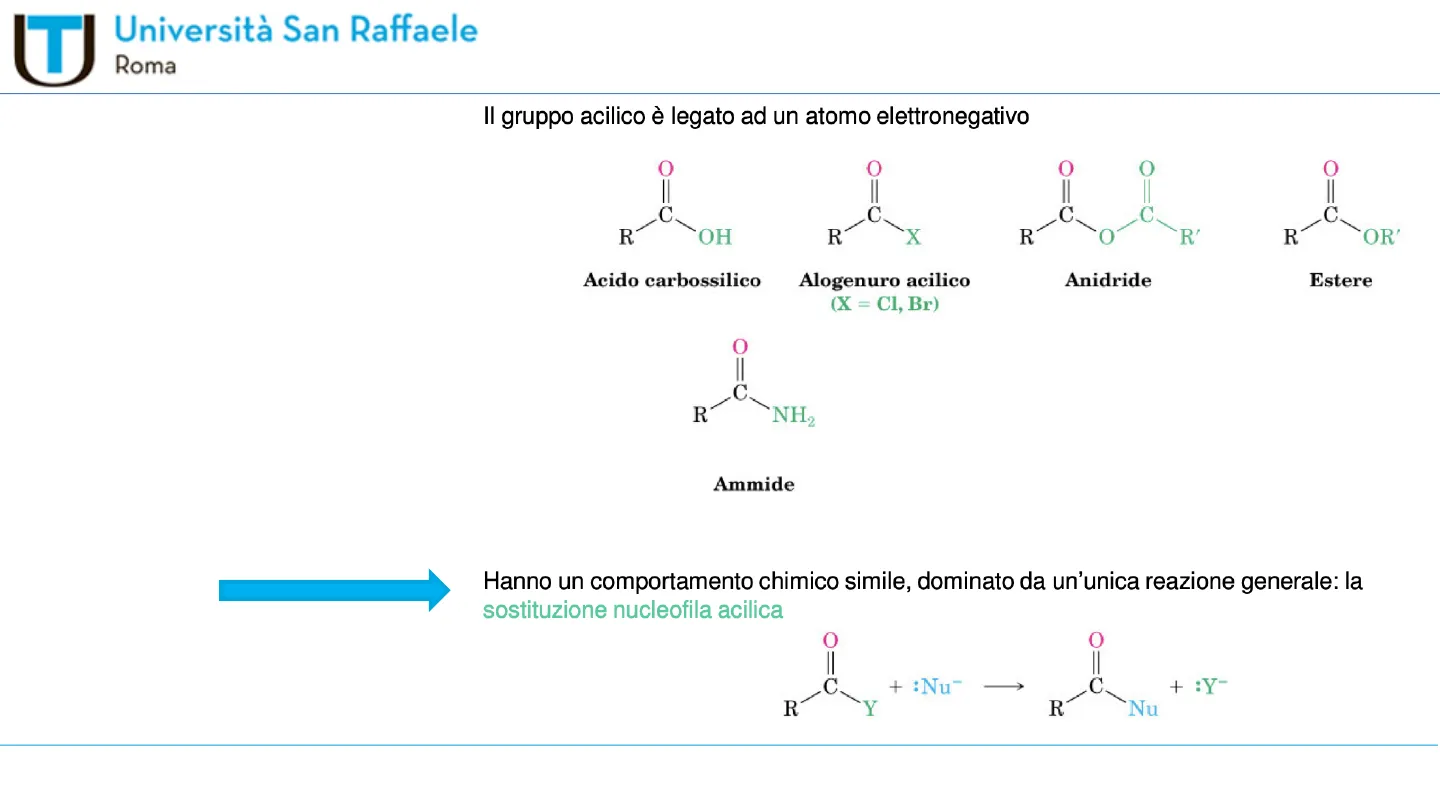
I derivati degli acidi Carbossilici A partire dagli acidi carbossilici, con reagenti adeguati, si ottengono diversi derivati, tutti caratterizzati dalla presenza del gruppo acilico -RCO. Il gruppo acilico è legato ad un atomo elettronegativo
O O O O O .C. R OH R X Acido carbossilico Alogenuro acilico (X = Cl, Br) Anidride Estere O II .C. R NH2 Ammide Hanno un comportamento chimico simile, dominato da un'unica reazione generale: la sostituzione nucleofila acilica
O 0 II C. + : Nu" C + :Y- R Y R Nu II .C. C. .C. R O R' R OR' I derivati degli acidi carbossilici, alogenuri acilici e anidridi 2 di 19
Sostituzione Nucleofila Acilica
Meccanismo Generale
MECCANISMO: Meccanismo generale di una rea- zione di sostituzione nucleofila acilica. Avviene l'addizione di un nucleofilo al gruppo carbonilico, con formazione di un intermedio tetraedrico.
+ :Nu"(o :Nu-H) .C R Y : 0: 5 C Nu YJ Una coppia di elettroni dell'ossigeno sposta il gruppo uscente Y, generando come prodotto un nuovo composto carbonilico.
> 0 II C + :Y- R Nu Y è un gruppo uscente: -OR,-NR2,-CI I derivati degli acidi carbossilici, alogenuri acilici e anidridi 3 di 19
Nota Bene: Attacco Nucleofilo
NOTA BENE: L'attacco nucleofilo ha un esito diverso che per aldeidi e chetoni
Gruppo uscente O C R Y Derivati degli acidi carbossilici Gruppo NON uscente - O 0 C C R H R R Aldeide Chetone I derivati degli acidi carbossilici, alogenuri acilici e anidridi 4 di 19
Reattività dei Derivati Carbossilici
Fattori Sterici
Alla velocità di reazione contribuiscono fattori sterici ...
0 O O 0 II II I R. C. R .C R H. C. 3 C V < < C R R R H H H H H Meno reattivo Reattività Più reattivo
Fattori Elettronici
... e fattori elettronici
O II O IL 0 O O II II R-C-X R-C-O-C-R R-C-OR' R-C-NH2 alogenuro acilico anidride estere ammide composto più reattivo composto meno reattivo o= I derivati degli acidi carbossilici, alogenuri acilici e anidridi 5 di 19
Interconversione dei Derivati
Interconversione di derivati degli acidi carbossilici. Un derivato acilico più reattivo può essere convertito in uno meno reattivo, ma non vale il contrario.
Più reattivo O C R CI O O Cloruro acilico C C. R O R' O Anidride I .C. R OR' O Estere II C R NH2 Meno reattivo Ammide I derivati degli acidi carbossilici, alogenuri acilici e anidridi 6 di 19 Reattività
Reazioni Generali dei Derivati
Alcune reazioni generali dei derivati degli acidi carbossilici
O C R NH2 O Amminolisi C. C R OR' R H Alcolisi Riduzione R'OH [H] 0 O H2O O R'MgX C. C R `OH C R R Idrolisi Reazioni di Grignard I derivati degli acidi carbossilici, alogenuri acilici e anidridi 7 di 19 Ulteriore reazione R Derivato acilico O Ulteriore reazione NH3
Alogenuri Acilici
Nomenclatura
Nomenclatura: Prima il nome del gruppo acilico trasformando il suffisso -ico in -ile, seguito dal nome dell'anione alogenuro. Esempio: CH3CH2COCl = propanoile cloruro (o cloruro di propanoile).
- Sono i più reattivi tra i derivati degli acidi carbossilici
- Sono intermedi di sintesi, rari in natura
O CI CI Br C Cloruro di acetile cloruro di etanoile) Bromuro di butirrile (bromuro di butanoile) Cloruro di benzoile CI CI Cloruro di esandioile (Cloruro di adipoile) I derivati degli acidi carbossilici, alogenuri acilici e anidridi 8 di 19
Reattività degli Alogenuri Acilici
O C R NH2 O H H Il [H] \ / C. R OR' R H R OH NH3 Estere Aldeide Alcol 1º [H] O II H2O O R'MgX II R'MgX 1 C C R 'R' R OH Chetone Alcol 3º Cloruro acilico O R' R' .C. R OH C R CI Acido 0 Ammide C C. R'OH I derivati degli acidi carbossilici, alogenuri acilici e anidridi 9 di 19
Idrolisi degli Alogenuri Acilici
Ci >:0: :Ö :- :0: :Base O Il .. C + : OH2 C H C. + H C R Cl R +:0- R OH CI< O I H H Cloruro acilico Acido carbossilico Idrolisi poiché si forma HCI viene normalmente aggiunta una base come piridina che sottragga acido e impedisca di formare reazioni secondarie I derivati degli acidi carbossilici, alogenuri acilici e anidridi 10 di 19 IL
Alcolisi degli Alogenuri Acilici
0 ǁ C OH C. Piridina O Benzoile cloruro Cicloesanolo Cicloesile benzoato (97%) Alcol primario (meno impedito e più reattivo) O O CH2OH -C. CH3 + -C. H3C HO HO Alcol secondario (più impedito e meno reattivo) Impedimenti sterici influiscono sulla velocità di reazione e possono essere sfruttati in sintesi complesse I derivati degli acidi carbossilici, alogenuri acilici e anidridi 11 di 19 O II C1 + Il Piridina O
Amminolisi degli Alogenuri Acilici
avviene con ammine primarie e secondarie ma non terziarie
0 (CH3)2CHCCI + 2 :NH3 0 II + > (CH3)2CHCNH2 + NHA CI 2-Metilpropanole cloruro 2-Metilpropanammide (83%) O 0 C-CI C-N(CH3)2 + + 2 : NH(CH3)2 > + NH2(CH3)2 Cl Benzoile cloruro N,N-Dimetilbenzammide (92%) I derivati degli acidi carbossilici, alogenuri acilici e anidridi 12 di 19
Riduzione degli Alogenuri Acilici
Agenti Riducenti
A seconda del reagente utilizzato danno aldeidi o alcoli 1° Agenti riducenti:
LiAIH4 エ ー H-AI-H + H Lİ idruro di litio e alluminio FORTE [(CH3)2 CHCH2]2AIH AI- H idruro di diisobutilalluminio (DIBAL-H) PIU' DEBOLE più ingombrato LiAIH[OC(CH3)2]3 0-4-I O-AI-O O H + Li idruro di litio tri-t-butossialluminio PIU' DEBOLE più ingombrato e meno nucleofilo I derivati degli acidi carbossilici, alogenuri acilici e anidridi 13 di 19
Reazioni di Riduzione
Alogenuri acilici:
1. LiAIH4 OH alcol 1° 2. H2O CI 1.LiAIH[OC(CH3)2]3, -78 ℃ O aldeide 2. H2O ... il gruppo uscente è CI- I derivati degli acidi carbossilici, alogenuri acilici e anidridi 14 di 19
Stadi della Riduzione
Primo stadio
O Co O + Z R Z R Z R H 0 + aldeide H3AI-H AIH3 N.B. : con i riducenti deboli la reazione si ferma qui!
Secondo stadio
0 C O C H-OH OH 0 R H R H + HO R H H H D + H3AI-H alcol 1º AIH3 non ci sono gruppi uscenti! I derivati degli acidi carbossilici, alogenuri acilici e anidridi 15 di 19 H
Le Anidridi
10 D R O R' IC R O-H H)-O R' Due molecole di acido condensate Se R = R' Anidridi semplici Se R # R' Anidridi miste Un po' meno reattive rispetto ai cloruri acilici Dopo gli alogenuri sono le più reattive tra i derivati degli acidi carbossilici Ø Sono intermedi di sintesi, rari in natura I derivati degli acidi carbossilici, alogenuri acilici e anidridi 16 di 19
Reazioni di SN Acilica delle Anidridi
Con Alcoli o Fenoli
Con alcoli (o fenoli) a dare esteri
O + OH O + OH O O + OH OH O O I derivati degli acidi carbossilici, alogenuri acilici e anidridi 17 di 19
Meccanismo delle Reazioni
Meccanismo
℮ O + + CH3OH R-C-OCOR + + R O R R OCH3 R O R OCH3 R OH OCH3 H H + OH OH O OH O O + + OH ASPIRINA I derivati degli acidi carbossilici, alogenuri acilici e anidridi 18 di 19
Con Ammoniaca o Ammine
Reazioni di SN acilica delle anidridi Con ammoniaca o ammine (primarie e secondarie) a dare ammidi
O + + 2 NH3 + O NH4 Meccanismo
℮ R-C-OCOR R-C-OCOR R NHCH3 R C R -Z + NHCH3 H @ CH3 CH3NH3 1 + CH3NH2 + R O CH3NH3 I derivati degli acidi carbossilici, alogenuri acilici e anidridi 19 di 19 + 2 CH3-NH2 NH2