Introduzione alle molecole organiche e ai gruppi funzionali
Slide di Università su Introduzione alle molecole organiche e ai gruppi funzionali. Il Pdf illustra le proprietà chimiche e fisiche delle molecole organiche, con un focus sui gruppi funzionali e la loro reattività, utile per lo studio della Chimica.
Mostra di più15 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Gruppi Funzionali
· Un gruppo funzionale è un atomo o un gruppo di atomi
con proprietà chimiche e fisiche tipiche. E' la parte
reattiva della molecola.
· La maggior parte delle molecole organiche hanno legami
C-C e C-H. Comunque, molte molecole organiche
hanno anche altre caratteristiche strutturali:
· Eteroatomi- Atomi diversi dal carbonio o idrogeno.
" Legami T - I legami T più comuni sono presenti nei
doppi legami C-C e C-O.
" Queste caratteristiche strutturali distinguono una
molecula organica da un'altra. Determinano inoltre la
geometria della molecula, le sue proprietà fisiche, la
reattività e includono quello che è chiamato gruppo
funzionale.· Gli eteroatomi e i legami « conferiscono reattività ad una
particolare molecola.
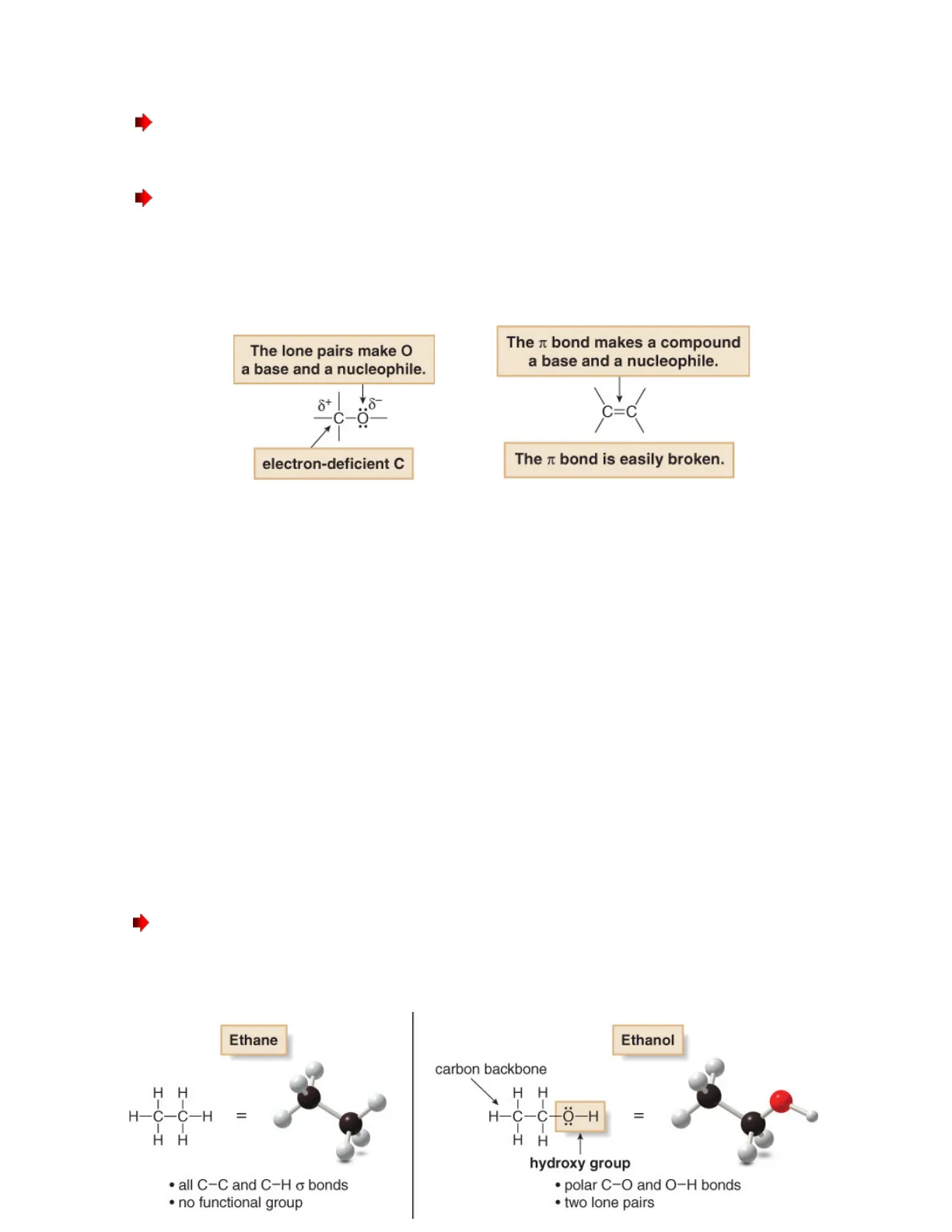
Gli eteroatomi hanno coppie solitarie e creano sul
carbonio siti carenti di elettroni.
> I legami T si rompono facilmente nelle reazioni chimiche.
Un legame it fa della molecola una base e un nucleofilo.
The lone pairs make O
a base and a nucleophile.
8+ 8
-C-O-
electron-deficient C
The x bond makes a compound
a base and a nucleophile.
C=C
The Tt bond is easily broken.
I legami C-C e C-H non sono privi di importanza. Essi
formano la spina dorsale carboniosa o lo scheletro al quale
sono legati i gruppi funzionali.
Esempi di Molecole
· Etano: Questa molecola ha solo legami C-C e C-H, quindi non
ha gruppi funzionali. L'etano non ha legami polari, nessuna
coppia solitaria, e nessun legame T, quindi non ha siti reattivi.
Per questi motivi, l'etano e molecole simili sono molto poco
reattive.
· Etanolo: Questa molecola ha un gruppo OH nel suo scheletro
carbonioso. Questo gruppo funzionale è chiamato gruppo
idrossi. L'etanolo ha coppie solitarie e legami polari che lo
rendono reattivo con una grande varietà di reagenti.
Il Gruppo funzionale idrossi rende le proprietà dell'etanolo
molto diverse da quelle dell'etano.
Ethane
エ ー
エ ー
H-C-C-H
=
H H
. all C-C and C-H o bonds
· no functional group
Ethanol
carbon backbone
HH
-
H-C-C-Ö-H
HH
hydroxy group
· polar C-O and O-H bonds
. two lone pairsGli idrocarburi sono composti costituiti solamente dagli elementi
carbonio e idrogeno. Possono essere alifatici o aromatici.
Tipi di Composti e Gruppi Funzionali
Type of compound
General structure
Example
Functional group
Alkane
R-H
CH3CH3
H
H
Alkene
C=C
C=C
double bond
1
1
H
H
Alkyne
-C=C-
H-C=C-H
triple bond
Aromatic compound
phenyl group
. Gli idrocarburi aromatici sono chiamati così perchè molti dei
primi composti aromatici conosciuti avevano un tipico odore
forte.
· L'idrocarburo aromatico più semplice è il benzene. L'anello a sei
termini e i tre legami Tt del benzene costituiscono un unico
gruppo funzionale.
· Quando un anello benzenico si lega a un altro gruppo, viene
chiamato gruppo fenile.
=
benzene
molecular formula C6H6
phenyl group
C6H5-
phenylcyclohexane
Type of compound
General structure
Example
3-D structure
Functional group
Alkyl halide
R-X:
CH3-Br:
-x
halo group
(X = F, CI, Br, I)
Alcohol
R-ÖH
CH3-ÖH
-OH
hydroxy group
Ether
R-Ö-R
CH3-Ö-CH3
-OR
alkoxy group
Amine
R-NH2 or
R2ÄH or R3Ñ
CH3-NH2
-NH2
amino group
Thiol
R-SH
CH3-SH
-SH
mercapto group
Sulfide
R-Š-R
CH3-§-CH3
-SR
alkylthio group
Esempi di Molecole con Legami C-Z
Esempi di Molecole contenenti legami o C-Z
OH
H
CH3CH2
CH2CH3
O
O
OH
diethyl ether
hemibrevetoxin B
Composti con Gruppo Carbonilico
Type of compound
General structure
Example
3-D structure
Functional group
:O:
:0:
Aldehyde
„C.
RUSH
I
CH3
H
C=0
carbonyl group
:O:
Ketone
„Č.
C
C.
CH3 CH3
C=0
carbonyl group
Carboxylic
acid
.C.
ÖH
CH5
-COOH
carboxy group
:O:
:0:
Ester
R-
ÖR
CH5
-ÖCH3
-COOR
:0:
:0:
-CONH2,
Amide
RÝ
.C .;; H (or R)
CH5
-CONHR, or
-CONR2
H (or R)
Acid
chloride
:O:
CH3 Či:
-COCI
Composti Contenenti il gruppo C=O:
· Questo gruppo è chiamato "gruppo carbonilico".
. Il legame polare C-O rende il carbonio carbonilico un
elettrofilo, mentre le coppie solitarie sull'O gli
permettono di reagire come un nucleofilo e come una
base.
. Il gruppo carbonilico contiene inoltre un legame î che
si rompe più facilmente di un legame o C-O.
Caratteristiche Reattive del Gruppo Carbonilico
Reactive features of a carbonyl group
lone pairs
:O:
easily broken Tt bond
.C.8+
electron-deficient C
C.
:0:
:O:
:O:
:O:
C-NH2Molecole Contenenti il Gruppo Funzionale C=O
Viracept
anti-HIV agent
aromatic ring
amide
sulfide
amide
S
O
HO
N
amide
H
OH
amine
+
alcohol
aromatic ring
alcohol
L
r
Proprietà Determinate dai Gruppi Funzionali
Un gruppo funzionale determina tutte le seguenti
proprietà di una molecola:
· Legami e forma
· Tipo e intensità delle forze intermolecolari
· Proprietà fisiche
· Nomenclatura
· Reattività chimica
Atenolol
antihypertensive agent
aromatic ring
ether
H2N
ZI
OH
amineForze Intermolecolari
Tipi di Interazioni Intermolecolari
· Ci sono diversi tipi di interazioni intermolecolari.
· I composti ionici contengono
particelle con carica di segno
opposto, tenute insieme da
interazioni elettrostatiche
estremamente forti. Queste
interazioni ioniche sono molto
più intense delle forze inter-
molecolari presenti tra le
molecole covalenti.
Interazioni ione-ione
+
+
I
I
++
-
+
+
+
+
-
+
-
+
+
+
+
+
strong electrostatic interaction
Forze Intermolecolari
· I composti covalenti sono costituiti da molecole distinte.
· La natura delle forze esistenti tra le molecole dipende
dal gruppo funzionale presente. Ci sono tre tipi diversi
di interazione, elencati di seguito in ordine di intensità
crescente:
· forze di van der Waals
· interazione dipolo-dipolo
· legame a idrogeno
Forze di van der Waals
Forze Intermolecolari-Forze di van der Waals
. Le forze di van der Waals sono anche chiamate di London.
· Sono interazioni deboli causate da variazioni momentanee nella
densità elettronica di una molecola.
. Sono le sole forze attrattive presenti in composti non polari.
Benché una molecola di
CH4 non abbia un dipolo
netto, in qualsiasi istante la
sua densità elettronica può
non essere completamente
simmetrica, creando un
dipolo temporaneo. Ciò può
indurre un dipolo
temporaneo in un'altra
molecola. Le interazioni
deboli di questi dipoli
temporanei costituiscono le
forze di van der Waals.
Interazioni van der Waals tra molecole di metano
8-
8+
8-
8+
5
8+
8-
8+
8
8+
8-
8+
8+
8
8+
Distribuzione di carica non simmetrica genera dipoli
temporanei
· Tutti i composti presentano forze di van der Waals.
· L'area della superficie di una molecola determina l'intensità
delle interazioni di van der Waals tra le molecole. Più l'area
della superficie è ampia, più la forza attrattiva tra due molecole
è estesa, e più le forze intermolecolari sono intense.
8+
8+
8
to
8
CH3CH2CH2CH2CH3
pentane
=
8+
8
CH3 CH3
8+ 8-
C-
CH3 CH3
neopentane
8+
8
smaller surface area
weaker van der Waals interactions
8
8
8
8-
8
A compact, spherical molecule
larger surface area
stronger van der Waals
interactions
to
8
8
8
to
8+
8
8+
8+
8+
8-
A long, cylindrical molecule
Interazioni Dipolo-Dipolo
Forze intermolecolari-Interazioni Dipolo-Dipolo
· Le interazioni dipolo-dipolo sono le forze di attrazione tra i
dipoli permanenti di due molecole polari.
· Nell'acetone i dipoli di molecole adiacenti si allineano in modo
tale che le cariche parzialmente negative e parzialmente
positive siano strettamente ravvicinate. Queste forze attrattive
causate da dipoli permanenti sono molto più forti rispetto alle
deboli forze di van der Waals.
CH3
C=Ö
=
8+ +
8+ +
8-
8+ +
8-
1
CH3
acetone
net attraction of permanent dipoles
Legame a Idrogeno
Forze intermolecolari-Legame a idrogeno
· Il legame a idrogeno tipicamente si verifica quando un
atomo di idrogeno legato a O, N, o F viene attratto
elettrostaticamente da una coppia solitaria di elettroni
su un atomo di O, N, o F di un'altra molecola.
8+
8+
H
1
N-O :-
=
-
-
H
8+
8+
Notare: all'aumentare della polarità di una molecola
organica,
aumenta
l'intensità
delle
sue
forze
intermolecolari.
Type of force
Relative strength
Exhibited by
Example
van der Waals
weak
all molecules
CH3CH2CH2CH2CH3
CH3CH2CH2CHO
CH3CH2CH2CH2OH
dipole-dipole
moderate
molecules with a net
dipole
CH3CH2CH2CHO
CH3CH2CH2CH2OH
hydrogen bonding
strong
molecules with an O-H,
N-H, or H-F bond
CH3CH2CH2CH2OH
ion-ion
very strong
ionic compounds
NaCI, LiF
Proprietà Fisiche
Punto di Ebollizione
Proprietà Fisiche-Punto di Ebollizione
· Il punto di ebollizione di un composto è la temperatura alla
quale un liquido si converte in fase vapore.
· Mentre il liquido bolle, serve energia per superare le forze
attrattive nello stato liquido più ordinato.
· Più intense sono le forze intermolecolari, più il punto di
ebollizione è alto.
· A parità di peso molecolare:
compounds with
van der Waals forces
compounds with
dipole-dipole interactions
compounds with
hydrogen bonding
Increasing strength of intermolecular forces
Increasing boiling point
Considerare l'esempio seguente. Ricordare che l'intensità
relativa delle forze intermolecolari aumenta dal pentano al
butanale, all'1-butanolo. I punti di ebollizione di questi
composti aumentano nello stesso ordine.
CH3CH2CH2CH2CH3
pentane
bp = 36 ℃
CH3CH2CH2CHO
butanal
bp = 76 ℃
CH3CH2CH2CH2OH
1-butanol
bp = 118 ℃
Increasing strength of intermolecular forces
Increasing boiling point
Con gruppi funzionali simili:
· Più estesa è l'area della superficie, più il punto di
ebollizione è alto.
· Più gli atomi sono polarizzabili, più il punto di
ebollizione è alto.
Punto di Fusione
Proprietà Fisiche-Punto di Fusione
· Il punto di fusione è la temperatura alla quale un solido
si converte nella sua fase liquida.
. Mentre fonde, serve energia per supeare le forze
attrattive presenti nel solido cristallino più ordinato.
· Più intense sono le forze intermolecolari, più il punto di
fusione è alto.
· Per uno stesso gruppo funzionale, più il composto è
simmetrico, più il punto di fusione è alto.
Solubilità
· La solubilità è la misura in cui un composto, chiamato
soluto, si scioglie in un liquido, chiamato solvente.
· Nel disciogliersi di
un composto,
l'energia necessaria
per rompere le
interazioni tra le
molecole o gli ioni
del soluto proviene
da nuove interazioni
tra il soluto e il
solvente.
solute
solvent
solute-solute interactions
new solute-solvent interactions
Energy comes from the new interactions
of the solute with the solvent.
· I composti si disciolgono in solventi che hanno gli stessi
tipi di forze intermolecolari.
· "Il simile scioglie il simile"
· Composti polari si sciolgono in solventi polari. Composti
non polari o debolmente polari si sciolgono in solventi
non polari o debolmente polari .