I legami chimici: formazione, ionici, covalenti e metallici
Slide da Adt sui legami chimici. Il Pdf esplora la formazione dei legami ionici, covalenti e metallici, le eccezioni alla regola dell'ottetto e le forze che tengono uniti gli atomi. Questo materiale di Chimica per la Scuola superiore è conciso e supportato da diagrammi esplicativi.
Mostra di più23 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Chimica
Formazione del legame chimico
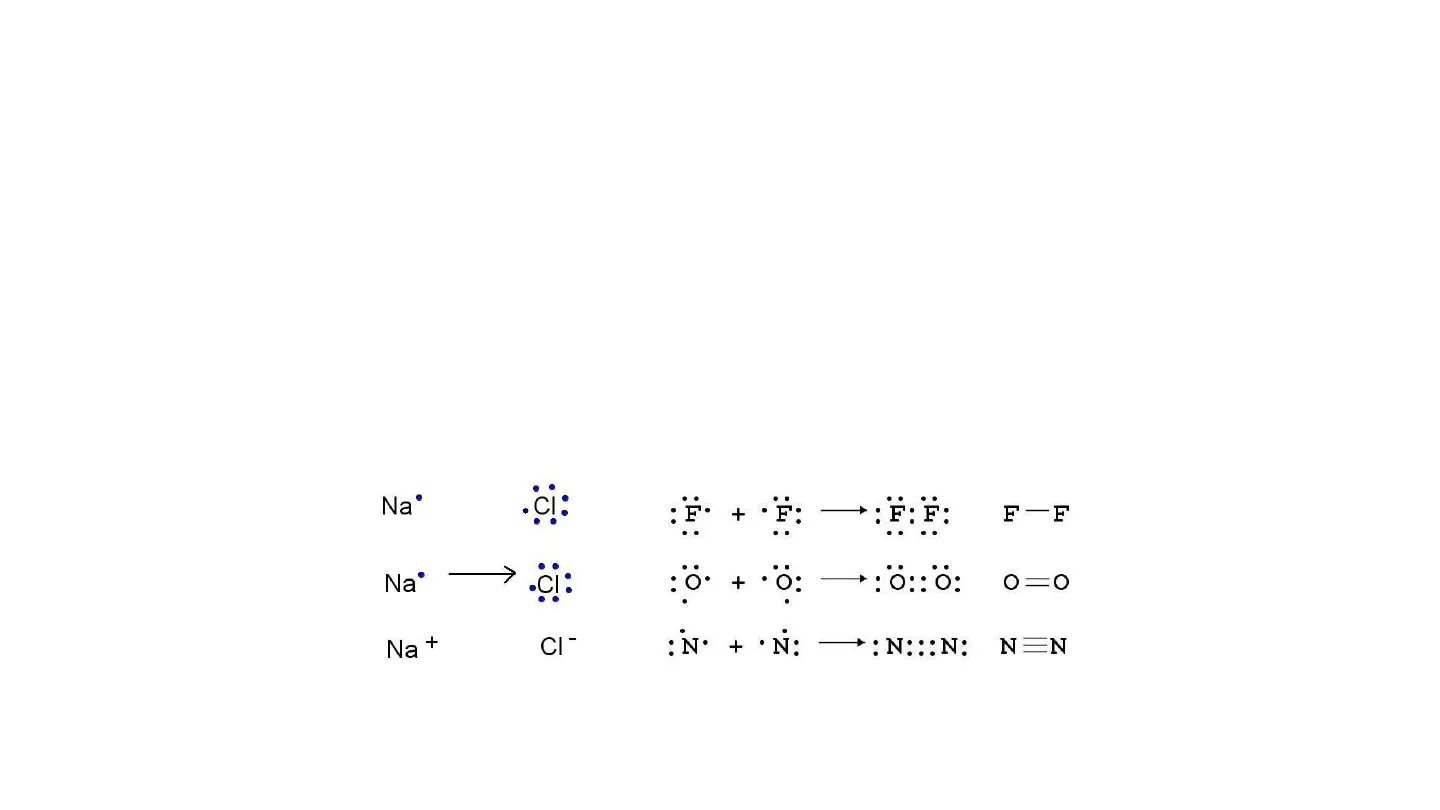
Con il termine legame si intendono le forze che tengono insieme atomi adiacenti. Quando tra due atomi avviene una reazione chimica, i loro elettroni di valenza si organizzano in maniera che una forza attrattiva netta - un legame chimico - si eserciti tra gli atomi. Ci sono tre tipi di legame: ionico, covalente e metallico. NB: la formazione dei legami è illustrata con i simboli di Lewis.
Na . CI: : F. F: F: F: F-F .. Na .ci: :9 *: 0 :: 0: 0=0 Na + CI- : N· + · N: - +: N ::: N: NEN +
Formazione del legame chimico (1916)
Nel 1916 il chimico statunitense G.B. Lewis formulò un modello capace di dare una spiegazione all'esistenza delle molecole. Secondo Lewis, gli atomi possono raggiungere la configurazione stabile tipica di un gas nobile sia scambiandosi elettroni, sia condividendoli.
CI + H - CI H- Simboli di Lewis
Gli elettroni presenti in un atomo possono essere divisi in due gruppi: elettroni di valenza e elettroni interni. Gli elettroni di valenza determinano le proprietà chimiche dell'atomo. Gli elettroni interni invece non sono coinvolti nel legame e nelle reazioni chimiche! Lewis introdusse una maniera utile per descrivere gli elettroni nel guscio di valenza di un atomo. I primi quattro elettroni di valenza, rappresentati da puntini, sono posti uno alla volta attorno al simbolo atomico; poi, se ci sono altri elettroni di valenza, questi vengono appaiati a quelli già presenti. Poiché questa configurazione comprende complessivamente otto elettroni, viene generalmente chiamata ottetto. Un ottetto di elettroni che circonda un atomo rappresenta una configurazione particolarmente stabile.
Gas nobili
I gas nobili, con l'eccezione dell'elio He, hanno otto elettroni di valenza e sono particolarmente poco reattivi (sono molto stabili).
D He Ne Ar Kr Xe Rn- La regola dell'ottetto regola i legami chimici
Nei legami rappresentati, tutti gli atomi (eccetto l'idrogeno) possiedono, comprese le coppie in condivisione, quattro coppie di elettroni; in questa maniera ogni atomo raggiunge una configurazione di gas nobile. Ogni atomo, infatti, è circondato da un ottetto di elettroni. La tendenza delle molecole e degli ioni poliatomici ad avere strutture in cui otto elettroni circondano ogni atomo è chiamata regola dell'ottetto. La regola dell'ottetto dice che, quando un atomo si combina con altri, raggiunge il massimo di stabilità scambiando o condividendo elettroni, in modo da conseguire una configurazione elettronica esterna a otto elettroni (o a due elettroni, nell'idrogeno) simile a quella del gas nobile più vicino nel sistema periodico.
: CI : Hº .Cl: H&.CI. . H:CI: . 0=c =° : CI : .. : CI : C : CI : . . . .- Eccezioni alla regola dell'ottetto
Nonostante la regola dell'ottetto sia un modello soddisfacente in grado di descrivere realisticamente il legame e la struttura di molti composti, ci sono delle eccezioni! Queste eccezioni includono:
- Molecole e ioni che hanno meno di quattro coppie di elettroni attorno all'atomo centrale. Il berillio Be, il boro B e l'alluminio Al tendono a formare composti in cui sono circondati da un numero di elettroni minore di otto. Questa situazione è detta ottetto incompleto. Es. BH3 H : B : H H- Eccezioni alla regola dell'ottetto
- Molecole e ioni che hanno più di quattro coppie di elettroni attorno all'atomo centrale. Gli elementi che appartengono al terzo periodo e oltre possono formare un ottetto espanso, con 10 o anche 12 elettroni attorno all'atomo centrale. Es. PCl5 :CI:- Eccezioni alla regola dell'ottetto
- Molecole e ioni che hanno un numero dispari di elettroni. A causa del numero dispari di elettroni non è possibile scrivere per queste molecole una struttura di Lewis che rispetti la regola dell'ottetto. Es. NO, con 17 elettroni di valenza -> anche se non rispetta la regola dell'ottetto per esso si può scrivere una struttura a punti che approssimi la situazione dei legami nella molecola. In questa struttura di Lewis l'elettrone spaiato è posto sull'azoto. Ö=N-O . . ·- Legame chimico
Quando due o più atomi formano un composto chimico, gli atomi sono tenuti insieme da forze attrattive in una disposizione spaziale caratteristica. Il legame chimico è la forza di attrazione tra gli atomi in un composto.
- Legame ionico
- Legame covalente
- Legame metallico
TYPES OF CHEMICAL BONDS Fis 1. Ionic VIA 9GAG.COM Fis 2. Covalent Fis 3. Metallic- Legame ionico
Un legame ionico si forma quando uno o più elettroni di valenza si trasferiscono da un atomo all'altro, creando ioni positivi e negativi. Non si verifica nessuna condivisione di elettroni! Il "legame" è la forza attrattiva tra gli ioni positivi e quelli negativi. Il legame ionico si ottiene quando la differenza di elettronegatività tra gli atomi è molto alta, superiore a 1,9.
CI Na+- Legame ionico
L'atomo più elettronegativo acquisisce l'elettrone e assume carica negativa, l'altro atomo che invece perde l'elettrone diventa carico positivamente. Tra i due ioni di carica opposta si instaura un'attrazione di natura elettrostatica. Es. quando Na e Cl reagiscono, un elettrone viene trasferito da un atomo di sodio a un atomo di cloro, per formare Na+ e Cl -. Na cede un elettrone e passa da [1s2 2s2 2p6 3s1] a Na+ con configurazione [1s2 2s2 2p6], equivalente alla configurazione del neon Ne. Cl acquista un elettrone e passa da {[Ne] 3s2 3p5] a Cl- con configurazione {[Ne] 3s2 3p6] equivalente alla configurazione di Ar.
+ Na C Na CI Na Sodium atom CI Chlorine atom Na+ Sodium ion (a cation) CI Chloride ion (an anion) Sodium chloride (NaCI)- Legame ionico: quali elementi lo instaurano?
Saranno preferiti gli elementi che si trasformano più facilmente in ioni: - elementi metallici del I, II e III gruppo che, avendo pochi elettroni, tendono a perderli diventando ioni positivi. Il catione che si forma ha la configurazione del gas nobile che lo precede! Es. Na [1s2 2s2 2p6 3s1] -> Na+ [1s2 2s2 2p6] : configurazione del Neon. - elementi non metallici del VI e VII gruppo che, avendone molti, tendono ad acquistarli diventando ioni negativi. L'anione che si forma ha la configurazione del gas nobile che lo segue! Es. Cl {[Ne] 3s2 3p5] -> Cl {[Ne] 3s2 3p6} : configurazione dell'Argon.
· Li · . Be · . B . · . C · . . 0 · . F · Ne. . . . .. .. . . . .. . .. .. Na . Mg . Al · . . Si . · . P .. S : CI .. · : Ar : . . .. .. .. .. · · ·- Legame covalente
Il legame covalente, al contrario del legame ionico, si instaura quando due atomi mettono in condivisione una o più coppie di elettroni di valenza, in modo tale che ciascuno degli atomi che partecipa al legame raggiunga l'ottetto. Inoltre, il legame covalente si instaura tra atomi con differenza di elettronegatività < a 1,9. Es. due atomi di cloro condividono una coppia di elettroni, un elettrone da ogni atomo, per formare un legame covalente.
.. .. .. .. : C1 . + · C1 : : CI : C1 : .. .. .. ..- Legame covalente: terminologia
I composti caratterizzati da legami covalenti sono detti composti covalenti (molecole).
F. + . F: .. +: FOF F-F .. La coppia di elettroni condivisa è detta coppia di legame. I restanti elettroni non condivisi che sono rappresentati attorno all'atomo di F sono detti coppie solitarie (o lone pairs).- Legame covalente omopolare ed eteropolare
:F. + .F: - .. .. F-F Legame covalente OMOPOLARE o PURO o APOLARE Gli atomi impegnati nel legame covalente sono atomi dello stesso elemento (molecole omonucleari). 8+ 0. 8+ 8+ 8+ 8+ 8 H:N : H H: O:H H: F: 8+H Legame covalente ETEROPOLARE o POLARE Gli atomi impegnati nel legame covalente sono atomi di elementi diversi (con differenza di elettronegatività < a 1,9).- Legame covalente singolo, doppio e triplo
Gli atomi possono mettere in compartecipazione una, due o tre coppie di elettroni: in questo caso parleremo rispettivamente di legame singolo, legame doppio e legame triplo.
-
:Ë:F: F-F
-
:0. + ·Ö: - :Ö :: Ö: 0=0
-
:Ń· + ·Ń: :NÊN: N=N- Legame covalente singolo, doppio e triplo
Stabilità del legame covalente
STABILITÀ DEL LEGAME La stabilità del legame è in relazione con l'energia del legame. legame triplo > legame doppio > legame singolo Dunque:
- la rottura di un legame triplo richiede un'energia maggiore di quella necessaria per rompere un legame doppio.
- a sua volta, la rottura di un legame doppio richiede più energia di quanta ne serva per rompere un legame singolo.
Lunghezza del legame covalente
LUNGHEZZA DEL LEGAME La lunghezza del legame è in relazione con la presenza (o l'assenza) di legami multipli. legame singolo > legame doppio > legame triplo Dunque:
- la distanza tra i nuclei è maggiore nel caso di un legame singolo, minore nel legame doppio e ancora minore nel legame triplo.- Legame covalente: legame dativo
Nella molecola di ammoniaca (NH2) l'azoto ha sei elettroni condivisi con i tre atomi di idrogeno e una coppia solitaria (lone pair): ha raggiunto l'ottetto! Siccome, però, un doppietto elettronico resta ancora disponibile può essere donato ad uno ione idrogeno che così raggiunge anch'esso l'ottetto (o più propriamente "duetto").
N: donatore H: accettore
+ H H:N: · H + H+ H · H:N: - > H+ .. H orbitale vuoto- Legame metallico
Gli atomi che costituiscono un metallo sono tenuti insieme da un tipo di legame chiamato legame metallico. Il legame metallico consiste in un'attrazione elettrostatica che si instaura tra gli ioni positivi metallici e gli elettroni delocalizzati che li circondano, liberi di muoversi in tutto il metallo.
O 0 + 0 + 0 + 0 + O + + + + O 0 O O + 0 + + 0 + -- Legame metallico: modello a nube elettronica
Il legame metallico può essere compreso mediante la teoria del modello a nube elettronica. Secondo questo modello all'interno di un metallo gli atomi perdono i loro elettroni di valenza trasformandosi in cationi. Gli ioni si dispongono secondo strutture geometriche ben definite. Gli elettroni di valenza diventano liberi di muoversi (elettroni delocalizzati) tra i vari cationi. Si può quindi immaginare un cristallo metallico come un reticolo costituito da ioni positivi immersi in una nube di elettroni mobili.
-
-
-
-
-
1 + + + Positive ions from the metal
-
-
-
-
-
1
-
-
-
-
-
+ + - + -
-
1
-
-
-
-
-
+ - + + -
-
-
-
-
-
Electron cloud that doesn't belong to any one metal ion