Biochimica della nutrizione: metabolismo e assorbimento di rame e ferro
Documento di Università su Biochimica della nutrizione. Il Pdf, utile per lo studio autonomo della biologia, esplora il metabolismo e l'assorbimento del Rame e del Ferro, evidenziando le differenze nei meccanismi di escrezione e trasporto.
Mostra di più24 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Biochimica della nutrizione
Lezione 6 - 17/02/2022
Livelli sistemici di Rame
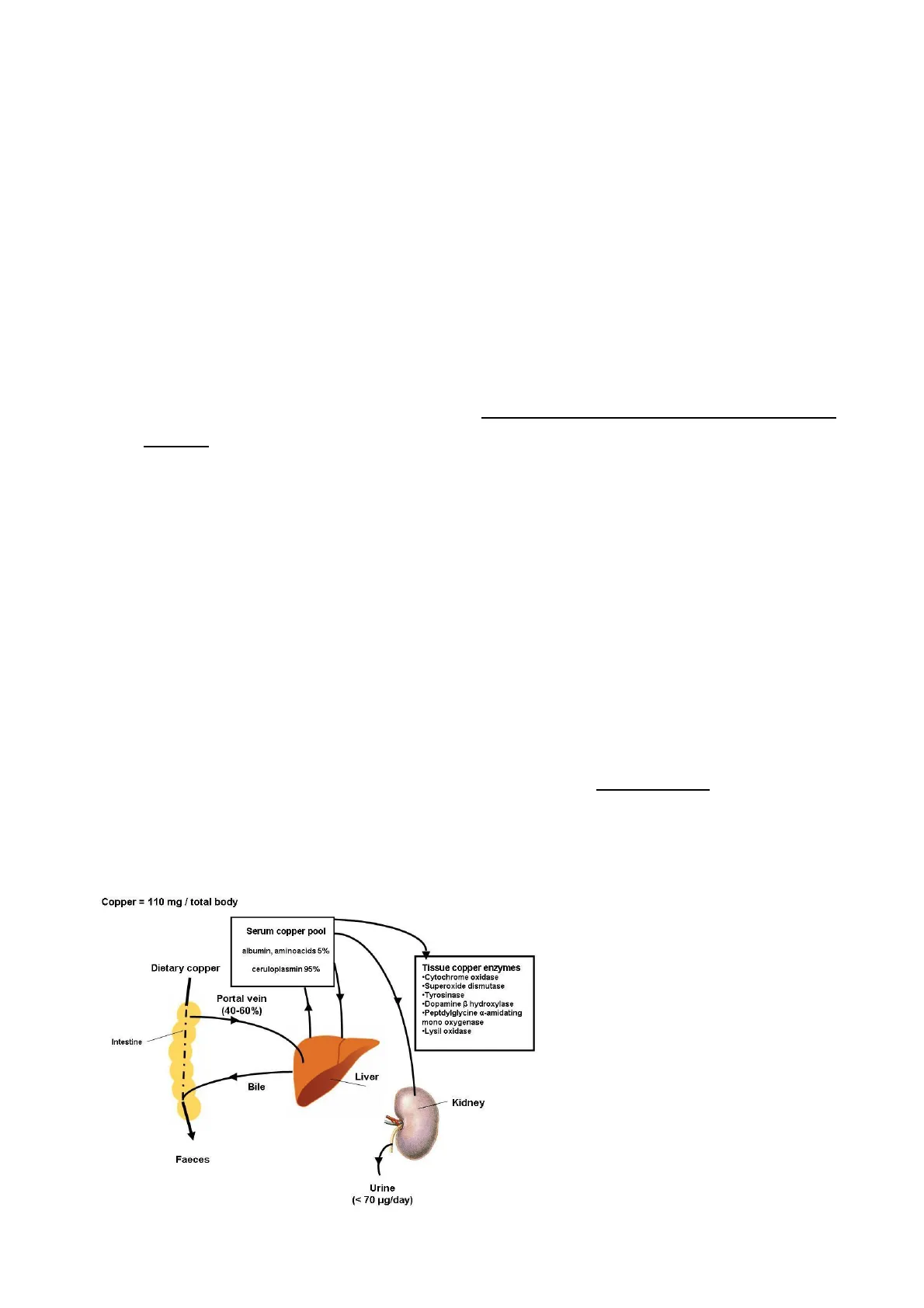
Il Rame ha concentrazioni molto più basse rispetto a quelle del Ferro. La sede principale maggiormente interessata nel metabolismo e nello smistamento di questo metallo è il Fegato:
- In questo organo è presente un sistema attivo di escrezione per il Rame; per cui quando il metallo raggiunge concentrazioni molto elevate, dal fegato viene indirizzato verso la cistifellea ed attraverso la bile viene rilasciato nell'intestino ed escreto con le feci.
La principale differenza tra il metabolismo del Rame e il metabolismo del Ferro sta proprio nel fatto che per il Rame è presente un sistema attivo di escrezione mentre per il Ferro non è presente. Le differenti concentrazioni del Rame e del Ferro all'interno dell'organismo sono dovute al fatto che il Ferro fa parte delle emoproteine, deputate al trasporto dell'ossigeno. Essendo infatti, il Ferro un elemento importante per il trasporto dell'ossigeno, vi è un controllo più forte che quindi non vede la presenza di sistemi di trasporto e di eliminazione attivi perché bisogna sempre assicurare la disponibilità del metallo per l'eritropoiesi. Per il rame è presente questo sistema che controlla le concentrazioni del metallo a livello epatico e che tende ad eliminarlo quando il metallo aumenta nell'organismo.
Copper = 110 mg / total body Serum copper pool albumin, aminoacids 5% Dietary copper ceruloplasmin 95% Tissue copper enzymes .Cytochrome oxidase .Superoxide dismutase .Tyrosinase Portal vein (40-60%) .Dopamine @ hydroxylase ·Peptdylglycine a-amidating mono oxygenase .Lysil oxidase Intestine Liver Bile Kidney Faeces Urine (< 70 µg/day)
Assorbimento del Rame
L'assorbimento avviene a livello dell'intestino tenue. Per il Rame sono stati identificati 2 trasportatori:
- Ctr-1 (Copper transport-1) [ trasportatore specifico per il Rame che
funziona da trasportatore per il Rame ridotto (Cu +1).
Visto che il Rame deve entrare nella forma ridotta, ci devono essere
sempre sulla membrana dell'enterocita dei sistemi di riduzione:
- STEAP 1,2: reduttasi specifica per il Rame.
- dCYTB (Duodenal): reduttasi che ha un ruolo sia nella riduzione del Rame sia del Ferro.
- DMT-1 (Divalent metal transport-1) I canale sia per il Ferro che per il Rame. Canale che trasporta metalli divalenti. Trasporta il Rame nella forma 2+.
A livello dell'intestino, i due metalli entrano in competizione; quindi se la concentrazione di uno dei due aumenta notevolmente, ne impedisce l'assorbimento dell'altro.
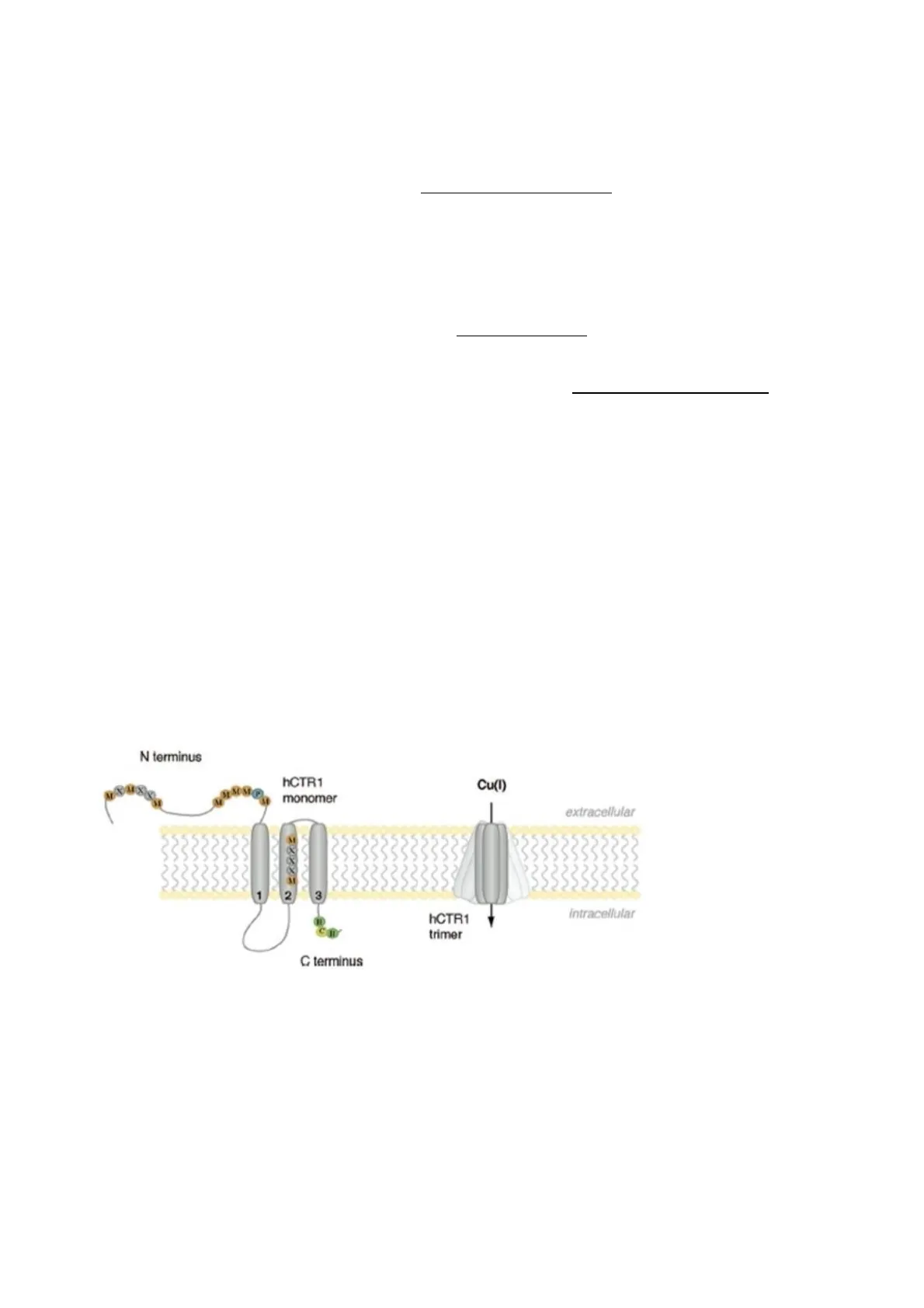
N terminus hCTR1 monomer Cu(I) extracellular 1 2 3 ® hCTR1 trimer Intracellular CO G terminus
Nell'immagine si osserva la struttura del trasportatore del Rame Ctr-1. E' una proteina integrale multipasso di membrana che attraversa tutta la membrana. All'interno della regione intramembrana sono presenti dei residui amminoacidici molto importanti che servono a legare ed a indirizzare il metallo verso il lato opposto della membrana. La regione N-terminale presenta diversi residui amminoacidici che legano il metallo per poi indirizzarlo verso l'interno del canale e quindi trasportarlo dall'ambiente extracellulare a quello intracellulare.
Destino intracellulare del Rame
Una volta che il Rame si trova all'interno della cellula, può intraprendere 4 differenti strade che possono dipendere anche dal tipo cellulare nel quale il Rame viene assimilato:
- Pathway citosolico I via citosolica che prevede il legame del metallo con gli enzimi a Rame (enzimi antiossidanti, chinasi, fattori di crescita, proteine di segnalazione e proteine strutturali).
- Pathway mitocondriale [ via mitocondriale che porta alla formazione della Citocromo ossidasi e quindi il complesso 4 della catena di trasporto degli elettroni. Il mitocondrio rappresenta anche una delle sedi principali di storage del Rame.
- Pathway di secrezione I via che porta alla sintesi di proteine plasmatiche che vengono sintetizzate a livello cellulare ma che poi svolgono la loro funzione a livello del plasma. Queste proteine vengono sintetizzate a livello del Reticolo Endoplasmatico, poi passano nel Golgi e poi vengono trasportate verso l'esterno. La via di secrezione serve sia per processi fisiologici per queste proteine, sia per la via di eliminazione del rame dalle cellule: processo che serve ad eliminare gli eccessi di Rame. Il processo di eliminazione avviene soltanto a livello delle cellule del fegato.
- Pathway di detossificazione I via che prevede lo smaltimento del Rame in eccesso. Rame che viene accumulato a livello dei lisosomi o delle metallotioneine (proteine a basso peso molecolare che possono legare diversi tipi di metalli; il più importante è lo Zinco).
Il rame all'interno della cellula, per evitare processi di ossido- riduzione con l'ossigeno, può essere complessato da amminoacidi o composti a basso peso molecolare tra cui il glutatione (tripeptide). Esso è un ottimo complessante del rame e lo rende in una forma non più reattiva nei confronti dell'ossigeno molecolare.
Chaperoni e Glutatione
Il Rame, una volta che è entrato attraverso il suo trasportatore principale (Ctr-1), viene legato o a complessi a basso peso molecolare (come il glutatione, sia nella forma ridotta che nella forma ossidata) oppure viene legato a chaperoni. Gli Chaperoni o GSH sono proteine che legano il Rame transitoriamente per poi destinarlo a proteine che usano il metallo come metallo strutturale. Il processo di legame del Rame al glutatione o agli chaperoni, serve sia per rendere specifico l'accettore del metallo, sia per evitare l'interazione dell'ossigeno con il metallo stesso. Rendere specifico perché il Rame può legarsi in maniera molto efficiente con tutta una classe di amminoacidi che si possono ritrovare su tutte le proteine mentre le proteine che usano il Rame come sito catalitico oppure strutturalmente sono proteine ben specifiche; quindi dare specificità per chi deve legare il metallo oppure no la si ottiene solo con l'utilizzo di Chaperoni che legano il metallo e riconoscono le proteine target che devono legare il metallo a scopi catalitici o strutturali. Il glutatione diventa un buon chelante del metallo per indirizzare il Rame verso le metallotioneine.
Cu-Chap. Cu" ALB CTR1 Cu" ATOX1 ATP7A Cu2+ Zn2+ ESTEAP1, 2 MT HEPH GSH GSSG Cu+ &dCYTB Fe3+ . For FP TF Cu2 Fel Fe2- FT DMTI Apical Plasma Membrane TJ Basolateral Plasma Membrane
Atox-1: Chaperone del Rame
Nella figura si può osservare lo chaperone più importante all'interno della cellula detto Atox-1 (Anti-oxidant-1) I questa proteina è stata messa in evidenza per la prima volta come agente antiossidante perché l'aumento della sua espressione, faceva diminuire il flusso di radicali. .Successivamente è stato osservato che questa proteina era uno chaperone che legava il Rame e che la sua attività antiossidante era dovuta al fatto che chelando il metallo, inibiva le reazioni del Rame con l'ossigeno e quindi portava di conseguenza ad una diminuzione delle specie radicaliche. Le metallotioneine (indicate in verde e giallo), sono proteine che legano i metalli (rame e zinco soprattutto) che funzionano da deposito del metallo. Il composto che indirizza il Rame verso le metallotioneine è il glutatione. Atox-1 è lo chaperone molecolare che indirizza il Rame verso la regione vasolaterale dell'enterocita [ In questa regione, c'è una proteina fondamentale detta ATP 7A che è una pompa di membrana. Questa pompa ha bisogno di energia (ATP) per effettuare il trasporto del metallo all'esterno della cellula. Questa pompa per il Rame svolge la stessa funzione che svolge la Ferroportina per il Ferro. All'esterno della cellula, il Rame, per essere trasportato a livello plasmatico, si lega preferenzialmente all'Albumina I in una regione N-terminale dell'albumina sono presenti residui amminoacidici che legano molto bene il metallo. L'enterocita oltre ad avere la via di trasporto verso l'esterno del rame attraverso lo chaperone Atox-1 e quindi permettere il passaggio del metallo dal lume intestinale verso il sangue, utilizza il metallo per tutti i processi intracellulari e quindi per donarlo a tutti i metallo-enzimi che servono per la funzionalità e l'omeostasi dell'enterocita stesso.
Funzione di Atox-1
E' la proteina più importante per lo smistamento del Rame e per il controllo della sua concentrazione a livello cellulare. E' una proteina costituita da circa 68 amminoacidi, presenta una sequenza altamente conservata. E' uno chaperone del Rame con proprietà antiossidanti dovute al fatto che la proteina lega il metallo e non gli permette di reagire con l'ossigeno molecolare.
Ruolo di Atox-1 nel trasporto del metallo
In tutte le cellule Atox-1 è responsabile del trasporto del metallo al distretto di secrezione (rappresentato dal passaggio tra il Reticolo endoplasmatico e il Golgi che poi attraverso le vescicole verrà portato verso la membrana plasmatica, si fonderà con essa e verrà rilasciato all'esterno). Atox-1 porta il Rame alla pompa di membrana ATP 7A che si trova sul versante vasolaterale. In tutte le altre cellule che non sono enterociti, il sistema di trasporto, si trova a livello del Trans-Golgi, quindi la pompa trasferirà il metallo alle metalloproteine a Rame che saranno di secrezione. Nella regione del Trans-Golgi si trovano le copper transporting ATPasi e servono per trasportare il metallo alle proteine al rame. Atox-1 ha la funzione di mantenere il corretto apporto del metallo sia a livello citosolico sia a livello mitocondriale.
Struttura di Atox-1
Cys12 Cu+ Cys15 Lys60 B1 α1
La struttura è costituita da dei foglietti ß intervallati da 2 a eliche. La struttura è B a B B a B con foglietti ß antiparalleli. Il sito di legame per il metallo è costituito da residui di cisteina che si trovano sulle a eliche: le a eliche hanno due cisteine dette funzionali perché legano il metallo in una sequenza conservata (metionina - amminoacido qualsiasi - cisteina - 2 amminoacidi qualsiasi - cisteina). Sequenza conservata fondamentale per legare il metallo e si trova in una regione tra ß1 e al. Atox-1 lega un solo atomo di Rame nella forma ridotta (Cu+1) e può acquisire il metallo anche quando esso è legato al complesso Rame- glutatione. La metionina, anche se non prende parte direttamente alla coordinazione del metallo (perché il Rame è coordinato solo dalle due Cisteina), è fondamentale per mantenere la struttura della regione adatta al legame del rame alle cisteine. La superficie delle a eliche è positiva ed è molto importante per il ruolo dello chaperone quando va a legarsi con la proteina target.
Interazione Atox-1 e ATP 7A
8 8H- 8 8- S SH 1L S SH ATOX-1 ATP 7A 1 -SH Ş- CuCD SH Cum SH'S
Schema che mette in dettaglio ciò che succede tra lo chaperone Atox-1 e la pompa ATP 7A. La pompa esiste in due isoforme che sono legate al metabolismo del rame (7A nell'enterocita e 7B a livello epatico). Vi è un'interazione fisica tra lo chaperone e la pompa che deve ricevere il metallo. L'interazione fisica avviene tra Atox-1 e la regione di legame del