Química per a oposicions de Bombers de la Generalitat
Document de Temari Bombers/es de la Generalitat. Òptim 2023 sobre Química. El Pdf, pensat per a oposicions, cobreix estats de la matèria, propietats físiques i químiques, reaccions, àcids i bases, i gasos, amb un enfocament clar i estructurat per a l'estudi de la Química.
See more10 Pages

Unlock the full PDF for free
Sign up to get full access to the document and start transforming it with AI.
Preview
TEMA 11: QUÍMICA
Temari Bombers/es de la Generalitat
Ò PT 1 M
TEMA 11
BLOC
DE CIÈNCIES
QUÍMICA
Estats de la materia i canvis d'estat. Propietats físiques i químiques.
Substàncies pures i mescles. Magnituds màssiques. Reaccions químiques.
Àcids i bases. Oxidació-reducció. Dissolucions. Compressió i expansió de
gasos. Gasos perfectes o ideals. Gasos comprimits, dissolts, liquats i criogènics.
YMPUS
PlanFL N
0x/ 1.30 Oil
.17/FN26.5
UPlanFLN
4 x /0 13
00/- FN26.5
Temari Bombers/es
de la Generalitat.
Optim 2023
Edició 3Temari Bombers/es
de la Generalitat
TEMA 11: QUÍMICA
Sumari del Tema 11
SUMARI
Cada apartat del sumari
redirigeix al lloc on es troba
l'apartat en qüestió.
- ESTATS DE LA MATÈRIA I CANVIS D'ESTAT
- LA MATERIA I L'ATOM
- LA TAULA PERIODICA
- ESTATS DE LA MATÈRIA
- CANVIS D'ESTAT
- Diagrama de fases: Punt triple i punt critic
- PROPIETATS FÍSIQUES I QUÍMIQUES DE LA MATÈRIA
- TIPUS D'ENLLAÇOS QUÍMICS
- Iònic
- Covalent
- Metàl.lic
- Enllaços d'hidrogen o forces de Van der Waals
- SUBSTANCIES PURES I MESCLES
- MAGNITUDS MASSIQUES I ALTRES MAGINTUDS
- MASSA ATOMICA
- UNITAT DE QUANTITAT DE SUBSTANCIA
- RELACIÓ UMA I GRAMS DE SUBSTANCIA
- ALTRES MAGNITUDS
- REACCIONS QUÍMIQUES
- DEFINICIÓ, REACTIUS I PRODUCTES
- LLEIS DE LES REACCIONS QUÍMIQUES
- TIPUS DE REACCIONS
- ÀCIDS I BASES
- OXIDACIÓ - REDUCCIÓ
- DISSOLUCIONS
- GASOS PERFECTES O IDEALS
- COMPRESSIÓ I EXPANSIÓ DE GASOS
- LLEI DE DALTON DE LES PRESSIONS PARCIALS
- GASOS COMPRIMITS, DISSOLTS, LIQUATS I CRIOGÈNICS
0
PT 1 M
PT 1 M
Temari Bombers/es
de la Generalitat
TEMA 11: QUÍMICA
Estats de la matèria i canvis d'estat
La matèria i l'àtom
La matèria és tot allò que ocupa espai i té massa. Està formada per àtoms.
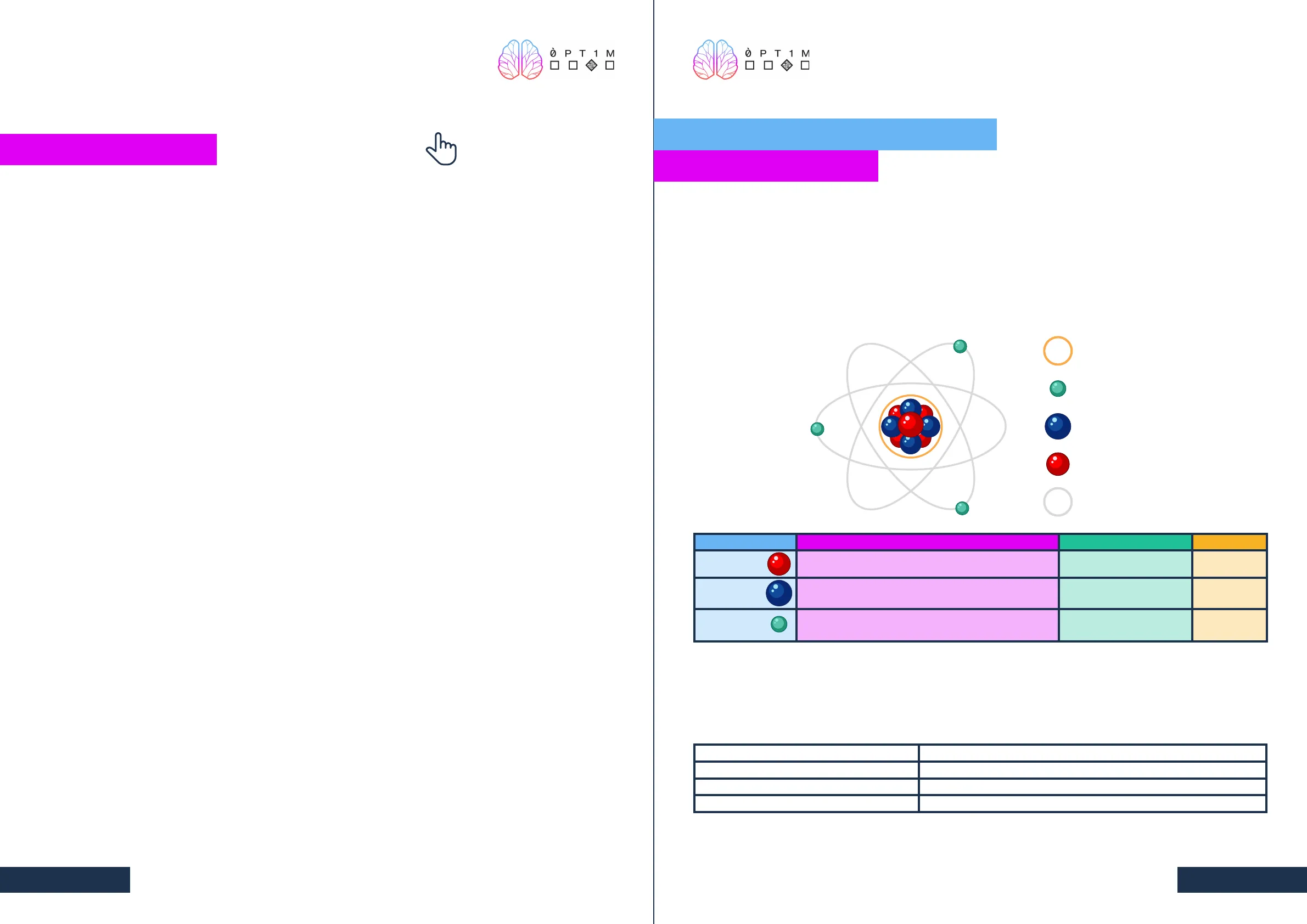
L'atom és la unitat més petita i indivisible de la materia formada per tres particules subatomiques, dues d'elles
formant el nucli i la tercera orbitant-lo:
- El nucli és la part central de l'àtom (nucleons):
- Protons.
- Neutrons.
. Orbitant al voltant del nucli trobem els: Electrons.
Nucleons
Electrons
Neutrons
Protons
Òrbita
Partícules subatòmiques
| Partícula | Situació | Carrega | Massa |
|---|---|---|---|
| Protons | Dins el nucli | (+) 1,602 . 10-19 Coulombs | 1,672 · 10-27 kg |
| Neutrons | Dins del nucli | 0 Coulombs | 1,675 · 10-27 kg |
| Electrons | Fora del nucli, a l'escorça o capes energètiques | (-)1,602 . 10-19 Coulombs | 9,101 · 10-31 kg |
Elements químics
Elements químics:
- Tots els atoms amb un mateix nombre de protons pertanyen al mateix element.
- Tenen les mateixes propietats químiques.
- Quan un atom perd o guanya protons, es transforma en un atom d'un altre element.
La informació principal d'un element químic és:
Nom i simbol
Identifica l'element
Nombre atomic (Z)
Nombre de protons
Nombre massic (A)
Nombre de protons (Z) + nombre de neutrons (N)
València
Nombre d'electrons d'un element en el seu ultim nivell d'energia
Pagina 2
Pàgina 3Temari Bombers/es
de la Generalitat
TEMA 11: QUÍMICA
0
PT 1 M
PT 1 M
Temari Bombers/es
de la Generalitat
TEMA 11: QUÍMICA
Isòtops
Isotop
Variació d'un element químic que posseeix un nombre diferent de neutrons a l'habitual, per tant el nombre màs-
sic (A) serà diferent.
e
e
e
p
pn
1
2
3
1H
7H
1H
Exemple: Els tres isòtops de l'hidrogen (tots amb 1 proto, Z = 1). El proti: hidrogen sense neutrons, A=1.
El deuteri: amb 1 neutro, A=2. El triti: amb 2 neutrons, A=3.
Ions
Ió
Àtom que no té la mateixa quantitat d'electrons que de protons. Té una carrega neta positiva o negativa.
- Anio té més electrons (carrega negativa).
- Catió> té menys electrons (càrrega positiva).
Compostos
Compost
- Substancia formada per àtoms o ions de dos o més elements químics diferents.
- La seva unitat s'anomena molécula.
- Exemple: L'aigua pura és un compost format per dos elements: hidrogen i oxigen.
La taula periòdica
1.2. La taula periodica
Taula que ordena els elements químics segons el seu nombre atòmic (118 elements segons l'última versió) i els
agrupa per propietats químiques i físiques semblants:
- Files -> Períodes (7), segons els nivells energètics de l'àtom.
- Columnes -> Grups (18) segons les configuracions electròniques de les últimes capes dels àtoms.
- Tres categories principals d'elements:
- Metalls: bons conductors de calor o electricitat.
- No metalls: pèssims conductors de calor o electricitat.
- Metal-loides: propietats híbrides entre conductors o aillants.
1,00€
METALLS
NO METALLS
4,0026
H
5
10,81
-Massa atomica relativa
Alcalinotenris
Halogens
10 20,177
B
C
N
O
F
Ne
Li
Be
Lantânid
BOF
-Nom de l'element
14
15 30,978 16
12,0G 17
29,948
Na
A
Si
P
S
CI
Ar
MALNE
ALLIMIN
20
121
47 BE7 23
24 51,9961
25 54 0380
27 58 9312
28 58.6934
29
31
32 72.6301
K
Ca
Sc
Ti
V
Cr
Mn
Fe
Co
Ni
Cu
Zn
Ga
Ge
As
Se
Br
Kr
37 85,4671 38
39
141
42
43
44
45 102.9055
146
106,47 47 1071682 48 117,414
49
THE710
51
52
126. 3045 54
Rb
Sr
Y
Zr
Nb
Mo
Tc
Ru
Rh
Pd
Ag
Cd
In
Sn
Sb
Te
1
Xe
ESTNONCI
56
57
71 72 171.49 73 181 3479 74
75
77 193,717
8 196,084 79 196,9666 80 200 587
82
83 201 0OD4 84
(209) 85
(71) 86
Cs
Ba
La-Lu
Hf
Ta
W
Re
Os
Ir
Pt
Au
Hg
TI
Pb
Bi
Po
At
Rn
BARI
HAFNI
TÀIVTAL
TUNGSTÉ
RENI
108
109
110
[291)
111
112 (285)
113
(286) |114
115
(285) 116
(233) 117
118 (2014)
Fr
Ra
Ac-Lr
Rf
Db
Sg
Bh
Hs
Mt
Ds
Rg
Cn
Nh
FI
Mc
Lv
Ts
Og
OGANESSÓ
RUTHERFORDI
DUEN
SEABORG
MEITNERI
DARMSTADTI
ROENTGENI
COPERNICI
HUIRIM
MOSCOM
LIVERMOR
69 161.8342
70
173,045 71 THLEGGI
La
Ce
Pr
Nd
Pm
Sm
Eu
Gd
Tb
Dy
Ho
Er
Tm
Yb
Lu
LANTAN
PRASEODIM
NEDOIM
PROMETI
SAMAR
ACOUN
DI SPROG
199
100
(257)
101
102
103 (26
Ac
Th
Pa
U
Np
Pu
Am
Cm
Bk
Cf
Es
Fm
Md
No
Lr
ACIN
PROTOACTIV
NEPTUN
AMERI
BERKELI
CALIFORN
EINSTEIN
FERIV
MENDELEVI
NARENGI
Estats de la matèria
1.3. Estats de la matèria
| Estat matèria | Forma | Volum | Densitat | Energia cinetica | Es pot comprimir? |
|---|---|---|---|---|---|
| Sòlid | Constant | Constant | Alta | Baixa | No |
| Líquid | Variable | Constant | Mitja | Mitja | No/molt poc |
| Gas | Variable | Variable | Baixa | Alta | Si |
Canvis d'estat
1.4. Canvis d'estat
- Amb reacció exotèrmica:
- Solidificació: El liquid es converteix en solid.
. Condensació: El gas es converteix en liquid, baixant la temperatura. Si augmenta molt la pressió
s'anomena liquefacció.
. Sublimació inversa regressiva: El gas es converteix en solid sense passar per l'estat líquid.
Pàgina 4
Pàgina 5
1
València
Punt d'ebullició ℃
-252.7
Punt de fusió ℃
-
-259.7
Simbol
Densitat
0.017
1s1.
Estructura atomica
Hidrogen
Nom
Nombre massic
(A = p + n)
A
Z
X
Nombre atomic
(Z = p)
1.00797
Pes atomic
Nombre atomic
1
Simbol del
element
B
Metall's de transición
Altres no metalls
Simbol
Actinids
Metal-loides
CARBONI
NITROGEN
COOPEN
12 24,306
13 26,9015
Altres metals
No determinat
Mg
CLOA
74 021E 34 78.971 35
79.934 36
CALC
GAL-LI
GIRMAN
APESA NIC
ESTANY
ANTIMOIN
TEL-ALE
55 137,9055
(223)
103 104 (267)
105 (270)
106 (269)
107
(T-4) |62
150.36 63
151,364 64
157.21
65 151,3754
66
167.500 67 164,83003 68
90 232,0377
91 231,0359
92 238,0283
193
94
(24) 95
TECNICI
BUITEN
PAL LA
PLATA
204.30
PLATÍ
PLOM
POLONI
35,45
18
He
Nombre atomic-
Casos nobles
HIDROGEN
à Thường mês mưadi)
VANACHT
MANGAN'S
COBALT
MIGUEL
50
13,011 7
59 HO,POTT 60 144,242 61
LUTECI
197
HTemari Bombers/es
de la Generalitat
TEMA 11: QUÍMICA
- Amb reacció endotérmica:
- Fusió: El solid es converteix en líquid.
- Vaporització o ebullició: El liquid es transforma en gas completament. Si només es transforma una
part s'anomena evaporació.
. Sublimació: El solid es transforma en gas directament sense passar per l'estat líquid.
Absorció d'energia termica
Sublimació
Fusió
Vaporització
Solid
Líquid
Gas
Solidificació
Condensació
Sublimació inversa
Cessió d'energia termica
Els canvis d'estat només modifiquen les propietats físiques de l'element següents:
- Densitat
- Viscositat
Conceptes clau dels canvis d'estat
Conceptes importants per entendre els canvis d'estat:
- Pressió de vapor:
- És la pressió que exerceix un gas sobre la seva fase líquida quan ambdós estats es troben
en equilibri dins d'un recipient.
- És una magnitud característica de cada substância.
- Augmenta amb la temperatura.
- És independent de la quantitat de líquid.
- Temperatura d'ebullició d'un líquid:
- És la temperatura a la qual la seva pressió de vapor és igual a la pressió externa.
En l'aigua en condicions normals aquesta temperatura és de 100 graus amb una pressió
de vapor d'1 atm i pot vencer la pressió atmosferica terrestre permetent que l'aigua vaporitzi.
En una muntanya tindrem menys pressió atmosferica que a la costa, per tant, es tardarà més a
coure els aliments i la temperatura d'ebullició serà més baixa. Com a resultat, l'aigua bullirà a
menys de 100 graus.
Ò PT 1 M
Temari Bombers/es
de la Generalitat
TEMA 11: QUÍMICA
- Calor específica:
- Calor necessaria perquè una unitat de massa augmenti un grau de temperatura.
Ce ->
J
ºK . Kg
ºC · Kg
J
- Calor latent:
- Calor necessaria per produir un canvi d'estat d'una unitat de massa, sense augmentar la seva
temperatura.
CI ->
J
Kg
1 Joule = 0,24 cal
1 cal = 4,18 J
Calor latent de l'aigua
| Calor latent de l'aigua | cal/g | J/kg |
|---|---|---|
| Calor latent de fusió (de solid a liquid) | 80 | 336.000 |
| Calor latent de vaporització (de liquid a gas) | 540 | 2.268.000 |
Diagrama de fases: Punt triple i punt crític
1.4.1. Diagrama de fases: Punt triple i punt critic
És un gràfic on es representen els estats de la matèria en funció de la temperatura i la pressió. Cada substância
té un diagrama de fases diferent i els punts características són:
- Temperatura crítica:
- Temperatura per sobre de la qual és impossible liquar un gas, encara que s'hi apliqui molta pressió.
- Temperatura més elevada on una substancia pot existir en fase líquida (punt critic).
- Com més força intermolecular tingui una substància, més alta serà la seva temperatura crítica.
- Pressió crítica:
- Pressió mínima necessaria per condensar un gas a la temperatura crítica.
- Punt triple:
- Punt on coexisteixen les tres fases d'una substância amb una determinada pressió i temperatura.
Comparativa de diagrames de fases
Comparativa entre els diagrames de l'aigua (H2O) i el dioxid de carboni (CO2)
Diagrama de fases genèric
Substàncies
que s'expandeixen
en congelar-se
Substancies que es
contreuen en congelar-se
Liquid
Punt
critic
Fusió
Fusió
Vaporització
Sòlid
Punt
triple
Sublimació
Vapor
Pàgina 7
T
P
Pàgina 6
Ø
PT 1 M
Temari Bombers/es
de la Generalitat
TEMA 11: QUÍMICA
ø
PT 1 M
PT 1 M
Tipus d'enllaços químics
2.1. Tipus d'enllaços químics
Enllaç Iònic
2.1.1. Iònic
- Unió molt forta entre un anió i un catió.
- Punt de fusió i ebullició molt alts.
- Es dissolen en aigua.
- Ex: NaCl (sal) i CaO (calç)
Enllaç iònic
Ió de sodi
Ió de clor
+
Clorur de sodi (NaCl)
Enllaç Covalent
2.1.2. Covalent
- Unió molt forta entre dos àtoms que comparteixen parells d'electrons.
Segons en nº de parells compartits son simples o senzills (1 parell),
dobles o triples.
- Si els dos electrons que formen l'enllaç son d'un mateix atom serà un
enllaç covalent datiu o coordinat.
- Punt de fusió i ebullició menors que en iònics. Segons la seva
electronegativitat poden ser polars o apolars.
- La solubilitat en aigua i la conductivitat elèctrica varia segons la substância.
- No condueixen l'electricitat.
- Sol donar-se entre no metalls.
. Ex: N2
Enllaç Metàl·lic
2.1.3. Metal-lic
- Unió de força variable entre catió i electrons deslocalitzats.
- Punt de fusió i ebullició molt alts.
- No solubles en aigua.
- Ex: Fe i Hg
Molécula
de Nitrogen (N)
Àtom de
nitrogen (N)
Àtom de
nitrogen (N)
·x
X.
Pàgina 8
Diagrama de fases del diòxid de carboni
Diagrama de fases
del dioxid de carboni
73
Punt
critic
Liquid
Solid
5,2
Punt
triple
T.
‘sublim
Gas
1
-78
-56,4
31,1
Temperatura ºC
Exemples:
A 1atm i -77 ºC el CO2 serà gas
A 6 atmi-50 °C el CO2 serà liquid
A 1 atm i -80 ℃ el CO2 serà solid
Propietats físiques i químiques de la matèria
2. Propietats físiques i químiques de la matèria
- Propietats generals o extensives:
- El seu valor depèn de la quantitat de matèria.
- Exemples: massa, pes, volum, inercia, energia, impenetrabilitat, porositat, divisibilitat, elasticitat,
mal-leabilitat, tenacitat i duresa, entre d'altres.
- Propietats especifiques o intensives:
El seu valor és independent de la quantitat de matèria. Es classifiquen en:
- Físiques:
- Aquelles que es poden percebre pels sentits.
- Exemples: la densitat, el punt de fusió, el punt d'ebullició, el coeficient de solubilitat, l'index
de refracció, el modul de Young i les propietats organoleptiques (color, olor, aroma, tast, textura).
- Químiques:
- Constituïdes pel comportament de les substancies en combinar-se amb d'altres, i els canvis en
la seva estructura com a consequència dels efectes de diferents classes d'energia.
- Exemples: corrosió d'àcids, poder calorific, acidesa, reactivitat, etc.
Temari Bombers/es
de la Generalitat
TEMA 11: QUÍMICA
Diagrama de fases de l'aigua
Diagrama de fases de l'aigua
Punt
critic
218
P
Liquid
Solid
1.00
Punt
triple
0.00603
Vapor
T. T.
0.00 0.01
T
100,0
T
374
Temperatura ºC
Exemples:
A 1atm i 80 ºC l'H2O serà liquida
A 0,006 atm i 50 °℃ l'H2O serà gas
A 200 atm i 120 °C l'H2O serà liquida
Pressió atm
P.
Àtom de sodi (Na)
Àtom de clor (Cl)
Pàgina 9