Replicación del DNA: características, telomerasa y ADN mitocondrial
Documento de Universidad sobre Replicación del DNA. El Pdf, un material de Biología, explora la replicación del DNA, un proceso fundamental para la transmisión genética, incluyendo la telomerasa y la replicación del ADN mitocondrial.
Ver más28 páginas
Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Replicación del DNA
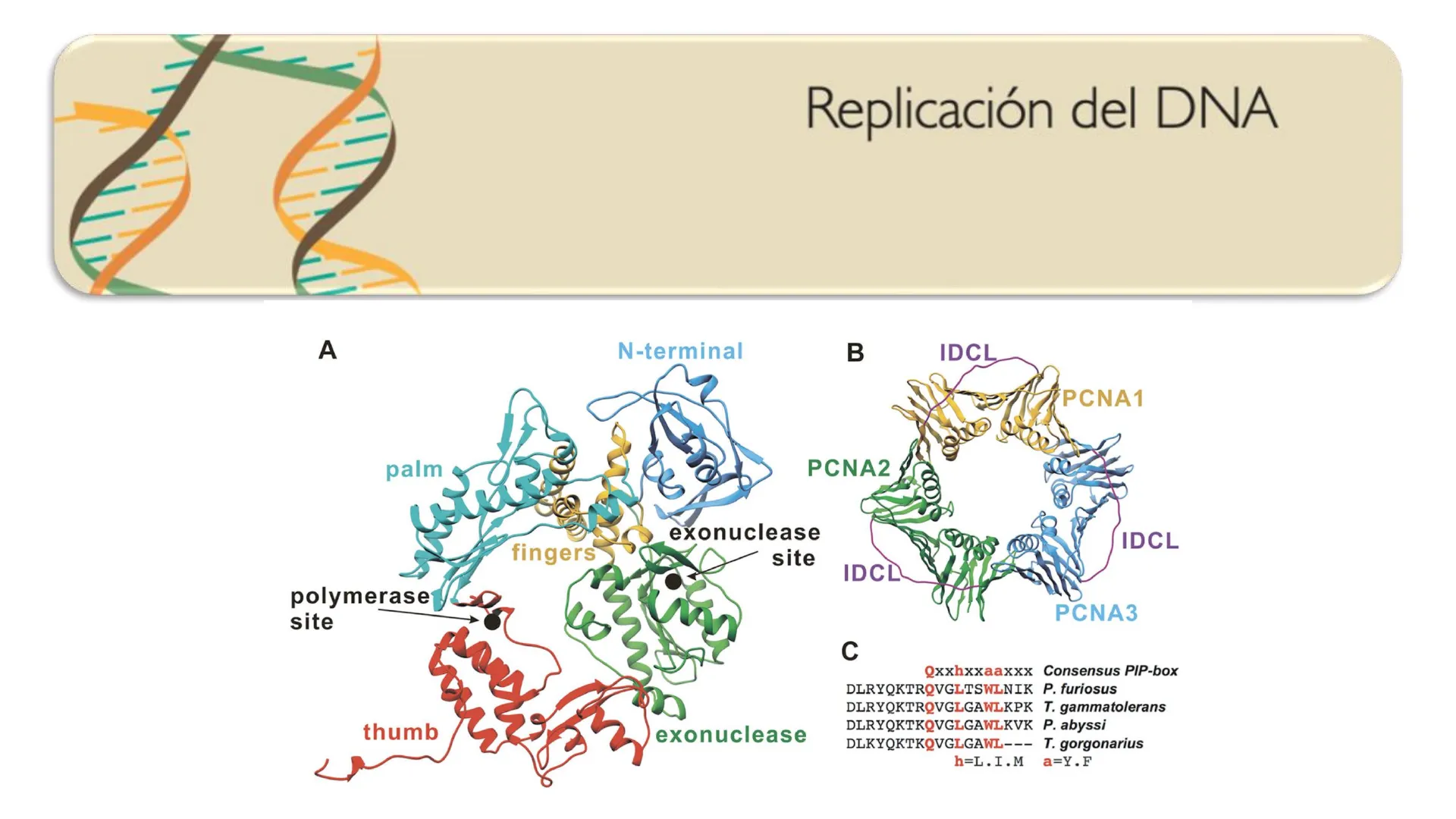
A N-terminal B IDCL PCNA1 palm PCNA2 IDCL fingers exonuclease site polymerase site PCNA3 C Qxxhxxaaxxx Consensus PIP-box DLRYQKTRQVGLTSWLNIK P. furiosus DLRYQKTRQVGLGAWLKPK T. gammatolerans DLRYQKTKQVGLGAWLKVK P. abyssi DLKYQKTKQVGLGAWL --- T. gorgonarius h=L.I.M a=Y.F thumb exonuclease
Características Generales de la Replicación
La replicación es el proceso, conceptualmente sencillo pero molecularmente complejo, mediante el cual a partir de una molécula de DNA progenitora o parental se sintetiza una nueva, originándose así dos moléculas de DNA hijas, de secuencia idéntica a la del DNA original. Esto permite el paso de la información genética a la descendencia (tanto la de una célula como la del individuo).
Aunque la replicación constituye el aspecto esencial del metabolismo del DNA, también se deben considerar como parte del mismo otros procesos relacionados directa o indirectamente: la recombinación o reordena- miento de la información genética, la mutación o alteración de la secuencia, y la reparación de las alteraciones o daños en el DNA. Cabe también añadir la degradación o catabolismo del DNA hacia nucleótidos, mediado por las nucleasas.
DNA' replicación conjunto de procesos metabólicos del DNA recombinación (errores) DNA mutación DNA' reparación
Carácter Semiconservador de la Replicación
Aunque hipotéticamente se pueden plantear tres mecanismos para la replicación, pronto se demostró que sólo el tercero tiene lugar en las células:
Replicación conservadora Un complejo enzimático recorrería el DNA, reconociendo la secuencia en ambas hebras para copiarlas simultáneamente, de forma que el DNA progenitor bicatenario se conservaría intacto mientras que la molécula hija de DNA contendría dos hebras totalmente nuevas
Replicación dispersante La síntesis se produciría por fragmentos, que se combinarían con partes del DNA progenitor, dando lugar a las dos moléculas hijas de DNA, ambas con fragmentos tanto nuevos como de las dos hebras del DNA progenitor
Replicación semiconservadora Es el mecanismo real. Las dos hebras del DNA progenitor sirven de molde para la síntesis de sus respectivas hebras complementarias. Cada molécula hija de DNA está formada por una hebra progenitora y otra hija (recién sintetizada). El mecanismo se repite en sucesivas generaciones de células. El nombre alude, precisamente, a que siempre se conserva la mitad de la molécula original
molécula de DNA progenitora La replicación semiconservadora del DNA es coherente con el modelo de doble hélice nuevos nucleótidos 3' conservadora dispersante semiconservadora hebra nueva 5 hebra nueva hebra hija hebra hebra progenitora progenitora hebra hija
Demostración Experimental de la Replicación Semiconservadora
El mecanismo real de la replicación lo demostraron por primera vez Mathew Meselson y Franklin W. Stahl en 1958, mediante experimentos muy completos, sencillos y representativos de muchos otros realizados en diversas áreas de la biología molecular. Aunque los aspectos moleculares de la replicación se establecieron posteriormente con el estudio de la DNA polimerasa, el experimento de Meselson y Stahl tiene interés, aparte de por su propio diseño, por haber sido la primera vez que se aplicaron tanto la técnica de sedimentación en gradiente de densidad como la introducción de isótopos en las moléculas de DNA (15N, infrecuente, y 14N, isótopo habitual).
Para comprender la novedad y trascendencia de estos experimentos en su momento y contexto, se van a considerar los antecedentes y el planteamiento antes de describir el resultado. Se aprovecha así este ejemplo para ilustrar el método científico, en especial cómo un diseño adecuado del experimento, que parece simple, permite obtener una información notable.
Antecedentes de la Demostración Experimental
El primer lugar, se examina la posibilidad de aplicar la técnica de equilibrio de sedimentación en gradiente de densidad, o centrifugación isopícnica (pág. 126), al análisis de muestras de DNA cuya densidad es diferente por estar marcado o no con el isótopo 15N.
Alcanzado el equilibrio de sedimentación, las moléculas de DNA se concentran formando una banda, detectada por su absorción UV DNA normal ("ligero", 14N) V DNA "pesado" (15N) Mezcla de DNA "pesado" y DNA "ligero" A 260 A, 260 1,69 1,71 1,73 densidad 1,75 1,69 1,71 1,73 1,75 densidad A 260 1,69 1,71 1,73 1,75 densidad Gradiente de densidad formado con CsCl La densidad del DNA pesado es 0,016 g/cm3 mayor (un 1%) que la del DNA ligero; por ello, se sitúa un poco más abajo en el gradiente Es posible separar ambos tipos de DNA (unos 0,5 mm entre las bandas)
Enzimología de la Replicación
Requerimientos de la Reacción de Síntesis de DNA
- Sustratos: se utilizan como sustratos el conjunto de los cuatro desoxinucleósidos-trifosfato: dATP, dGTP, dCTP y dTTP. De cada uno de ellos queda incorporado en el nuevo DNA la parte dNMP de la molécula. Tanto dNMP como dNDP no sirven como sustratos.
- Cofactores: para una actividad óptima se requiere un ion metálico divalente como cofactor, asociado a los dNTP y a la polimerasa. Aunque in vitro este papel pueden desempeñarlo tanto Mn2+ como Mg2+, es este último el que actúa in vivo.
- Molde o plantilla>ésta es, quizá, la principal característica de la reacción. El orden correcto de incorporación de los nucleótidos viene determinado por su complementariedad de bases con la secuencia de cada hebra de DNA, que actúa así como molde o plantilla.
- Cebador: la síntesis de una nueva hebra de DNA no puede comenzarse a partir de dos nucleótidos, sino que requiere un fragmento monocatenario iniciador, denominado cebador, que aporte un grupo 3'-OH libre. Se trata de un oligonucleótido, por lo común RNA, que debe estar emparejado con la hebra progenitora de DNA, de forma complementaria y antiparalela. Este requisito puede expresarse afirmando que la replicación no es autoiniciadora (a diferencia de la transcripción, pág. 268), sino que sólo elonga o alarga moléculas preexistentes.
Mecanismo de la Reacción de Polimerización
Se inicia la reacción con el emparejamiento de un dNTP complementario al nucleótido de la hebra molde (DNA) en la posición vecinal al extremo 3' de la hebra en crecimiento (inicialmente, el RNA cebador; luego, la hebra que se está sintetizando). La reacción propiamente dicha consiste en la unión del dNTP seleccionado, que queda como dNMP, liberándose PP ¡. Ello implica la formación de un enlace fosfoéster entre el fosfato a del dNTP que se incorpora y el 3'-OH libre de la cadena en crecimiento (inicialmente, del cebador). La ruptura del enlace fosfoanhídrido (a-B) del dNTP proporciona la energía necesaria para impulsar la reacción, ayudada por la subsiguiente hidrólisis del PP¡ a 2 Pi catalizada por la pirofosfatasa. Tras muchas reacciones similares sucesivas, el producto es la nueva hebra de DNA:
n1 dATP + n2 dGTP + n3 dCTP + n4 dTTP DNA molde, DNA + (n1 + n2 + n3 + n4) PPi RNA cebador, Mg2+, DNA polimerasa
REACCIÓN DE POLIMERIZACIÓNDEL ADN P PH P 3' 5' -- P P P OH OH T C T A G G A A T C ® P P P P ® -- 5' 7 -> 20 5' ® P P ® OH T T A G G A A T C a ® P P P P P. 3' -- 5' 3' -- @ c nucleótido trifosfato +1
Tipos de Polimerasas
Aunque la reacción de síntesis de DNA es universal, es decir, tiene lugar de idéntica forma en todos los organismos y ubicaciones subcelulares, su catálisis la efectúan en cada caso distintas enzimas, bajo la denominación común de DNA polimerasas (abreviadas como DNApol). Estrictamente su nombre es más completo, polimerasas de DNA dirigidas por DNA (o dependientes de DNA), para indicar tanto la molécula que sintetizan como la que emplean como molde. Más adelante se estudiarán otras polimerasas de DNA o de RNA que utilizan distintos moldes; para ofrecer una visión unificada se resumen a con- tinuación:
| Molécula sintetizada | Molécula molde | Nombre completo | Ejemplos (nombre común) |
|---|---|---|---|
| DNA | DNA | Polimerasa de DNA dirigida por DNA | DNA polimerasas |
| RNA | DNA | Polimerasa de RNA dirigida por DNA | RNA polimerasas o transcriptasas Primasas |
| DNA | RNA | Polimerasa de DNA dirigida por RNA | Transcriptasas inversas Telomerasas |
| RNA | RNA | Polimerasa de RNA dirigida por RNA | RNA replicasas |
DNA Polimerasas Procarióticas: Actividades Polimerasa y Exonucleasas
CARACTERÍSTICAS DE LA DNA POLIMERASA I DE E. coli DNApol-I (unida al DNA) una sola cadena polipeptídica, 103 kDa centro activo polimerasa (5'-> 3') centro activo 3'-exonucleasa centro activo 5'-exonucleasa Fragmento "grande" o de Klenow C-terminal, 68 kDa. Presenta las actividades polimerasa y 3'-exonucleasa. Muy bien estudiado, se emplea con frecuencia para la síntesis in vitro de DNA. hebra molde 3' 5 hebra 5 3' nueva XU proteólisis con subtilisina o tripsina Nucleótido recién incorporado (3'), a punto de unirse a la hebra en crecimiento. Si es erróneo, será eliminado por la actividad 3'-exonucleasa. El nucleótido 5' terminal, correctamente emparejado, puede ser eliminado por la actividad 5'-exonucleasa. Fragmento "pequeño" N-terminal, 35 kDa. Sólo muestra la actividad 5'-exonucleasa. Estructura poco conocida.
Características Bioquímicas y Funcionales de las DNA Polimerasas
| Procariotas | Eucariotas | |||||||
|---|---|---|---|---|---|---|---|---|
| Polimerasa: | I | II | = | a | B | Y | 8 | Ubicación subcelular |
| Núcleo | Núcleo | Mitocondria | Núcleo | Núcleo | ||||
| Actividades enzimáticas: | ||||||||
| Primasa (inicio) | No | No | No | Sí | No | No | No | No |
| Polimerasa 5' -> 3' (elongación) | Sí | Sí | Sí | Sí | Sí | Sí | Sí | Sí |
| 3'-Exonucleasa (o 3' -> 5') (corrección de pruebas) | Sí | Sí | Sí | No | No | Sí | Sí | Sí |
| 5'-Exonucleasa (o 5'->3') (eliminación de cebadores) | Sí | No | No | No | No | No | No | No |
| Función en la célula: | ||||||||
| Replicación (síntesis continuada de hebras nuevas, adelantada y retardada) | No | No | Sí | Sólo inicialmente | No | Sí | Sí | Sí |
| Empalme de fragmentos de Okazaki | Sí | No | No | No | No | Sí | (con nucleasas) | |
| Velocidad de replicación: | ||||||||
| Velocidad de polimerización (nucleótidos/segundo) | 16-20 | 2-7 | 250-1.000 | |||||
| Procesividad (nucleótidos añadidos antes de su disociación) | Baja | 3-200 | Media | ≥ 10.000 | Muy alta | ≥ 5×105 | Baja | 100-200 |
| Baja | Elevada | Elevada | Elevada con PCNA con/sin PCNA | ≥ 5.000 |
Características Estructurales de las DNA Polimerasas
| Procariotas | Eucariotas2 | |||||||
|---|---|---|---|---|---|---|---|---|
| Polimerasa: | I | II | a | Y | 8 | 00 | ||
| Masa total (kDa)(3) | 103 | 90 | £ 900 | 356 | 39 | 160 | 173 | 313 |
| N.º de subunidades | 1 | ≥ 4 | 22 | 4 | 1 | 3 | 203 | 4 |
| Masa de subunidades (4) | (5) | 125 | 125 | 258 | 35 | |||
| 48 | 55 |
1 Al menos en E. coli se han identificado otras dos polimerasas, IV y V. 2Los datos corresponden a humanos. Existen otras DNA polimerasas minoritarias o no esenciales. 3Masa molecular de la holoenzima, o enzima funcional con todas sus subunidades. 4La DNApol-III de E. coli está formada por 22 subunidades de 10 tipos, con una composición global (a, 8, 0)272(y, 8, 8', 0, 4)284. De ellas, la agrupación (a,8,0) se conoce como "núcleo" o "centro" de la polimerasa. El centro activo polimerasa está en la subunidad x (130 kDa), mientras que el centro 3'-exonucleasa o actividad correctora de pruebas está en la 8. 5La DNApol a humana está formada por 4 subunidades diferentes: 180 kDa, con el centro activo polimerasa; 48 kDa, con el centro activo primasa; 58 kDa, cofactor de la primasa; 70 kDa, reguladora de la polimerasa.