Enlace Químico: Propiedades de los Elementos y Compuestos en Química
Documento de Universidad sobre Enlace Químico. Propiedades de los Elementos y de los Compuestos. El Pdf, un documento de Química para Universidad, explora los enlaces primarios, la electronegatividad, el enlace metálico y las fuerzas intermoleculares, incluyendo la teoría de bandas y los enlaces por puente de hidrógeno.
Ver más30 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Enlaces primarios y electronegatividad
Tema 2 ENLACE QUÍMICO. PROPIEDADES DE LOS ELEMENTOS Y DE LOS COMPUESTOS.
- Enlaces primarios: metálico, covalente, iónico.
Tipos de enlace según la electronegatividad
1.1. Tipos de enlace en función de la electronegatividad. En la década de 1930, Linus Pauling propuso un parámetro llamado electronegatividad del átomo, que permite decidir si el enlace es polar, cuál átomo del enlace es negativo y cuál es positivo, y si un enlace es más polar que otro. La electronegatividad (x), de un átomo se define como una medida de la capacidad de un átomo en una molécula para atraer electrones hacia sí mismo. Varias características y tendencias periódicas son aparentes, el elemento con mayor electronegatividad es el flúor y se le asigna un valor de x=4.0. El elemento con menor electronegatividad es el metal alcalino francio. La electronegatividad generalmente aumenta de izquierda a derecha a través de un periodo y disminuye al descender por un grupo. Esto es lo opuesto a la tendencia observada para el carácter metálico. Los metales tienen de manera típica valores bajos de electronegatividad, que abarcan desde ligeramente menos de 1 hasta cerca de 2. Los valores de electronegatividad para los metaloides son cercanos a 2, mientras que los no metales tienen valores mayores de 2. No se tienen valores para He, Ne y Ar porque no se sabe que estos elementos formen compuestos químicos.
Valores de electronegatividad y tipos de enlaces
Valores de electronegatividad Tipos de enlaces Formación X elevada electronegatividad X-X covalente Se lleva a cabo entre no metales. Entre elementos de elevada electronegatividad. X-Y Y iónico baja electronegatividad Y-Y metálico Se lleva a cabo entre metales, elementos de baja electronegatividad
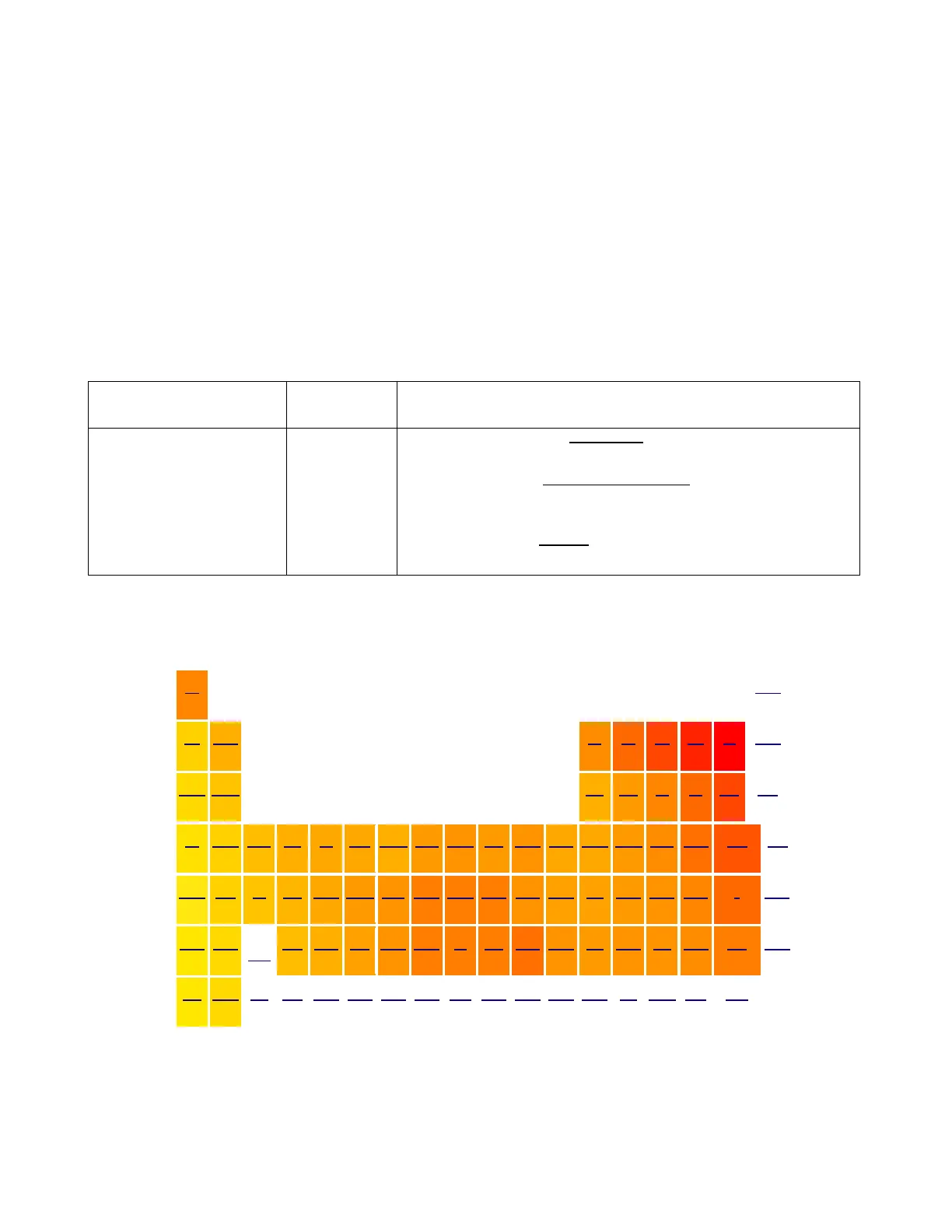
Tabla Periódica con valores de electronegatividad
Tabla Periódica con valores de electronegatividad Radio atómico disminuye > Energía de ionización aumenta > Electronegatividad aumenta> He 1 2.1 BC N O F Ne 1.0 1.5 2.0 2.5 3.0 3.5 4.0 Na Mg Al Si P S Cl Ar 0.9 1.2 1.5 1.8 2.1 2.5 3.0 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Kr 4 0.8 1.0 1.3 1.5 1.6 1.6 1.5 1.8 1.9 1.9 1.9 1.6 1.6 1.8 2.0 2.4 Br 2.8 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 5 0.8 1.0 1.2 1.4 1.6 1.8 1.9 2.2 2.2 2.2 1.9 1.7 1.7 1.8 1.9 2.1 2.5 Cs Ba Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 0.7 0.9 1.3 1.5 1.7 1.9 2.2 2.2 2.2 2.4 1.9 1.8 1.9 1.9 2.0 2.2 Fr Ra Lr Rf Db Sq Bh Hs Mt Ds Rq Cn Nh FI Mc Lv Ts 0.7 0.7
Enlace metálico y modelos
1.2. Enlace metálico.
Modelo del Mar de electrones y Teoría de bandas
1.2.1. Modelo del Mar de electrones y Teoría de bandas. Los enlaces metálicos se caracterizan por la puesta en común de los electrones de valencia que no se encuentran localizados entre los átomos (enlace covalente) o sobre un ión (enlace iónico), pero que están repartidos en el conjunto de la red de iones. 6 Lu 7 H Li Be 2 3 Se lleva a cabo entre un metal y un no metal. un elemento de elevada electronegatividad y uno de baja x. Entre mayor sea la diferencia de electronegatividades, mayor carácter iónico.Los metales están formados por lo tanto, de elementos que poseen pocos electrones de valencia; elementos de los grupos IA y IIIA de la Tabla Periódica. Aquellos que tienen el carácter metálico más marcado están en el grupo IA: no poseen más que un electrón de valencia. A medida que uno se desplaza hacia la derecha de la Tabla Periódica el carácter covalente del enlace aparece cada vez más marcado. Así el Bismuto (grupo VB) tiene un enlace mixto "covalente-metálico". El arreglo cristalino de los materiales metálicos resulta de las fuerzas de atracción y de repulsión que se ejercen entre los iones positivos y la nube de electrones deslocalizados. Las estructuras cristalinas que se derivan son por regla general altamente simétricas, de compactación elevada y pueden considerarse como apilamiento de esferas.
Conductividad y Teoría de Bandas
Conductividad y Teoría de Bandas Los electrones en un átomo sencillo, ocupan niveles discretos de energía. El principio de exclusión de Pauling indica que cada nivel (orbital) contiene únicamente 2 electrones. Por ejemplo, el nivel 2sde un átomo simple contiene un nivel de energía y dos electrones. El nivel 2p contiene tres orbitales y un total de 6 electrones. Cuando N átomos se unen para formar un sólido, el principio de exclusión de Pauling aún requiere que sólo dos electrones en todo el sólido tengan la misma energía. Cada nivel de energía por lo tanto, se convierte en una banda, como puede mostrarse para el sodio en la figura abajo. En consecuencia, la banda 2s en un sólido contiene N niveles de energía y 2N electrones, dos en cada nivel de energía. Cada uno de los niveles 2p, contiene N niveles de energía y 2N electrones. Puesto que las bandas 2p realmente se traslapan, se puede alternativamente describir una banda simple 2p ancha que contiene 3N niveles de energía y 6N electrones, (figura de la izquierda)
Conductividad Eléctrica y Teoría de bandas
Conductividad Eléctrica y Teoría de bandas Li Mg Electrones 2N electrones Banda de Valencia solapa con la banda de conducción Mg(Z = 4)_ce >1s2252 2p 6N electrones Energía 2p 25 -00 2N electrones tối Banda de Valencia 1s-40- 2N electrones Li Li2 Lis Li4 LiN 1 átomo 2 átomos N átomos Mg Mg2 Mg3 Mg4 MgN LOS NIVELES DE ENERGÍA SE ENSANCHAN EN FORMA DE BANDAS, conforme se incrementa el número de electrones agrupados. Es decir, cuando existe un enorme número de átomos, éstos se encuentran en su máxima compactación en los metales, por lo que los niveles de energía tambien se superponen compactándose y creando para cada nivel de energía bandas ensanchadas para cada nivel específico de energía. Al aumentar el nº de átomos de Li el cristal crece, se van añadiendo niveles de energía adicionales, de manera que el espaciado entre los niveles es cada vez más pequeño: se forman Bandas de Energía. N átomos de Li dan N orbitales con una separación extremadamente pequeña entre cada par de niveles de energía sucesivos: -N/2 forman la Banda de Valencia (BV): llenos de e- -N/2 forman la Banda de Conducción (BC): vacíos de e -. En el caso del metal Li, la conductividad se explica por el movimiento de los e- desde la BV hacia la BC, que está vacía. Una vez que los e- alcanzan la BC se pueden mover libremente en ella. Además, se generan huecos en la BV y se favorece el movimiento de los e- de niveles inferiores de la BV En el caso del metal Mg, la BV solapa con la BC. La conductividad se explica por el movimiento de los electrones desde la BV hacia los niveles más bajos de la BC. En un átomo aislado, los niveles de energía de los electrones ligados al núcleo están perfectamente cuantificados y regidos por el principio de Pauli. Lo anterior no es así, cuando la distancia entre los átomos disminuye para alcanzar un valor de equilibrio, tal y como se produce en los sólidos. La interpenetración y la interacción de los orbitales electrónicos vecinos comportan un ensanchamiento de los niveles de energía, los cuales forman entonces una banda de energía constituida de 3500 Banda de Valencia semillena Li(Z = 3) ce > Is22s' Banda de Conducción Energía 1+4 2sniveles discretos. Cada uno de estos niveles discretos corresponde a una de las energías permitidas de los electrones, y el número de niveles es igual al número de átomos del sólido. Una banda de energía contiene un número muy grande de niveles de energía distintos, pero poco diferentes los unos de los otros. (Figura de la derecha). A la distancia de equilibrio entre los átomos, la anchura de las bandas depende del nivel de energía inicial de los electrones y del grado de recubrimiento de esas energías (figura a la derecha parte b). En los sólidos, los niveles de energía de los electrones de las capas profundas forman bandas estrechas llamadas bandas internas. Por el contrario, los niveles de energía de los electrones de capas externas o capas de valencia, forman bandas más anchas llamadas bandas de valencia. Las bandas que corresponden a los estados excitados de los electrones de las capas externas se denominan bandas de conducción; la energía superior de la banda de valencia se designa por el símbolo Ev y por el símbolo Ec la energía inferior de la banda de conducción. El ancho, Eg, de la banda prohibida, que separa la banda de valencia de la banda de conducción (Eg=Ec-Ev), constituye un parámetro importante. En los sólidos con enlace covalente e iónico, debido a que esta banda prohibida es lo suficientemente ancha (Eg> 4 eV), los electrones de la banda de valencia, bajo el efecto de un campo eléctrico, no se encuentran lo suficientemente excitados para pasar a la banda de conducción y convertirse en electrones libres de desplazarse. Los sólidos con enlace iónico y covalente, son por lo tanto aislantes eléctricos. Por el contrario, en los metales, el ancho de la banda prohibida es nula, porque las bandas de valencia y conducción se enciman o traslapan (Ev>Ec) Ya que los electrones de la banda de valencia no ocupan todos los niveles de energía disponibles de esta banda, ellos pueden adquirir, bajo el efecto de un campo eléctrico, una energía cinética suficiente para pasar a niveles de energía superiores y convertirse así, libres de desplazarse; en este caso, el sólido es un conductor electrónico.
Tipos de materiales según la banda prohibida
1 BC BC BC Ep = 10 eV BV BV a) Aislante b) Conductor c) Semiconductor
Caso particular de los semiconductores tipo n y tipo p
Caso particular de los semiconductores tipo n y tipo p Semiconductor tipo n Semiconductor tipo n a b a b S Si Si O OC S OO O S 00 S Electrón libre Banda de valencia Banda de valencia Se crea un nivel aceptor (Ea) Figura teoría de bandas a) En un material aislante electrónico, todos los niveles de energía están ocupados: el ancho Eg de la banda prohibida es tal que los electrones de la banda de valencia no pueden excitarse suficientemente para pasar a la banda de conducción, la cual queda vacía. b) En un material conductor electrónico, una parte de los niveles de energía de la banda de valencia se encuentran sin ocupar, y las bandas de valencia y de conducción se empalman o traslapan. c) En un material semiconductor las bandas de valencia y conducción se encuentran más cercanas Ejemplo: Intervalo prohibido de energía para algunos semiconductores y aislantes Gap de Energia (el) Aiutadores Semicondactores eV Diamante 5.33 Silicio 1.14 Oxido de Zinc 3,2 Germanio 0.67 Cloruro de Plata 3.2 Telaio 0,33 Saltro de Cadmio 2.42 Antimoniuro de Indio 0.23 Se crea un nivel donador (Ed) Banda de conducción Si OO Si Si O O O O OC Si -C 0-0- S C C S + Hueco Los esquemas de la izquierda (a) representan la estructura química del semiconductor, la matriz es de Si en ambos casos. Un átomo del grupo V (tipo n) sustituye a un silicio Si; un átomo del grupo III (tipo p) sustituye a un átomo de Si. Los de la derecha (b) representan el esquema de bandas de un semiconductor Todos los semiconductores requieren de temperatura para su funcionamiento Banda de conducción Ep == 1 eV BV*