Principios y métodos básicos del cultivo celular: técnicas y características
Documento de Universidad sobre Principios y Métodos Básicos de Cultivo Celular. El Pdf, un apunte de Biología para Universidad, explora las técnicas, ventajas y desventajas del cultivo celular, así como las características de las células cultivadas y los cultivos histotípicos y organotípicos.
Ver más44 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Técnicas de cultivo celular
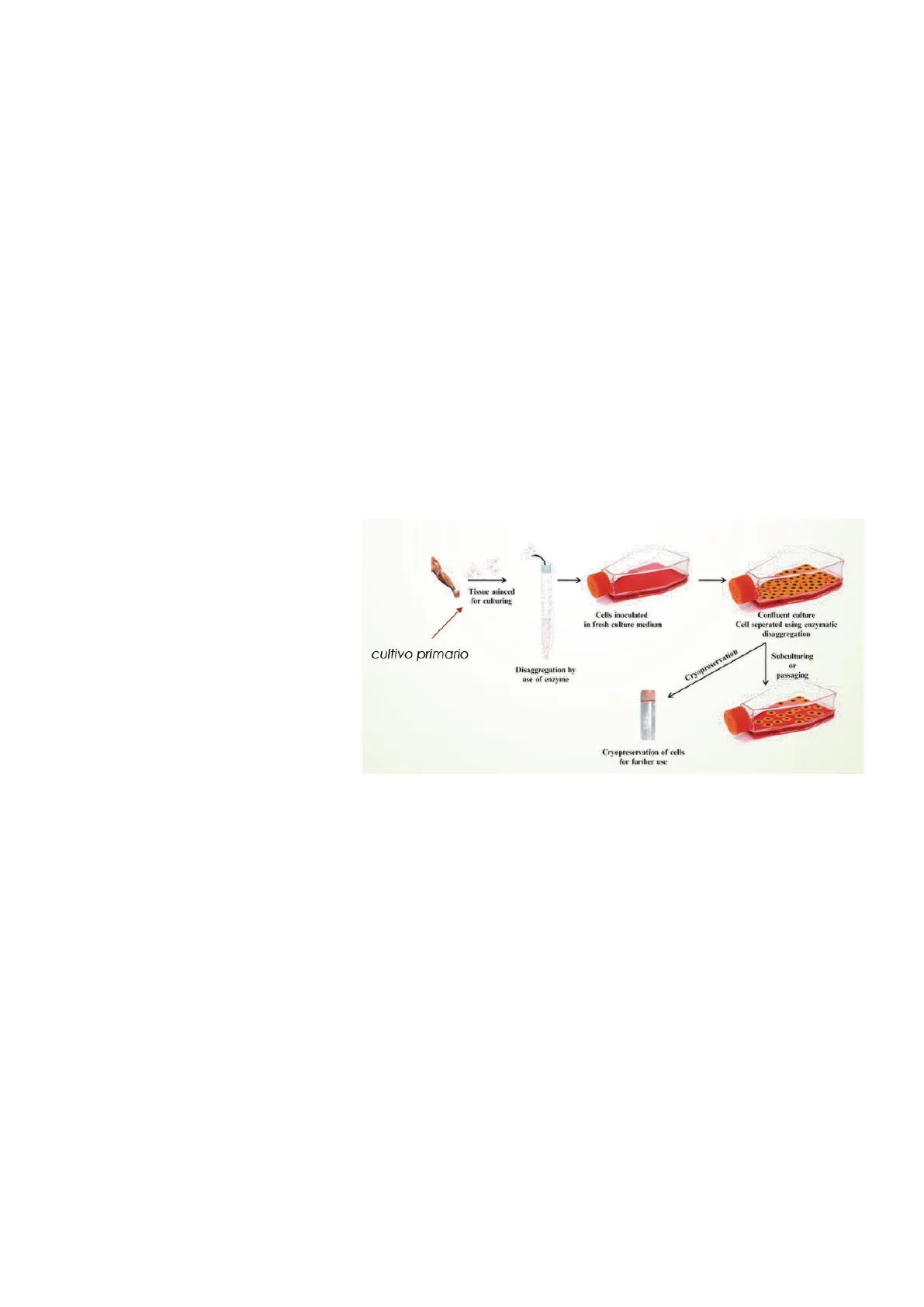
Consisten en el cultivo de células dispersas obtenidas de un tejido a partir de disgregación mecánica, enzimática o química, o de líneas celulares establecidas.
- Denominación inicial: cultivo tisular (tissue culture). Se llamaba así porque partíamos de un
tejido.
- Se cogía un trozo del paciente (animal, planta ... ) -> se observó que ciertas células migraban de manera individual y proliferaban. - > Se observó con tratamiento mecánico, enzimático o químico se favorecía la disgregación -›Ejemplo: tripsina.
- Cuando trabajamos al partir de un tejido, hablamos de cultivo primario.
- Cuando las células llenan el frasco, hay que pasarlas a un frasco de cultivo nuevo, con nuevo medio, para que se sigan dividiendo (subcultivo). A partir de aquí podemos hablar de línea celular.
- 'Cultivo celular' también puede usarse para referirse a cultivos tridimensionales de tejidos no desagregados (organ culture).
Tissue minced for culturing Cells inoculated in fresh culture medium Confluent culture Cell seperated using enzymatic disaggregation cultivo primario Disaggregation by use of enzyme Cryopreservation Subculturing or passaging Cryopreservation of cells for further use
Historia del cultivo celular
- 1885 Roux. Mantiene células embrionarias de pollo en solución salina (PBS) durante varios días. Esta solución no tiene nutrientes, por lo que las células acaban muriendo.
- 1907 Harrison. Cultiva médula espinal embrionaria de anfibios. Observa el crecimiento de los axones de los neuroblastos, y establecé que el axón se formaba por expansión a partir del cuerpo neuronal y no por fusión de una cadena de celulas (no es una hilera de células individuales).
- 1910 Burrows. Logra identificar un medio de cultivo adecuado (plasma) para nutrir los explantes de tejidos embrionarios de pollo.
- 1912 Burrows y Carrel. Comprueban que las células pueden crecer en cultivo.
- 1916 Rous y Jones. Emplean por primera vez tripsina para disociar células (disgregación enzimática)
- 1952 Gey. Establece una línea celular continua de carcinoma cervical humano conocida actualmente como "línea celular HeLa". (Henrietta Lacks)- 1954 Rita Levi-Montalcini. Establece que el factor de crecimiento nervioso (NGF) estimula el crecimiento de los axones en tejidos en cultivo (Premio Nobel 1986).
- 1955 Eagle. Realiza el primer estudio sistemático de los requerimientos nutricionales de las células en cultivo (qué nutrientes se debían añadir para que las células estuviesen vivas y creciesen)
- 1961 Hayflick y Moorhead. Comprueban que los fibroblastos humanos en cultivo mueren tras un número limitado de divisiones.
Ventajas de las técnicas de cultivo celular
- Control de las condiciones fisicoquímicas y fisiológicas (en incubadores de CO2, por ejemplo)
- Fisicoquímicas: pH, temperatura, presión osmótica, presión de oxígeno (O2) y de dióxido de carbono (CO2).
- Fisiológicas: composición del medio de cultivo en nutrientes, metabolitos, hormonas, etc.
- Ventajas respecto a células in-vivo:
- Muestra homogénea -> buena caracterización: los clones in vitro van a ser mucho más similares entre ellos que las células que podemos encontrar en distintos individuos en la naturaleza.
- Economía experimental (vs. in vivo): por ejemplo, tener ratones en el laboratorio es más caro (comida, hábitat ... ) que tener células.
- Aspectos éticos (vs. in vivo).
Desventajas de las técnicas de cultivo celular
- Contaminaciones por microorganismos.
- Coste elevado del equipamiento y material.
- Desventajas biológicas (vs. in vivo):
- Inestabilidad de las poblaciones celulares (inestabilidad genética, desdiferenciación, selección (al final siempre escoges a las que más perduran, las que más han proliferado ... )
- Falta de control nervioso y endocrino
- Ausencia de estructura 3D y de relaciones intercelulares específicas (obtienes una monocapa de células)
- Cambios relacionados con el metabolismo energético
Características de la célula cultivada
Cultivo primario
->Cultivo primario: se obtiene a partir de células procedentes de un tejido, por disgregación (enzimática/mecánica/ química) o migración.
- son células capaces de proliferar pese a haber perdido las interacciones célula-célula y célula-matriz extracelular.
- se produce un proceso de selección.
- cuando ocupan toda la superficie disponible de la botella se dice que han alcanzado la confluencia (ejemplo: las células están al90% de confluencia)
- en esta etapa, las células establecen contactos entre ellas que inhiben su proliferación y el crecimiento se detiene.
- para mantener el cultivo es necesario transplantar las células a un nuevo soporte (diluir las en nuevo medio de cultivo y pasarlas a otros frascos) y realizar sucesivos subcultivos. En este caso se habla ya de línea celular.
Crecimiento en monocapa
-> Crecimiento en monocapa:
10% 30% 50% 90%
- Las células crecen adheridas sobre un soporte sólido (plástico o vidrio) (Cuesta al menos una noche que se adhieran, y después ya empiezan a dividirse)
- El anclaje al sustrato es un prerrequisito para la proliferación celular (pero no siempre: ejemplo, células de la sangre, u otras que son más agresivas, como las cancerígenas)
- Es el modo normal de proliferación de la mayor parte de las células con excepción de las células hematopoyéticas
Crecimiento en suspensión
-> Crecimiento en suspensión:
- Son independientes de anclaje.
- Es propio de células hematopoyéticas, células madre, de algunas líneas transformadas y de células tumorales.
Suspension culture Adherent culture B NCI-H69 200um D E NCI-N592
Morfología celular
Hay 3 morfotipos principales de células:
- Fibroblástico: muy alargadas, bipolares o multipolares. Crecen adheridas al sustrato
- Epiteliales: Células más poligonales. Dimensiones más regulares. Crecen adheridas al sustrato, formando mosaicos.
- Linfoblásticas esféricas. No necesitan anclarse, crecen en suspensión.
-> Habrá otras que según su especialización que tendrán formas especiales (por ejemplo, las neuronas)
Hay algunas células que pueden cambiar su morfología si son tratadas (artículo): Las células de la próstata con las que se trabajaba se desarrollaban y tomaban una morfología diferente al transfectarlas con In addition to the basic categories listed above, certain cells display morphological characteristics specific to their specialized role in its host. . Neuronal cells exist in different shapes and sizes, but they can roughly be divided into two basic morphological categories, type I with long axons used to move signals over long distances and type II without axons. A typical neuron projects cellular extensions with many branches from the cell body, which is referred to as a dendritic tree. Neuronal cells can be unipolar or pseudounipolar with the dendrite and axon emerging from the same process, bipolar with the axon and single dendrite on opposite ends of the soma (the central part of the cell containing the nucleus), or multipolar with more than two dendrites.un factor de transcripción (forma alargada, aspecto similar a las neuronas)
Características de la célula cultivada (continuación)
- Líneas celulares finitas: dejan de dividirse tras un número limitado de divisiones en cultivo (ej. fibroblastos, 25-40 divisiones). Superado ese límite, las células entran en una etapa que se denomina senescencia en la que pierden su capacidad de proliferar (supuestamente por el acortamiento de los telómeros) y mueren.
- Líneas celulares continuas: sufren una transformación que les hace capaces de crecer indefinidamente (ej. HeLa) [La transformación puede ser espontánea, o inducida por radiaciones, virus, agentes químicos ... ]
Continuous cell line Primary Culture Total cell yield (theoretical) Cell line 1 Transformation 1016 1st subcultre 2nd subcultre Senescence & Death Seeding Subcultural interval Serial passage 106 0 4 6 8 10 12 14 20 Weeks
La gráfica representa: En el eje Y: Numero de células (escala logaritmica). En el ejeX: tiempo Periodo de latencia (para que se adhieran al sustrato). Las vamos pasando a distintos cultivos. Primero hablamos de linea finita: la mayoria de las células sufren senescencia y mueren. Otras sufren una transformación, (o bien espontanea o bien quimicamente), y esas siguen dividiendose indefinidamente. Se crea una línea indefinida. OJO: Las inmortalizadas NO siempre son cancerosas. También puede haber líneas normales, que se dividen indefinidamente, pero que no son cancerosas. Eso es MUY importante a la hora de experimentar. Por ejemplo, has diseñado una droga que mata a las células cancerosas, pero también necesitas demostrar que no mate células sanas del cuerpo.
Características de las células transformadas in vitro
Características de las células transformadas in vitro (no deben presentar todas, pero sí tendrán la mayoría de ellas)
Relativas al núcleo
- Alta relación núcleo-citoplasma (células en procesos proliferativos altos tienen esta característica: núcleos enormes y citoplasmas pequeños)
- Alteraciones cromosómicas (en número y estructura).
Relativas a la superficie celular
- Cambios en la membrana plasmá9ca (transporte, movilidad de proteínas, aumento de blebbing). [Blebbing: membranas tienen invaginaciones, como 'burbujas'. Típico en células transformadas.]
- Cambios antigénicos, de glucoproteínas de membrana.
Alteraciones de la adherencia
- Independencia de anclaje: disminución de la necesidad de adherencia a superficies (no es necesario para empezar a proliferar)
- Disminución de la capa externa de fibronectina.
Normal Colon Colon Adenocarcinoma Increased N/C Ratio Loss of Lumen
- Desorganización de las fibras de estrés (haces de filamentos de actina).
- Aumento de la producción de proteasas y, por tanto, incremento de la proteólisis extracelular. (Van a poder invadir y migrar al tejido circundante. Cuanto más agresivo, mayor capacidad de desplazarse.)
Relativas al crecimiento y división
- No inhibición del crecimiento por densidad celular (pueden formar tumores).
- Bajos requerimientos de factores de crecimiento (Cuanto menos dependa del medio que lo rodea, mayor poder tiene)
- Inmortalidad.
- Capacidad de inducir tumores.
Cultivos histotípicos y organotípicos (cultivos 3D)
Cultivo histotípico
Cultivo histotípico (con un solo tipo celular): amplificación de un solo tipo celular en ambiente tridimensional que mimetice la estructura original del tejido-> se intentan generar cultivos 3D a partir de líneas celulares.
->Esferoides: clusters de células formadas por reasociación de células en cultivo. Pueden crecer en suspensión o en la parte superior de una matriz 3D.
Se pueden obtener por varios métodos:
- método de la superficie no adherente-› Se puede cubrir el vidrio con algo que modifique las cargas de la célula y del frasco, de modo que las células sienten repulsión contra el frasco-> No se pegan.
- cultivo en suspensión: agitación/ viscosidad del medio -> se favorece que colisionen y se reagrupen.
- método de la gota colgante
*Esferoides multicelulares (MCTS: Multicellular tumor spheroids): hoy en día también se trabaja con esferoides con más de un tipo celular. Ya no son cultivos histotípicos porque hay más de un tipo celular.
Cultivo organotípico
Cultivo organotípico: se caracterizan porque constan de varios tipos celulares que interaccionan entre sí de una forma que intenta ser lo más similar posible a la original.
Figura 1. Método de la gota colgante. a) Esferoides en la cara inferior de un vidrio circular. b) Esferoides en una placa de 96 pocillos de fondo horadado. En cada gota así creada, las células se desplazan hacia el fondo de la misma, donde forman un agregado, para originar finalmente una masa de forma esferoidal o esferoide (figura 2).
Figura 2. Esquema del desplazamiento celular durante la formación de un esferoide en el interior de una gota colgante.
- Este tipo de cultivos persigue la creación "in vitro" de tejidos u órganos completamente funcionales que puedan ser utilizados en injertos o en transplantes.
- Los cultivos organotípicos constituyen la base de la ingeniería de tejidos.