Función hepática y proteínas plasmáticas, Contraste de Fases
Diapositivas de Contraste de Fases Centro de Formación de Tel sobre la función hepática y las proteínas. El Pdf, un material de Biología de nivel universitario, detalla la fisiología del hígado, la síntesis de proteínas plasmáticas y los métodos de determinación, como Kjeldahl y Biuret.
Ver más44 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Función hepática y proteínas
Dudas en los: Foros o WhatsApp al 653 82 62 03 http://formaciontecnicolaboratorio.com/ @Contraste Fases f Contrastedefases
CONTRASTE DE FASES
Centro de formación de TEL1. Introducción: fisiología
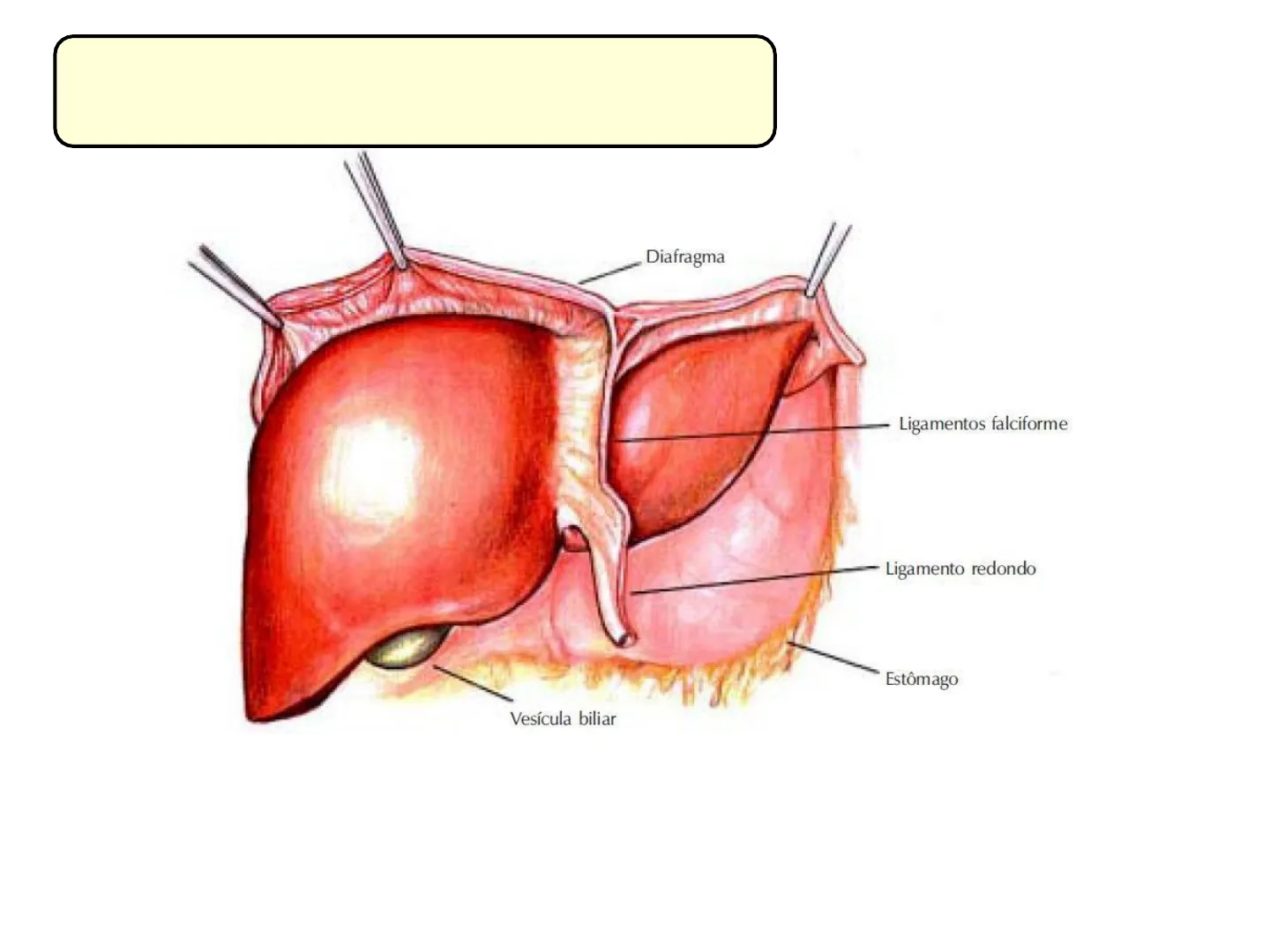
El hígado
Diafragma Ligamentos falciforme Ligamento redondo Estômago Vesícula biliar
- Viscera de mayor volumen
- Ocupa el hipocondrio derecho, gran parte del epigastrio y parte del hipocondrio izquierdo
- Está dividido anatómicamente en dos lóbulos y está recubierto por una fina capa de tejido conjuntivo denominada cápsula de Glisson.Diafragma Ligam 31 Ligamento redo Estômago Vesícula biliar Hígado
PA Acino portal Area portal (AP) CV Arteria hepática Conducto biliar PA Vena porta Lobulillo clásico CV CV Lobulillo portal Vena central (VC) PA PA PA C CV CV Lobulillo hepático Hepatocito
- La mínima unidad FUNCIONAL del hígado es ACINO HEPATICO
- La mínima unidad ESTRUCTURAL del hígado es LOBULILLO HEPATICO
- Células de Kupffer: macrófagos localizados en el hígadoFunciones
1 1
- Vasculares
- Metabólicas: hidratos de carbono, proteínas y lípidos
- Síntesis de proteínas con funciones estructurales, transportadores, tampónde pH, etc
- Síntesis colesterol, lípidos, factores de coagulación, hormonas, etc.
- Secretora y excretora
- Catabolismo de sustancias hormonales
- Almacenamiento de energía: glucógeno
- Almacenamiento de vitaminas y metales
- Función inmunológica, defensivas
- Eliminación de tóxicosPara leer ...
- Funciones Vasculares: *Formación de linfa * Almacenamiento y filtración de sangre
- Funciones defensivas: *Células Kupffer eliminan las partículas y bacterias que hayan podido entrar Por vía intestinal.
- Metabolismo de los hidratos de carbono: * Almacenamiento de glucógeno *Gluconeogénesis: formación de glucosa a partir de los intermediarios del ciclo de Krebs y la glucólisis *Conversión de galactosa y fructosa en glucosa *Formación de compuestos químicos importantes a partir de productos intermedios del metabolismo de los carbohidratos.
- Síntesis hormonas: angiotensina, triyodotironina
- Almacenamiento de vitaminas
- Almacenamiento de hierro
- Eliminación o excrección de fármacos, hormonas y otras sustancias
- Producción de las células sanguíneas durante la vida fetal (primer trimestre)
Estudio de la capacidad de síntesis hepática
- Proteínas plasmáticas Simples u HOLOPROTEÍNAS: están compuestas exclusivamente por aminoácidos. Conjugadas o HETEROPROTEÍNAS: además de por aminoácidos, están formadas por sustancias de naturaleza no proteica
- Factores de la coagulación
- Lípidos y lipoproteínas
- Urea Síntesis de la mayor parte de las proteínas. (Excepción: inmunoglobulinas, factor von Willenbrand).
Síntesis de proteínas plasmáticas
Albumin beta alfa-1 alfa-2 gamma Proteinograma: electroforesis de proteínas séricas, método semicuantitativo que nos permite visualizar el conjunto de las proteínas presentes en el suero de un paciente a través de su patrón electroforético. Una vez separadas por electroforesis, la cantidad de proteínas se determina por fotometría o por espectrofotometría (absorbancia a 200-220 nm). Las bandas del proteinograma son: albúmina, alfa 1, alfa2, beta y gamma.ANÁLISIS DE PROTEÍNAS PLASMÁTICAS POR ELECTROFORESIS EN ACETATO DE CELULOSA Preparación: Tras realizar la electroforesis: punto de aplicación corriente eléctrica tinción (-) 1 (+) - aplicación de la muestra de plasma o suero 0 + Tira de acetato de celulosa impregnada con y sus extremos sumergidos en tampón de pH básico (típicamente 8,6). Todas las proteínas plasmáticas adquieren carga negativa y por ello avanzan hacia el ánodo. globulinas y Absorbancia B Distancia avanzada mayor movilidad mayor carga negativa menor punto isoeléctrico A pH 8,6 todas las proteínas tienen carga negativa Perfil electroforético (densitograma) (proteinograma) Alb +
CONSIDERACIONES DEL PROTEINOGRAMA
- Su UTILIDAD es la detección y seguimiento de bandas monoclonales (paraproteína, componente monoclonal) que es la presencia de una inmunoglobulina anormal y/o de alguno de sus fragmentos que se dan en las gammapatías monoclonales que son un conjunto de enfermedades hematológicas, en las que hay una expansión clonal de células plasmáticas con presencia de inmunoglobulina clonal en sangre y/o orina.
- PREANALÍTICA. Se realiza en SUERO (si se hace en plasma aparece banda del fibrinogeno). Posibles interferencias (pueden simular una banda): hemolisis (banda en beta1), 1 PCR, contrastes, antibióticos, tratamientos con fármacos Ac monoclonales £
- Métodos para la DETECCIÓN (capaz de detectar componentes monoclonales de concentración igual o inferior a 1 g/L): electroforesis capilar (ligeramente mejor) y electroforesis en gel de agarosa.
- Método de CONFIRMACIÓN Y CARACTERIZACIÓN (saber qué tipo es): inmunofijación
- El seguimiento se recomienda hacer por el mismo método.
- En ORINA de estos pacientes recordar que se encuentra la proteinuria de Bence-Jones. Se puede hacer proteinograma o inmunofijacion para su detección (hay que concentrar previamente la orina unas 100-150 veces)
- DISPROTEINEMIA: alteración en la distribución de las fracciones obtenidas tras una electroforesis de suero.
Síntesis de proteínas plasmáticas
FRACCIÓN ELECTROFORÉTICA PROTEINAS FUNCIONES
PREALBÚMINA (no se aprecia apenas, no se considera banda) Prealbúmina Unión con tiroxina
ALBÚMINA Albúmina Presión coleidosmótica Transporte metabolitos hormonas Reserva proteica
ALFA 1-GLOBULINAS Alfa-lipoproteína alfa 1 glicoproteina ácida (Orosomucoide) Alfa-1-antitripsina Transcortina o globulina fijadora de corticoesteriodes (CBG) Protrombina Alfa-1-microglobulina Alfa1 fetoproteina Globulina fijadora de tiroxina (TBG) Transcobalamina Transporte de lípidos Reactante de fase aguda Inactivador de proteasas Unión con el cortisol Proenzima de la trombina Sistema inmunitario Marcador tumoral hepático Transporte tiroxina Transporte vitamina B12
ALFA 2 GLOBULINAS Ceruloplasmina Alfa-2-macroglobulina Haptoglobulina Eritropoyetina Alfa-2-lipoproteína (VLDL colesterol) Eritropoyetina Transporte cobre Inactivador proteasas (ej plasmina) Unión con hemoglobina Eritropoyesis Metabolismo lipídico Hormona eritropoyesis
BETA GLOBULINAS Transferrina (o siderofilina) Hemopexina Beta 2 microglobulina Beta-lipoproteína (LDL colesterol) Fibrinógeno, C3, C4 Fibronectina, Lactógeno placentario, sp-1-glicoproteína PCR* (puede aparecer final de beta o principio de gamma) Transporte del hierro Unión con el grupo hemo Componente HLA Metabolismo lipídico Coagulación Sistema del complemento Respuesta inmune innata
GAMMA GLOBULINAS Complemento C1q Inmunoglobulinas (OJO sintetizadas por linfocitos B y células plasmáticas, no por el hígado); algunas Ig como IgA pueden aparecer en otras bandas como beta o alfa2) Sistema del complemento Anticuerpos
Proteínas
Métodos de determinación
CUANTITATIVOS *Nefelometría *Turbidimetría Precipitación con ácido sulfosalicílico Precipitación con tricloroacético (precipita albúmina y globulinas) Precipitación gamma globulinas reactivo Kunkel zinc Método cloruro de benzetonio Etc *Espectrometría (220-280 nm) Método azul brillante de Coomassie G250 Método Lowry (reactivo de Folin) Método Rojo de Pirogalol-Molibdato Método rojo de Ponceau Método rojo de pirogalol Modificaciones del Método Biuret: el de elección Absorbancia a 280 nm Etc *Refractometría (en desuso) *Método de Kjeldahl: el de referencia
SEPARACIÓN *Electroforesis y medida absorbancia a 200-220 nm: SDS-PAGE Electroforesis capilar Isoelectroenfoque Electroforesis bidimensional Inmunoelectroforesis Etc Para determinación de proteínas individuales se utilizan inmunoensayos, especialmente INMUNONEFELOMETRÍA *Inmunoensayos *Inmunonefelometría *Inmunoturbidimetría *Inmunofijación *Inmunosustracción
Métodos de determinación de proteínas
- Método Kjeldahl : método de referencia Digestión acida, se convierte el nitrógeno en ión amonio, que se cuantifica por titulación o colorimetricamente con la reacción de Nessler
- Método de Biuret : el de elección en SUERO Los enlaces peptídicos de las proteínas reaccionan con iones cobre en solución alcalina para dar lugar a un producto coloreado que presenta un máximo de absorbancia a 540 nm. La reacción se produce con cualquier compuesto que contenga como mínimo dos grupos H2N-CH2-, H2N-C-, H2N-CS-, o grupos similares seguidos o separados por un átomo de carbono o de nitrógeno. Los aminoácidos y los dipeptidos no dan la reacción de Biuret, pero los tripeptidos ya la dan. La intensidad del color formado es proporcional al número de enlaces peptídicos que reaccionan y, por lo tanto, al número de moléculas de proteína presentes en la muestra. El reactivo de Biuret contiene tartrato sódico para mantener solubles en la solución alcalina los iones cúpricos; también lleva yoduro como antioxidante.
Métodos de determinación de proteínas (preguntas directas)
- Para determinación de proteínas individuales se utilizan inmunoensayos, especialmente INMUNONEFELOMETRÍA U J
- Para pequeñas concentraciones de proteínas (líquidos biológicos y orina): ÁCIDO TRICLOROACÉTICO (precipitación), AZUL COOMASSIE BRILLANTE (método de Bradford), ROJO PIROGALOL
- El VERDE DE BROMOCRESOL y PÚRPURA DE BROMOCRESOL es específico para la albúmina
- PONCEAU S se utiliza en electroforesis de proteínas séricas para teñir tanto albúmina como globulinas
- El método de Biuret no es óptimo para cuantificar proteínas en orina o LCR
Albúmina
- Proteína más abundante en sangre (66 % del total de proteínas)
- Vida media: 20-22 días
- Mantiene la presión oncótica intravascular o presión coloidosmótica (es una forma de presión osmótica)
- Función trasportadora
- Depósito de aminoácidos
AUMENTADA: -Deshidratación -Shock
DISMINUIDA: -Desnutrición -Enfermedad hepática -Malaabdorción -Sínd nefrótico -Quemaduras
- Los métodos que emplean verde de bromocresol y el púrpura de bromocresol utilizados en la determinación de albúmina
Recordar El Ca y el Mg van unidos en sangre a la albúmina. Una disminución de la albúmina provocará una disminución del calcio total y el Mg total (PERO NO EL IÓNICO)