Líquidos biológicos: fisiología del LCR y características de los líquidos serosos
Diapositivas de Contraste de Fases sobre Líquidos biológicos. El Pdf, un recurso de Biología para Universidad, detalla la fisiología del líquido cerebroespinal (LCR), sus funciones y la formación del plasma, incluyendo las causas del derrame pleural.
Ver más49 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Líquidos Biológicos: Fisiología del LCR
Tema 2. Líquidos biológicos
?
Dudas en los:
Foros o
WhatsApp al 653 82 62 03
http://formaciontecnicolaboratorio.com/
@Contraste Fases
f
Contrastedefases
CONTRASTE DE FASES
Centro de formación de TELLCR
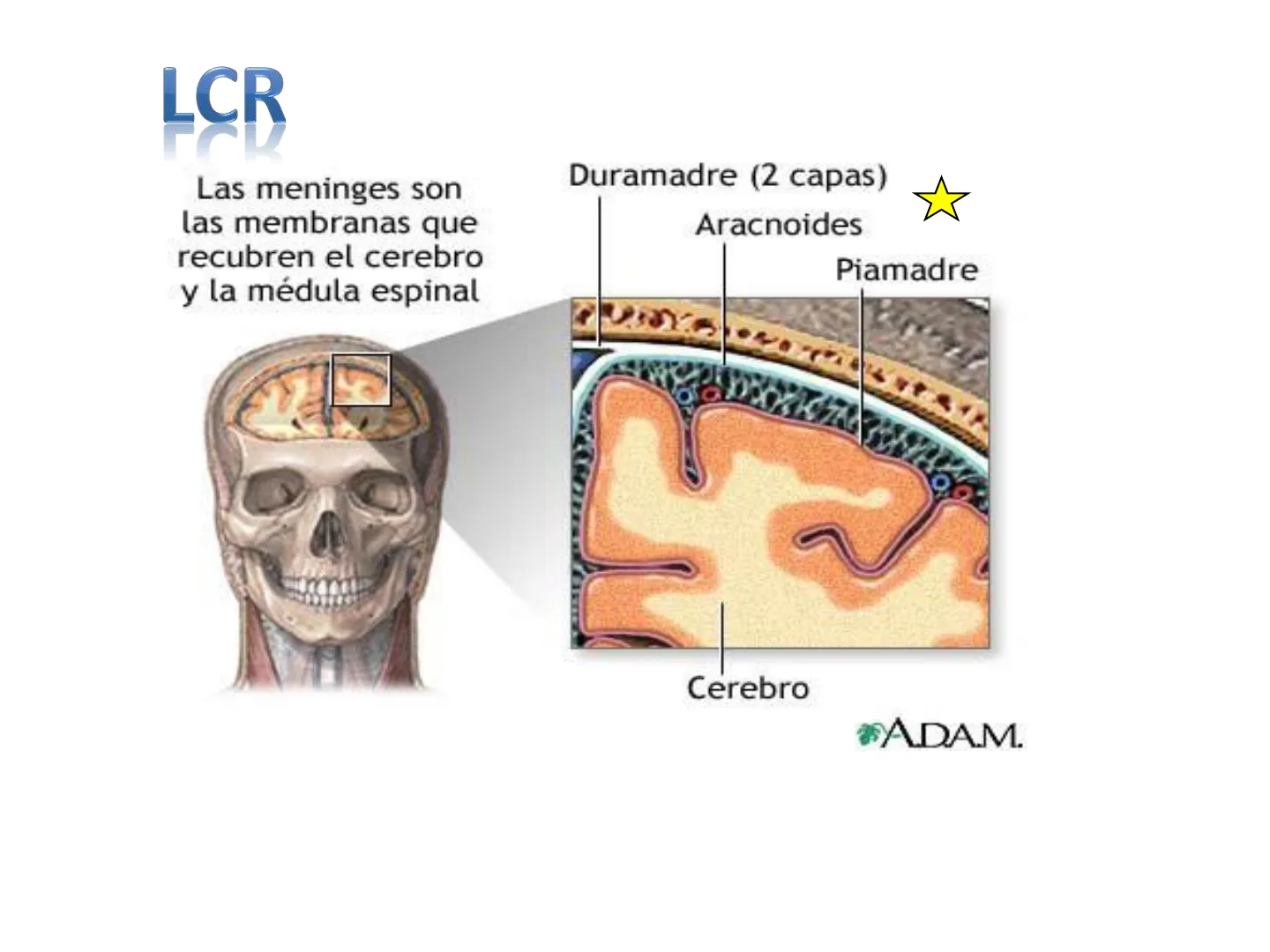
Fisiología del LCR y Meninges
Fisiología
Las meninges son
las membranas que
recubren el cerebro
y la médula espinal
Duramadre (2 capas)
Aracnoides
Piamadre
Cerebro
#ADAM.
El LCR es un medio nutriente del sistema nervioso central y es vía de excreción para
productos metabólicos del sistema nervioso central.
El LCR se encuentra en el espacio subaracnoideo, entre la piamadre y la aracnoides.LCR
Circulación del LCR
Fisiología
Plexo
choroide
Ventriculo
lateral
Espacio
subaracnoide
-
Vellosidad amacnoide
Sinus Sagital
D
Tercer
ventriculo
Acueducto
de Sylvius
Cuarto
ventriculo
Nervios
espinales
El líquido formado en los ventrículos cerebrales laterales pasa al tercer y cuarto
ventrículo, sigue hasta la cisterna magna, atraviesa los agujeros de Luschka y Magendie y
penetra dentro del espacio subaracnoideo, donde circula por los hemisferios cerebrales,
mientras que una pequeña cantidad circula hacia abajo por la médula espinal.Vista posterior de las meninges
Duramadre
Membrana aracnoide
Espacio subaracnoideo
Piamadre
Figura 1. Representación esquemática de las meninges.
Formación y Reabsorción del LCR
Epitelio coroideo
SECRECIÓN
(Na', CI, HCO2-,
Ca2+, agua)
Cilios
Aminoácidos,
bases orgánicas
Membrana
apical
Membrana
basolateral
Capilar
ABSORCIÓN
(I", CIO,, SCN,
PAH)
Figura 2. Representación esquemática de la histología de los plexos coroideos y de los
mecanismos implicados en la formación de líquido cefalorraquídeo.
LCR se forma: en los plexos coroideos (70%)
y en menor porcentaje en epéndimo (30%)
LCR se reabsorbe: vellosidades aracnoideas
Funciones del LCR
- Soporte y protección del SN
- Transporte de sustancias (hormonas, neurotransmisores, ... )
- Vehículo para la excrección de productos de la actividad del metabolismo cerebral
- Controlar las características químicas del entorno del SNCLCR
Barrera Hematoencefálica
Concepto de barrera hematoencefálica
Endothelial cell
Tight junctions
Pores
Endothelial cell
Astrocyte
Interstitial fluid
Cerebrospinal
fluid
Astrocyte
Endothelial
cell
Blood
Blood
Endothelial
cell
Proteins
Select
hydrophilic
solutes
Carrier
mediated
transport
Hydrophilic
solutes
Transcytosis
of proteins
Pore
Tight
junction
Hydrophobic
solutes
(a) Typical capillary
(b) Brain capillary
Barrera hematoencefalica: separación anatómica entre la circulación general y el espacio
cefalorraquídeo formada por el endotelio capilar, la vaina glial perivascular y la membrana pial.
Como se observa en el dibujo de la derecha, el paso de sustancias está muy restringido (unión de
membranas más estrecho, sin poros abiertos, etc)
Hydrophobic
solutes
Proteins .LCR
Extracción del LCR
Extracción
Se extrae el líquido cefalorraquídeo
de entre dos vértebras
#ADAM.
Médula espinal
,Vértebras
T1
12
Aguja
L3
L4
Líquido cefalorraquídeo
15
$1
-El procedimiento más habitual para la obtención del LCR es la punción lumbar. El paciente se coloca en
decúbito lateral, con las rodillas pegadas al pecho y el cuello flexionado de modo que queden abiertos los
espacios intervertebrales.
-La presión del LCR en adultos es de 90 - 180 mm H20 y en niños entre 10 - 100 mm H20, de manera que
de la punción sale gota a gota
-La punción se realiza entre la tercera y cuarta vértebra lumbar, o entre la cuarta y quinta vértebra
lumbar
-Otras formas de obtención son la punción ventricular y la punción cisternal (cisterna magna). Ambas
son técnicas neuroquirúrgicasLCR
Características del LCR
Características
Aspecto: transparente
Color: agua de roca
Volumen total: 100- 150 mL
Volumen intraventricular: 20-30 ml
Formación 500 ml/ día
Presión: 10-20 cm de agua
Glucosa: 45-80 mg/dl (20 mg/dl menos que en sangre)
Proteínas: 15-45 mg/dl
Células: 0-6 células/uL (todas células mononucleadas) (linfocitos)
Neonatos: 0-30 células/uL (monocitos)
Niños <4 años: 0-20 células/uL
Cloro: 120-130 mEq/l
El análisis del LCR aporta información sobre los procesos patológicos
relacionados con el encéfalo, médula y meninges y procesos
hemorrágicos producidos en las cavidades que los contienen.LCR
Condiciones Preanalíticas del LCR
Condiciones preanalíticas
La muestra de LCR debe recogerse en tres tubos estériles de forma
secuencial. No se añade conservante (tubo seco)
- Chemistry
- Serology
- Microbiology
Hematology
o el más
TURBIO (SEIMC)
Mandar al laboratorio lo más
rápidamente posible (entregar
en mano) y analizar cuanto
antes
Si no se pudiera analizar
BIOQUÍMICA: se puede congelar
CONTAJE DE CÉLULAS: refrigerada
MICROBIOLOGÍA:
Transporte y Conservación de Muestras de LCR
| Transporte | Conservación | ||
| Bacterias | Frasco estéril | ≤15 min, TA | ≤24 h, 35°℃ |
| Micobacterias | Frasco estéril | ≤2 h, TA | ≤24 h, 2-8℃ |
| Hongos | Frasco estéril | ≤2 h, TA | ≤24 h, 35ºC |
| Virus | Frasco estéril | ≤15 min, TA o 2-8℃ | ≤24 h, 2-8℃ |
| Serología | Frasco estéril | ≤2 h, TA | ≤24 h, 2-8℃ |
| Parásitos | Frasco estéril | ≤15 min, TA | |
| Detección ácidos nucleicos | Frasco estéril | ≤2 h, TA | ≤24 h, 2-8℃LCR |
Estudio Macroscópico del LCR
Estudio macroscópico
- Agua de roca
- Amarillento (xantocromía)
- Hemática
- Turbio
Hay que tener en cuenta la prenalítica: medicación, forma de extracción, etc
PUNCIÓN TRAUMÁTICA, es cuando, en el proceso de extracción del LCR antes de llegar a la zona
donde se encuentra el LCR se atraviesan capilares sanguíneos. Si esto ocurre aparecerán hematíes
procedentes de la sangre y no del LCR, en la muestra extraída.LCR
Xantocromía en LCR
Xantocromía: coloración de LCR tras centrifugación
Un líquido xantocrómico, término utilizado para describir
el LCR después de centrifugaddo, con un sobrenadante
rosado, anaranjado o de color amarillo, es indicativo de
la presencia de productos de la degradación de glóbulos
rojos, dependiendo de la cantidad de éstos presentes en
el LCR y el tiempo que han permanecido en el.
Causas: hemorragia subaracnoidea, elevados niveles
séricos de bilirrubina, carotenos, incremento de
concentración proteica, metástasis, contrastes yodados,
etc
?
?
Lisis de hematíes
Hemorragia subaracnoidea
4-6 horas
12 h
6-10 días
Diferenciación entre Punción Traumática y Hemorragia Subaracnoidea
| Determinaciones | PUNCIÓN TRAUMÁTICA | HEMORRAGIA SUBARACNOIDEA |
| ASPECTO TUBO 1, 2,3 | Desigual (se va aclarando) | Igual |
| COÁGULOS | A menudo | No se observan |
| SOBRENADANTE | Incoloro | Xantocrómico |
| ESPECTOFOTOMETRÍA | Negativo | Detección Hb, bilirrubina, etc |
Su mayor utilidad es la distinción entre punción traumática y hemorragia subaracnoideaLCR
Contaje Celular en LCR
Contaje Manual de Células
Contaje de células (hematíes y leucocitos)
Manual
Se llenan por capilaridad
Automática
NEUBAUER
IMPROVED
BRIGHT-LINE
Tiefe
Depth
Profondeur
0,100 mm
GERMANY
BLAU
BRAND
BRAND
0,0025 mm2
Cámara Neubauer
Tiefe
Depth
Profondeur
0.200 mm
0.0625mm/
Fuchs-
Rosenthal
bright-line
MARIENFELD
MAREFELD
LABORATORY GLASSWARE
1 mm
Cámara Fuchs Rosenthal
Otras cámaras de contaje: thoma,
BurkerLCR
Cámara de Neubauer para Contaje Celular
Contaje celular
Manual
NEUBAUER
IMPROVED
BRIGHT-LINE
Tiefe
Depth
Profondeur
0,100 mm
BRAND
0,0025 mm2
Cámara Neubauer
Cuando se coloca el cubreobjetos en la
cámara de Neubauer correctamente, se
observan unas irisaciones de colores
entre las dos láminas de vidrio llamadas
ANILLOS DE NEWTON
Las dimensiones de la Cámara de Neubauer son las siguientes:
1 mm de longitud
1 mm de ancho
1 x 1 x 0,1 = 0,1 mm3
0.1 mm de profundidad
1
2
3
4
5
6
7
8
9
Number of cells counted × dilution
=cells/p.L
Number of squares counted X volume of 1 square
La altura de las cámaras de Thoma y de Burker también
es de 0,1 mm. La de Funchs-Rosenthal es de 0,2 mm
Se debe contar toda la cámara porque
generalmente hay pocas célulasLCR
Diferenciación Manual de Leucocitos
Contaje celular
2. Diferenciación de leucocitos
Manual
A. Citocentrifugación
Stainless
steel
Cytoclip
slide clip
Completed assembly
Cytoslide ™
microscope
slide
Cytofunnel™ disposable
sample chamber with
attached filter card
In-load position
In operation
B. Tinción: simple (azul de metileno) o diferencial (mismos que en sangre periférica: Wright,
Giemsa, May-Grunwald, etc)
C. Visualización microscopio
En ocasiones en la diferenciación se utiliza:
Líquido de Turk. Contiene una solución hipotónica de ácido acético glacial que lisa los hematíes y azul de
metileno que mejora el contraste para contaje y diferenciación de leucocitos
Líquido de Hayem. Contiene solución isotónica de cloruro de mercurio para contaje de hematíes (lisa
leucocitos)
Líquido de Rees Ecker. (no utilizado en líquidos) se utiliza en sangre para contar plaquetas.LCR
Diferenciación Automática de Leucocitos
Contaje celular
2. Diferenciación de leucocitos
Automática
TC-BF (células totales)
DIFF
HF-BF* (células de alta fluorescencia)
Eje FL
WBC-BF (leucocitos)
MN (células mononucleares)
PMN (células polimorfonucleares)
Eos-BF* (eosinófilos)
Neu-BF* (neutrófilos)
Eje SS
Células de alta fluorescencia: relacionadas con la presencia de células
atípicas MALIGNASALGUNOS EJEMPLOS
Linfocitos y monocitos en LCR normal
Mieloblastos de una leucemia mielocítica
Neutrófilos con bacterias intracelulares
Linfocitos y monocitos en meningitis víricaLCR
Pleocitosis y Corrección de Leucocitos en LCR
Contaje celular
Normal: Adulto 0-5 células/uL
Recién nacido 0-30 células/uL
Con
predominio de células
mononucleadas
(monocitos
y
linfocitos).
El incremento de células del LCR se denomina pleocitosis
Aumento de neutrófilos : infeciones bacterianas o fúngicas
Aumento de linfocitos: infecciones víricas o fúngicas
Aumento de eosinófilos: parasitosis o inf. fúngicas
Aumento de blastos: leucemia
Nido de células: tumor, neoplasia
Si hay punción traumática, el recuento de leucocitos del
LCR se puede corregir restando los leucocitos introducidos
de la sangre (se calcula mediante una regla de 3 con el nº
de leucocitos y nº de hematíes de la sangre)
1000 eritrocitos/mm3 elevan 1-2 leucocitos/mm3
(leucocitos periféricos) x
(eritrocitos LCR)
Número de leucocitos/mm3 =
(introducidos)
eritrocitos periféricos
1000 eritrocitos/mm3 en líquido cefalorraquídeo eleva las
proteínas de 1 a 1.5 mg/dl
Tipos de Células en LCR según Patología
| Neutrófilos | Linfocitos | Eosinófilos |
| Meningitis bacteriana | Meningitis vírica | Infección parasitaria |
| Meningitis micótica incipiente | Meningitis sifilítica | Infección micótica |
| Absceso cerebral | Infección por Listeria, Leptospira | Reacción a materiales extraños |
| Empiema subdural | Infestación parasitaria SNC | Polineuritis |
| Postepilepsias | Trastornos degenerativos | Posthemorragia subaracnoidea |
| Otros trastornos inflamatorios | Postinfarto SNC | Administración de sustancias por vía subaracnoidea |
| Metástasis SNC |