Espectrofotometría: técnica fundamental en el análisis bioquímico
Diapositivas sobre espectrofotometría: una técnica fundamental en el análisis bioquímico. El Pdf explora la interacción entre radiación electromagnética y materia, delineando el espectro electromagnético y diversas técnicas espectrométricas como UV-Vis, IR, Raman y Emisión Atómica, con sus principios y aplicaciones en Química para Universidad.
Ver más59 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Espectrofotometría: Técnica Fundamental en Análisis Bioquímico
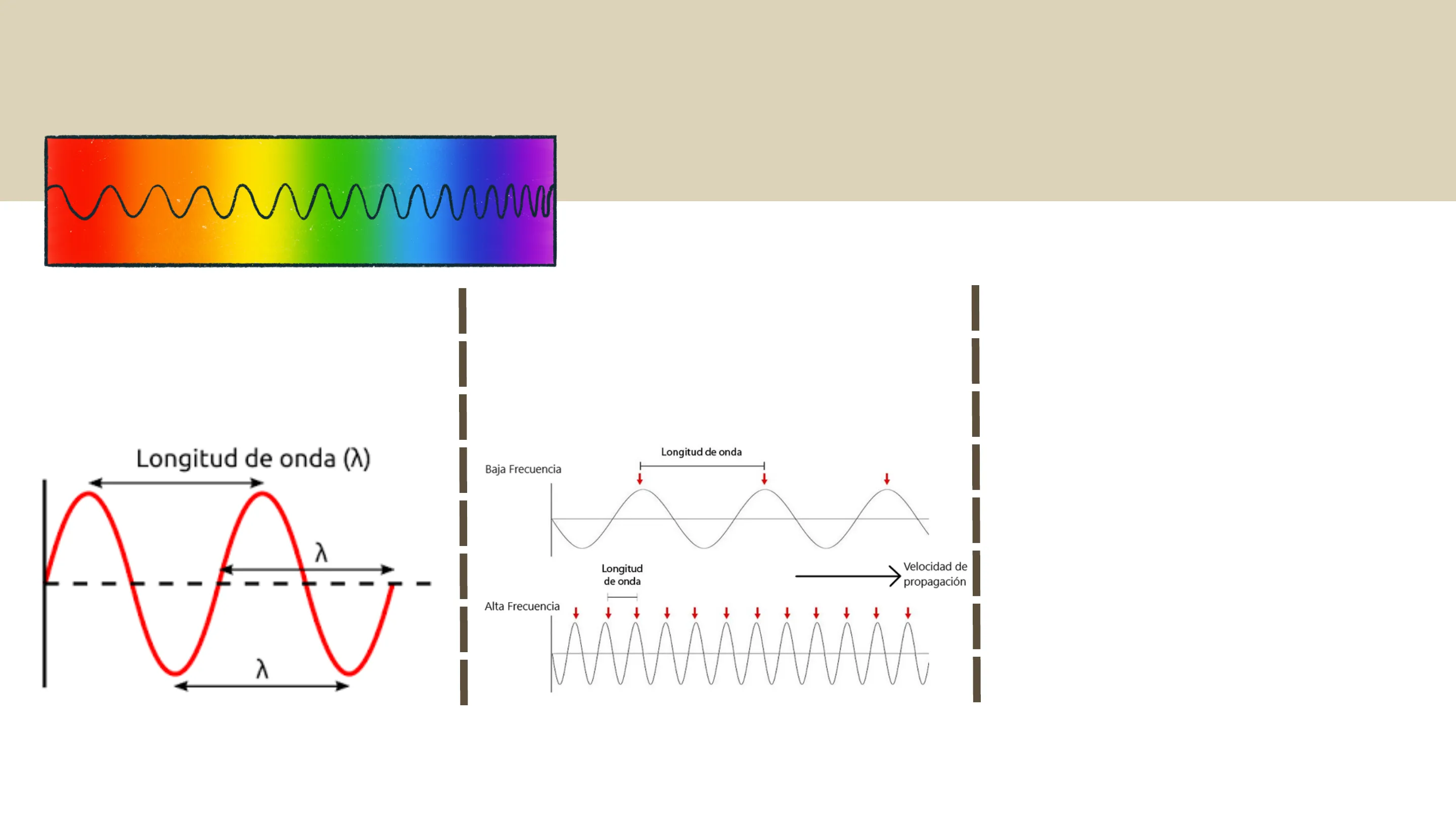
7205 Abe 0.000 100.0 $1 nm ... Read Blank Tema 2: Espectrofotometría: Una técnica fundamental en el análisis bioquímico La espectrofotometría es una técnica analítica ampliamente utilizada en los laboratorios clínicos y biomédicos. Se basa en la interacción de la radiación electromagnética (REM) con la materia, específicamente, con las moléculas. Esta interacción puede provocar la absorción, transmisión o dispersión de la luz, lo que permite la detección y cuantificación de diferentes sustancias. Patricia Encabo JENWAY 600El espectro electromagnético: Un mapa de la luz W Longitud de onda (2) Longitud de onda (2) Longitud de onda Baja Frecuencia 1 1 λ I I - Frecuencia (v) Energía (E) Longitud de onda -> Î Energía 1 frecuencia -> Î Energía Longitud de onda Velocidad de propagación Alta FrecuenciaEl espectro electromagnético El espectro electromagnético es como una "gama de colores" que incluye todos los tipos de radiación electromagnética, desde las ondas más largas, como las ondas de radio, hasta las más cortas, como los rayos gamma. Cada tipo de onda tiene una longitud de onda y frecuencia diferente, y todas viajan a la velocidad de la luz.
- Energía
+ I Tamaño de onda +
- Ondas de radio
- Microondas
- Infrarrojo (IR)
- Luz visible
- Ultravioleta (UV)
- Rayos X
- Rayos gamma
Tipos de Interacciones Radiación-Muestra
- Transmisión
- Absorción
- Emisión
- Dispersión
- Reflexión
- Difracción
- Fluorescencia Transmisión Absorción Dispersión Reflexión Refracción Difracción
Técnicas Espectrométricas
Métodos de análisis que se utilizan para estudiar cómo la radiación electromagnética interactúa con la materia.
Principales Características de las Técnicas Espectrométricas
- Tipo de radiación utilizada
- Interacción con la materia
- Información obtenida
- Concentración de sustancias en una muestra.
- Identificación de moléculas y átomos. o Estructura química y comportamiento molecular. !
Ejemplos de Técnicas Espectrométricas
- Espectroscopia UV-Vis:
- Espectroscopia Infrarroja (IR)
- Espectroscopia Raman
- Espectroscopia de Emisión Atómica
- Espectroscopia de Fluorescencia
- Espectroscopia de Resonancia Magnética Nuclear (RMN)
- Espectrometría de Masas (MS)
Espectroscopia UV-Vis
- Principio: Se basa en la absorción de luz ultravioleta o visible por la muestra. Las moléculas absorben energía y los electrones se excitan a niveles de energía más altos.
- Aplicación: Determinación de la concentración de compuestos en solución y estudios de enlaces electrónicos en moléculas.
- Uso común: Química analítica para medir la concentración de sustancias coloreadas o que absorben UV.
Espectroscopía Infrarroja (IR)
- Principio: Se basa en la absorción de radiación infrarroja por las moléculas, lo que provoca vibraciones en los enlaces químicos.
- Aplicación: Identificación de grupos funcionales en moléculas orgánicas y análisis estructural.
- Uso común: Análisis de sustancias químicas para estudiar su estructura molecular y composiciones.
Espectroscopia Raman
- Principio: Se basa en la dispersión inelástica de la luz, donde la radiación interactúa con las vibraciones moleculares y se dispersa con un cambio de energía.
- Aplicación: Determinar la estructura molecular, especialmente para compuestos que no absorben bien en el infrarrojo.
- Uso común: Caracterización de materiales y moléculas biológicas.
Espectroscopía de Emisión Atómica
- Principio: Los átomos en una muestra se excitan térmicamente (por ejemplo, en una llama o plasma), y luego emiten luz cuando vuelven a su estado fundamental.
- Aplicación: Identificación y cuantificación de elementos en una muestra.
- Uso común: Análisis de metales y otros elementos en muestras químicas o biológicas.
Espectroscopía de Fluorescencia
- Principio: Después de que una muestra absorbe radiación, emite radiación a una longitud de onda mayor (menor energía).
- Aplicación: Detección de compuestos fluorescentes en bajas concentraciones.
- Uso común: Biología molecular para etiquetar y detectar biomoléculas.
Espectroscopía de Resonancia Magnética Nuclear (RMN)
- Principio: Los núcleos de ciertos átomos (como el hidrógeno) responden a un campo magnético y absorben radiación en el rango de radiofrecuencia. Al dejar de ser irradiados, los núcleos liberan energía en forma de radiación, la cual se mide.
- Aplicación: Determinación de estructuras moleculares tridimensionales y el entorno químico de los átomos.
- Uso común: Análisis de compuestos orgánicos y biomoléculas.
Espectrometría de Masas (MS)
- Principio: La muestra se ioniza, y los iones resultantes se separan en función de su relación masa/carga mediante campos eléctricos o magnéticos.
- Aplicación: Identificación y cuantificación de compuestos y elementos.
- Uso común: Determinación de masas moleculares, estudios de fragmentación y análisis cuantitativo de mezclas.
El Espectrómetro
Instrumento que se utiliza para llevar a cabo estas técnicas espectrométricas. Es el dispositivo que mide cómo una muestra interactúa con la radiación.
Elementos del Espectrómetro
- Fuente de radiación
- Monocromador o dispersor de luz
- Cubeta
- Detector
- Muestra
Espectrometría de Absorción Molecular
Es una técnica espectroscópica utilizada para analizar la absorción de luz por moléculas en una muestra
Absorción Molecular
La absorción molecular es el proceso mediante el cual las moléculas de una muestra toman (o absorben) luz cuando esta pasa a través de ella. Este fenómeno ocurre porque las moléculas tienen la capacidad de absorber ciertas longitudes de onda de luz debido a sus estructuras internas.
Transmitancia
T= lo T (%) = 1 . 100 lo
Absorbancia
A = log 1 T = - log T A= 2 - log %T
Ley de Beer-Lambert
Describe la relación entre la absorción de luz y la concentración de la sustancia en una muestra.
A = s . b . c A: es la absorbancia (también conocida como densidad óptica). E: coeficiente de extinción molar (o coeficiente de absorción). Se mide en l/(mol.cm) c: es la concentración del soluto en la solución. Se mide en mol/l positive deviation ideal absorbance negative deviation concentration
Espectrometría de Absorción Molecular: Procedimiento
Procedimiento de la Medición
- Preparación de la Muestra: Se coloca la muestra en una cubeta adecuada y se inserta en el compartimento del espectrómetro.
- Selección de Longitud de Onda: o El monocromador selecciona una longitud de onda específica de la luz para pasar a través de la muestra.
- Medición de Absorbancia: La luz que pasa a través de la muestra se mide por el detector. La absorbancia se calcula comparando la intensidad de la luz transmitida con la intensidad de la luz incidente.
- Análisis de Datos: Los datos de absorbancia se utilizan para determinar la concentración de la sustancia en la muestra y para obtener información sobre su estructura y propiedades.
Es el instrumento utilizado en la espectrometría de absorción molecular es el espectrómetro de UV-Vis. Es un instrumento que mide la absorbancia o transmitancia de una muestra cuando se expone a radiación en las regiones del espectro electromagnético correspondientes a la luz ultravioleta (UV) y visible (Vis).
Espectrometría de Absorción Molecular: Aplicaciones
- Determinación de Concentración: Medición de la concentración de solutos en soluciones, especialmente en química analítica y bioquímica.
- Identificación de Compuestos: Identificación de compuestos químicos y análisis de estructuras moleculares mediante el estudio de sus espectros de absorción.
- Estudios de Cinética Química: Monitoreo de la velocidad de las reacciones químicas a lo largo del tiempo observando cambios en la absorbancia.
- Control de Calidad: Análisis de productos farmacéuticos, alimentos y otros productos para asegurar la calidad y pureza.
Espectrometría de Absorción Molecular: Ventajas y Limitaciones
Ventajas
Alta Sensibilidad: Puede detectar concentraciones muy bajas de compuestos. Versatilidad: Adecuada para una amplia gama de compuestos y condiciones.
Limitaciones
Interferencias: La presencia de otras sustancias puede interferir con la medición si absorben en el mismo rango de longitud de onda. Requisitos de Preparación: Las muestras deben estar en forma líquida y en una concentración adecuada para obtener mediciones precisas.
Curvas de Calibrado
Es una gráfica que relaciona la absorbancia medida con las concentraciones conocidas de una serie de soluciones estándar. Se utiliza para determinar la concentración de una sustancia en una muestra desconocida, comparando su absorbancia con la de las soluciones estándar.
Fórmula de Lambert-Beer Real
A=e.b.c+n n: absorbancia de los blancos, debería ser cero si no hay absorbancia cuando la concentración es cero.
Uso de las Curvas de Nivel
Una vez que se ha creado la curva de calibración, se puede medir la absorbancia de una muestra desconocida. Usando la ecuación de la recta de la curva de calibración, es posible calcular la concentración de la muestra desconocida. Esto se hace sustituyendo la absorbancia de la muestra en la ecuación para resolver la concentración .
Curvas de Calibrado: Construcción
Construcción Curvas de Nivel: Factor de Calibración
Cuando se cuenta con una disolución patrón (de concentración conocida, Cp) para una molécula específica (con coeficiente de extición molar, E), es posible determinar la concentración de otra disolución de la misma sustancia utilizando un factor de calibración.
Debido a que b y & Ap Am Cm p son el mismo valor
Procedimiento de Calibración: Construcción Curvas de Nivel
- Preparación de estándares: Se preparan varias soluciones con concentraciones conocidas de la sustancia a analizar. Estas concentraciones deben estar dentro del rango en el que se espera que se encuentre la muestra desconocida.
- Medición de la propiedad de interés: En espectrofotometría UV-Vis, la propiedad medida es la absorbancia de cada solución estándar a una longitud de onda específica (normalmente aquella donde la sustancia tiene su máxima absorción).
- Construcción de la gráfica: Se representa en un gráfico la absorbancia (eje Y) frente a la concentración (eje X) de las soluciones estándar.
- Obtención de la ecuación de la recta: Si la relación es lineal (como predice la Ley de Beer-Lambert), se obtiene una recta.