Propiedades de los Líquidos: Fuerzas Intermoleculares y Punto de Ebullición
Diapositivas del Tecnológico de Monterrey sobre las propiedades de los líquidos. El Pdf explora las fuerzas intermoleculares y el punto de ebullición, incluyendo definiciones clave y ejercicios. Este material de Química de nivel universitario es ideal para el estudio autónomo.
Ver más17 páginas

Visualiza gratis el PDF completo
Regístrate para acceder al documento completo y transformarlo con la IA.
Vista previa
Tecnológico de Monterrey
SESIÓN 7
TEMA 2.2 Propiedades de los líquidos
Ma. Luisa Martínez López luisa.martinez@tec.mx MODELO EDUCATIVO TEC21
Estados de agregación de la materia
¿De que depende el estados de agregación de la materia?
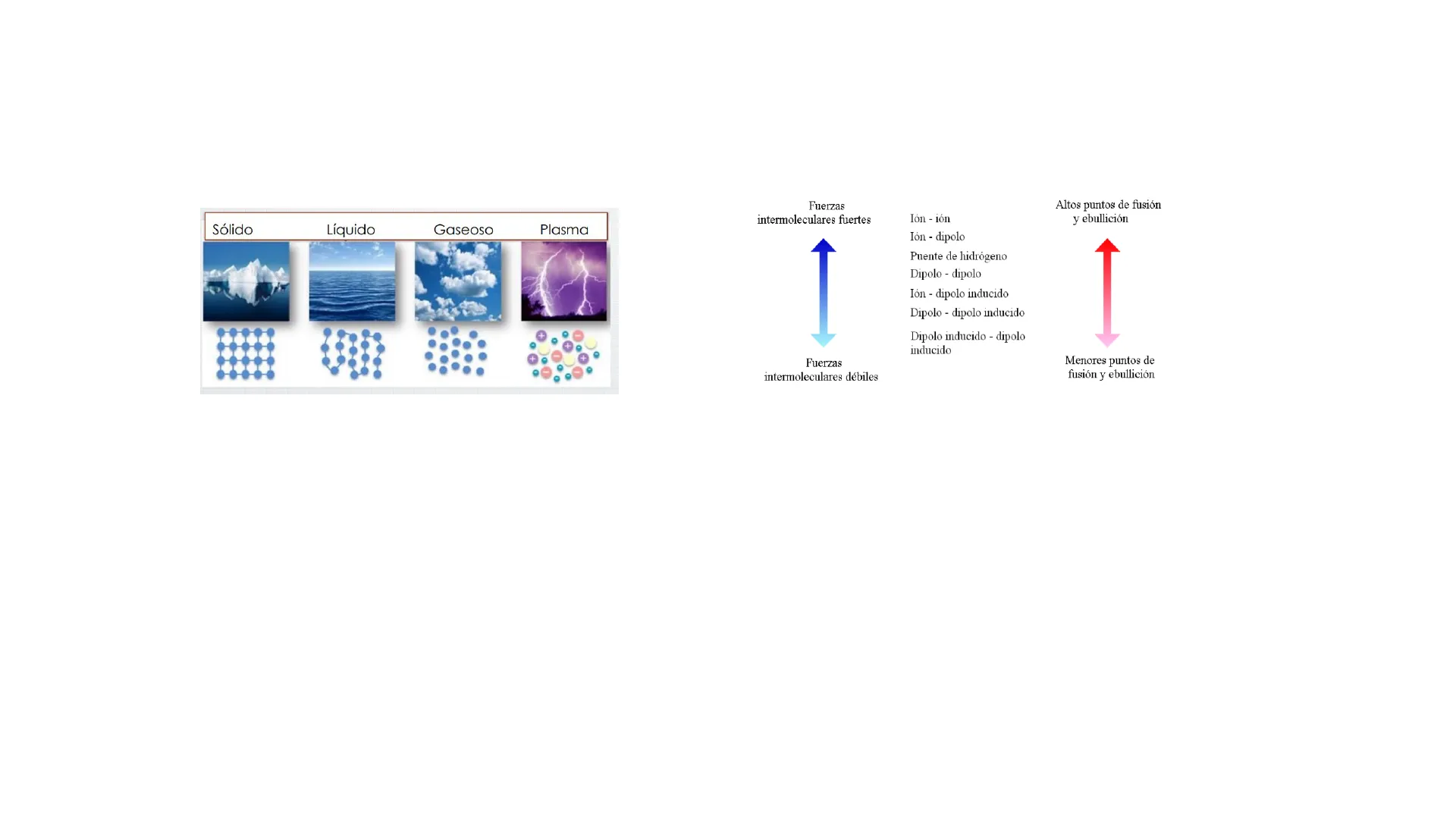
Sólido Líquido Gaseoso Plasma C
Fuerzas intermoleculares fuertes Ión - ión Ión - dipolo Puente de hidrógeno Dipolo - dipolo Ión - dipolo inducido Dipolo - dipolo inducido Dipolo inducido - dipolo inducido
Fuerzas intermoleculares débiles Altos puntos de fusión y ebullición Menores puntos de fusión y ebullición
¿Cuál de las siguientes sustancias es más probable que exista como líquido a la temperatura ambiente? a) Etano, CH3-CH3 b) Etilamina, CH3CH2NH2 c) Trifluorometano, CH3-F
2Difusión
Se presenta en líquido y en gases. Mezcla espontánea que resulta del movimiento aleatorio de moléculas al pasar de zonas de mayor concentración a otra de menor.
3Viscosidad
- Es la resistencia de un líquido a fluir.
- Un líquido fluye desplazando unas moléculas sobre sobre otras.
- Cuanto más viscoso es un líquido, más lento es su flujo.
- Se incrementa con atracciones intermoleculares fuertes.
- Puede disminuir con la temperatura.
0W-40 0W-30 5W-30 10W-30 15W-40
4Viscosidad
TABLA 11.3 Viscosidad de algunos líquidos comunes a 20℃
Líquido Acetona (C3H6O) Benceno (C6H6) Sangre Tetracloruro de carbono (CC14) Éter dietílico (C2H5OC2H5) Etanol (C2H5OH) Glicerol (C3HgO3) Mercurio (Hg) Agua (H2O)
Viscosidad (N s/m2)* 3.16 × 104 6.24 × 104 4 × 10-3 9.69 × 10-4 2.33 × 104 1.20 × 10-3 1.49 1.55 × 10-3 1.01 × 10-3
CH2-OH CH-OH I CH2-OH
5Tensión superficial
Las moléculas que se encuentran en el seno de un líquido son atraídas en todas direcciones por las fuerzas intermoleculares. Sin embargo, las moléculas de la superficie son atraídas hacia abajo y hacia los lados por otras moléculas, pero no hacia arriba de la superficie.
6Tensión superficial
La tensión superficial es una medida de la fuerza elástica que existe en la superficie de un líquido. La tensión superficial es la cantidad de energía necesaria para estirar o aumentar la superficie de un líquido por unidad de área.
Las fuerzas no se compensan (La superficie actúa como una membrana) Las fuerzas moleculares se compensan
7Tensión superficial y fuerzas intermoleculares
FUERZA INTERMOLECULAR FUERZAS VAN DER WAALS DIPOLO-DIPOLO ESPECIAL MOLÉCULA Fuerzas de London Dipolo - dipolo Puente de hidrógeno APOLAR X X P TIENE F - H O - H N - H X V R NO TIENE F - H O - H N - H V X
Sustancia Dietil éter Etanol Butanol Agua Mercurio
Fórmula CH3CH2OCH2CH3 CH3CH2OH CH3CH2CH2CH2OH H2O Hg
Tensión Superficial (J/m2) 1.7x10-2 2.3 ×10-2 2.5 ×10-2 7.3 ×10-2 48 x10-2
Fuerzas intermoleculares London enlaces de hidrógeno y London enlaces de hidrógeno y London enlaces de hidrógeno enlace metálico
8Ejercicios de viscosidad
1) Acomoda las siguientes moléculas de mayor a menor viscosidad y escribe qué tipo de interacción molecular presenta.
CH3 CH2CH2CH2CH3 CH3CH2CH2CH2CH2OH CH3CH2CH2CH2CHO H2O Pentano Pentanol Pentanal Agua
FUERZA INTERMOLECULAR FUERZAS VAN DER WAALS DIPOLO-DIPOLO ESPECIAL MOLÉCULA Fuerzas de London Dipolo - dipolo Puente de hidrógeno APOLAR X X TIENE F - H 0 O - H N - H X R NO TIENE F - H O - H N - H X
9Fuerzas de adhesión y cohesión
Las fuerzas de cohesión unen a las moléculas entre sí, es decir, son fuerzas intermoleculares. Las fuerzas de adhesión es una atracción entre moléculas distintas, es decir, unen a las moléculas a la superficie.
Adhesion Cohesion Adhesion sion H ion H 0 0 sion
10Capilaridad
La capilaridad es el resultado de estas de fuerzas de adhesión y cohesión. Cuando la adhesión es más fuerte que la cohesión, el líquido sube por el tubo capilar. Este proceso continúa hasta que la fuerza adhesiva se contrarresta por el peso del liquido en el tubo. Cuando la cohesión es mayor que la adhesión, como en el caso del mercurio, se observa una depresión del líquido en el tubo capilar.
Menisco cóncavo Menisco convexo
11Presión de vapor
Una de las características más importantes de los líquidos es su capacidad para evaporarse. No todas las partículas del líquido tienen la misma energia cinética. La presión de vapor es la presión ejercida por un vapor puro sobre su fase líquida cuando ambos encuentran en equilibrio dinámico. La presión de vapor depende de la temperatura y de la naturaleza del líquido. Cuanto más grandes son las fuerzas de atracción intermolecular, menor es su presión de vapor .
12Punto de ebullición
Un líquido en un recipiente abierto, sufre evaporación. Si la temperatura es lo suficientemente alta, se forma dentro del líquido burbujas de vapor que ascenderán a la superficie, se dice que el líquido hierve. El punto de ebullición se define como la temperatura a la cual la presión de vapor iguala a la presión externa o atmosférica.
13Factores que afectan el punto de ebullición
El punto de ebullición de un líquido depende de la presión externa a la cual esté sometido. Si la presión externa o atmosférica es baja, se necesita poca energía para que la presión de vapor del líquido iguale a la presión externa, luego su punto de ebullición es bajo.
PUNTO DE EBULLICIÓN DEL AGUA
100℃ 92°C 75℃ 35 342 35 Nivel del Mar Cd. de México Monte Everest
14Ejercicio de propiedades de líquidos
¿Cuál de las siguientes propiedades indica que las fuerzas intermoleculares de un líquido son fuertes? a) tensión superficial muy baja b) punto de ebullición muy bajo c) presión de vapor muy baja.
15Ejercicio de fuerzas moleculares
Acomoda la siguiente información según corresponda
Mayores fuerzas moleculares Menores fuerzas moleculares Viscosidad alta Viscosidad baja Alta tensión superficial Baja tensión superficial Alto punto de ebullición Bajo punto de ebullición Alta presión de vapor Baja presión de vapor
16ACTIVIDADES POR REALIZAR
PREVIAS A LA SESIÓN 8 (S4)
Q1028 Tarea 6.Líquidos (Mastering Chemistry) Lectura previa "Propiedad de los sólidos" Avance 3 de la situación problena
17