Lezione 16: Conduttometria, metodi ottici e spettroscopia in Chimica
Documento di Università sulla Lezione 16, che esplora la conduttometria e i metodi ottici. Il Pdf, utile per lo studio della Chimica a livello universitario, descrive la misurazione della resistenza con ponti di Wheatstone e Kohlrausch, la titolazione acido-base conduttometrica e introduce la spettroscopia.
Mostra di più16 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Continuo conduttometria
Come si misura la resistenza?
La resistenza si può misurare sfruttando sia il principio della corrente continua che il principio della corrente alternata. Si tratta di due ponti che prendono il nome di ponte di wenston o il ponte fi Kohlrausch: si tratta di circuiti che permettono di misurare la resistenza.
Per quanto riguarda soprattutto il secondo, si fa riferimento ad un circuito che sfrutta il confronto con una resistenza nota:
R. R G 12 A B Cursore che scorri sul filo A-B A Alimentatore di corrente Se tra A e B passa corrente, questa si ripartisce tra i 2 rami paralleli: R1 = Rx da cui: Rx = R1 . 12
Come vediamo, sotto il simbolo della G, c'è un galvanometro che smisura corrente, tale per cui se per il sistema non c'è passaggio di corrente, esso si stabilizzerà sullo 0. D'altra parte, se invece viene fatta passare una certa quantità di corrente, generata da un alimentatore, essa scorrerà tra il filo A e il B. come possiamo vedere dall'immagine, abbiamo due resistenze: una di esse è nota mentre la seconda, elemento della nostra analisi, è incognita; nel momento in cui viene fatta passare corrente tra A e B, è possibile notare lo spostamento di un cursore fino al momento in cui esso stesso si blocca. Quello che fa il cursore è dare una misura della lunghezza del filo 11 e del filo 12: 11 è proporzionale a R1 mentre 12 è proporzionale a Rx. Impostando quindi la proporzione che si legge nella parte inferiore dell'immagine, è possibile risalire alla resistenza incognita.
Ripresa della titolazione acido-base per via conduttometrica
Come abbimo detto nella scorsa lezione, durante una titolazione c'è la sostituzione di cationi e anioni, per cui la conseguenza variazione della conducibilità (+ ricordandoci che la mobilità di H+ e OH- è molto maggiore rispetto agli altri ioni). Come dicevamo, questa tecnica può esser usata soprattutto con acidi e basi forti. Avendo invece specie deboli non si può usare tale metodo.
In questo caso, in particolare con un acido debole, la curva della conducibilità si abbassa molto e, abbassandosi, risultano non più due linee verticali nette, tale per cui identificare l'intersezione è piuttosto complicato. Nel momento in cui l'intersezione ci dà il valore del volume equivalente e poiché con specie deboli non è applicabile il metodo visto fino ad ora, chiediamoci come trattare tale situazione.
Come vedremo, per determinare il volume equivalente avendo specie deboli, e quindi una curva stondata, si possono usare altri 3 possibili metodi:
- Kolthoff
- Davien - Righellato
- Righellato
Riassumendo, man mano che diminuisce la forza dell'acido, la curva è sempre più inclinata, non permettendo quindi l'individuazione del punto di intersezione, coincidente con il volume equivalente. Ecco allora che si può ricorrere a uno dei 3 metodo alternativi che vedremo, i quali ci danno la possibilità di ricavare l'intersezione ricercata. In tutti e tre i casi abbimo un acido debole ma, come vedremo ora nello specifico, si tratta di tre metodi diversi.
Metodo di Kolthoff
in questo primo caso abbiamo un acido debole e una base forte; attenzione però al fatto che in questo caso l'acido deve avere una costante di dissociazione dal valore minore di 10-5.
a) b) ml titolante p. eq.
La curva di un acido debole con base forte è la prima che vediamo, indicata con la lettera a: se avessimo solo questa non capiremmo con esattezza il volume equivalente. Per rimediare tracciamo una seconda linea, detta linea del sale: dall'intersezione delle due curve si ha la possibilità di ricavare il volume equivalente e quindi il punto equivalente.
In breve il Peq sarà dato dal punto di tangente tra la curva e la linea del sale quindi il punto equivalente sarà l'unico punto in cui il sale esiste da solo.
Metodo di Devien - Righellato
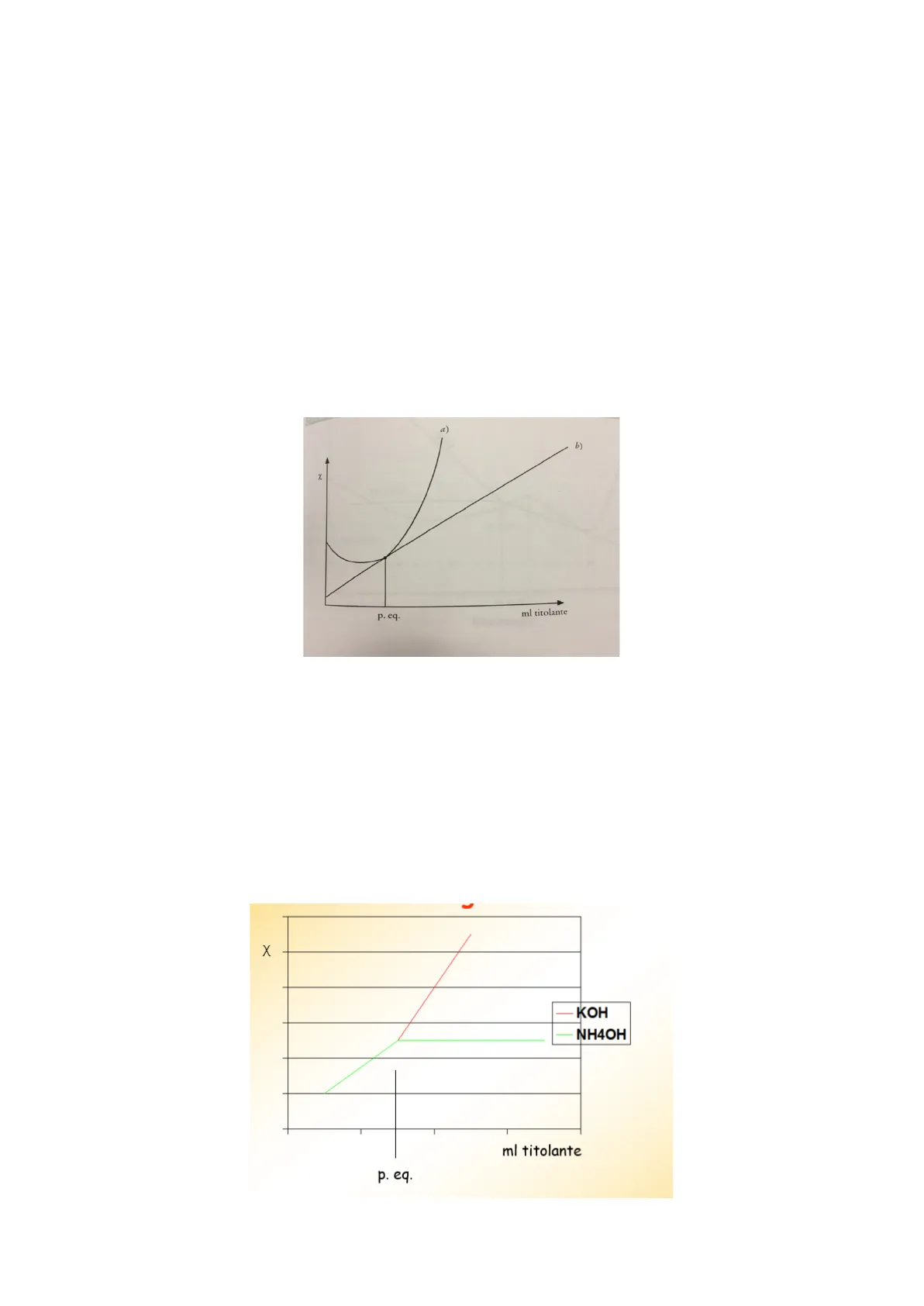
in questo secondo metodo si ha la titolazione di un acido debole ma vengono utilizzate due diverse basi, una forte e una debole. La caratteristica di tali basi è quella di avere cationi con valori della conducibilità simile tra loro.
X -KOH NH4OH ml titolante p. eq.Abbimo detto che in questo caso abbimo acido debole e due basi. Le basi qua usate sono la potassa e l'idrossido di ammonio, la prima forte e la seconda debole, caratterizzate come abbiamo detto da valori di conducibilità dei cationi simili.
Dall'osservazione del grafico possiamo notare che all'inizio si ha un tratto crescente della curva ad indicare un aumento di conducibilità: ciò avviene in ragione del fatto che abbiamo un acido debole che, sottoposto al processo di diluizione, aumenta il numero di molecole per unità di volume, tale per cui con maggiore dissociazione abbiamo maggior numero di molecole che conducono corrente. Il tutto arriva poi fino al punto in cui la curva di biforca in due. Ma perché le due curve si dividono? Ciò avviene poiché abbiamo una base forte e una debole: nel caso della forte abbimo tantissimi ioni OH- che provocano netto aumento della conducibilità. D'altra parte, nel caso dell'idrossido di ammonio, base debole, le specie OH- presenti in soluzione sono molto di meno poiché esse aumenteranno con la diluizione. Il punto in cui le due curve si dividono rappresenterà proprio il volume equivalente, e quindi il punto equivalente.
Metodo di Righellato
nel terzo metodo viene prima fatta una titolazione di un acido debole con una base debole ma, essendo questa in quantità insufficienti, segue l'aggiunta di una seconda base, stavolta base forte.
Alla soluzione in esame si aggiunge una quantità di NH4OH non sufficiente a neutralizzare completamente l'acido e poi si completa la titolazione con la soda Acido + NH4OH e acido + NaOH X Diminuz conducibilità per diversa mobilità ionica 2 cationi a: acido + NH4OH eccesso NaOH b: acido + NaOH NaOH NH4OH Sale sodico c: sale ammonico + NaOH a) +b) c) P. eq. ml titolante Titolaz con NH4OH completamento titolaz con NaOH Sostituzion NH4+ con Na+
Partiamo dall'acido debole e l'idrossido di ammonio, a cui viene aggiunta la soda. All'inizio, come al solito, abbiamo una curva che tende a diminuire sempre perché abbiamo un acido debole con pochi ioni in soluzione. A questo punto aggiungiamo in soluzione la base forte, cioè la soda: in presenza di soda abbiamo tanti ioni OH- che si dissociano, definendo un aumento della conducibilità. Il punto più alto individua il volume equivalente. A questo punto la conducibilità tende ad aumentare poiché si forma sale sodico in cui abbiamo sostituzione degli ioni ammonio con gli ioni sodio: sostituendo gli ioni ammonio con quelli sodio, possiamo vedere come lo ione sodio abbia una conducibilità minore, tale per cui si ha un'ulteriore crollo della curva.
Arrivati in questa situazione, abbiamo eccesso di soda, per cui di nuovo eccesso di OH- che di dissociano, e quindi un nuovo aumento della conducibilità, che definisce uno zig zag della curva.
Acido poliprotico
Siccome fino ad ora abbimo considerato un acido con un solo protone, ma se avessimo un acido poliprotico, cioè un acido con 2 o più protoni da dissociare definendo quindi diverse costanti di dissociazione?
n questo caso otteniamo un grafico di questo tipo, cioè con due volumi equivalenti, cioè con due punti finali, uno relativo al primo protone e uno relativo al secondo protone (in ragione del fatto che trattiamo un acido diprotico):
C acido diprotico PF, PF2 V
! è importante però ricordare che è possibile titolare un acido Diprotico, solo se è soddisfatta una condizione: il rapporto tra le due pK di dissociazione acida è maggiore o uguale a 4, ovvero: pKa1/pKa2 > 4 (quindi Ka1/Ka2 > 104)
In una situazione come questa i due equilibri si possono considerare indipendenti, cioè dissociati in modo successivo ed indipendente tra loro, e quindi si potranno rilevare due PF, relativi alla neutralizzazione dei due H: il primo relativo alla Ka1 , l'altro relativo alla Ka2.
Titolazioni con formazione di precipitato
E se volessimo titolare un precipitato? quindi il nostro obiettivo è quello di condurre una titolazione precipitometrica andando a determinare il punto finale sfruttando il metodo conduttometrico. Come facciamo?
Lo possiamo fare solo se abbiamo un precipitato che sia quantitativo, cioè solo se la quantità di reattivo in soluzione è effettivamente elevata.
Andiamo anche qua a vedere come facciamo a determinare il Peq per estrapolazione grafica:
1600 1500 0 1400 O 1300 0 1200 1100 Conducibilità 1000 0 900 800₲ 700 600 0.0 10.0 20.0 30.0 40.0 50.0 volume di soluzione titolante (ml) Titolazione conduttimetrica di AgNO3 con NaClIl grafico, come vediamo è molto al limite: per questo è necessario che i reattivi siano presenti in quantità abbastanza elevata, altrimenti non si ha la possibilità di tracciare il punto di intersezione.
Nella titolazione argentometrica dei cloruri con AgNO3 a titolo noto avviene la seguente reazione: Cl +Ag+ + NO3-> AgCI + NO3
prima del punto finale la precipitazione di AgCI elimina gli ioni CI (76,4) e li sostituisce con gli ioni NO3 (71,4), che hanno mobilità molto simile e quindi la conducibilità rimane praticamente costante (motivo per il quale la curva ha un andamento quasi orizzontale. A reazione ultimata un'ulteriore aggiunta di reattivo comporta un improvviso aumento di conducibilità, e quindi una salita brusca della curva, dovuta all'eccesso di Ag+ e di NO3 (titolante), nonché per l'eccesso di ioni presenti in soluzione.
Analisi delle acque
Con la conducibilità si misura la quantità di sali disciolta in acqua.
Più cariche sono presenti in acqua e più sali vi saranno disciolti.
Il siemens (S) e l'unità di riferimento scelta per esprimere la conducibilità dell'acqua.
In genere per valori al di sotto di 10 S l'acqua e considerata deionizzata.
Il dato di conducibilità indica quindi con immediatezza il grado di mineralizzazione delle acque.
Se il valore è alto si tratta di un'acqua ricca di sali, se è basso si tratta di un'acqua povera di sali
La conducibilità dipende dalla temperatura, perciò occorre riportare i valori alla temperatura di riferimento (20℃).
Limite di legge previsto dal D.Lgs. 31/2001: 2.500 microSiemens/cm.
METODI OTTICI
Cos'è la luce?
La luce è una radiazione elettromagnetica: nello specifico parliamo di onda elettromagnetiche perché la luce è costituita da due componenti, una elettrica e una magnetica, le quali si propagano su due piani, perpendicolari tra loro e perpendicolari alla direzione della propagazione della radiazione stessa.
Ecco quindi che la luce altro non è che una certa quantità di energia che si propaga nello spazio nel modo che abbiamo descritto.
L'energia che viene trasportata non è però mia uniformemente distribuita, bensì è concentrata in alcune zone specifiche; entriamo quindi nel campo della quantistica.
Secondo la teoria di Einstein infatti l'energia è pari al prodotto della massa per la velocità di propagazione della luce, nonché è pari al prodotto della costante di Plank per la frequenza:
Ma che cos'è la frequenza? E cos'è invece la lunghezza d'onda?
La frequenza, caratteristica fondamentale di ogni radiazione elettromagnetica, ci dà una misura del numero di oscillazioni che l'onda compie nell'unità di tempo.
D'altra parte la distanza tra i due massimi di onda viene detta lunghezza d'onda.
Tali parametri sono inversamente proporzionali () = 1/ v): se quindi un'onda ha frequenza bassa avrà lunghezza d'onda grande e viceversa.
Un'altra caratteristica della radiazione elettromagnetica è il periodo, cioè il tempo richiesto per passare attraverso due massimi d'onda.