Biologia: aminoacidi, proteine e acidi nucleici, Università San Raffaele Roma
Slide dall'Università San Raffaele Roma su Biologia. Il Pdf, pensato per l'università, esplora la materia vivente, gli aminoacidi, le proteine e gli acidi nucleici come DNA e RNA, con illustrazioni dettagliate della cromatina.
Mostra di più34 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Aminoacidi e proteine
Università San Raffaele Roma Prof. ssa Michela Montorsi BIOLOGIA Aminoacidi e proteine V Acidi nucleici: DNA e RNA 2.2 nanometri passo dell'elica = 10 paia di basi = 3.4 nanometri solco minore solco maggiore La materia vivente 1 di 34
Aminoacidi
Struttura degli aminoacidi
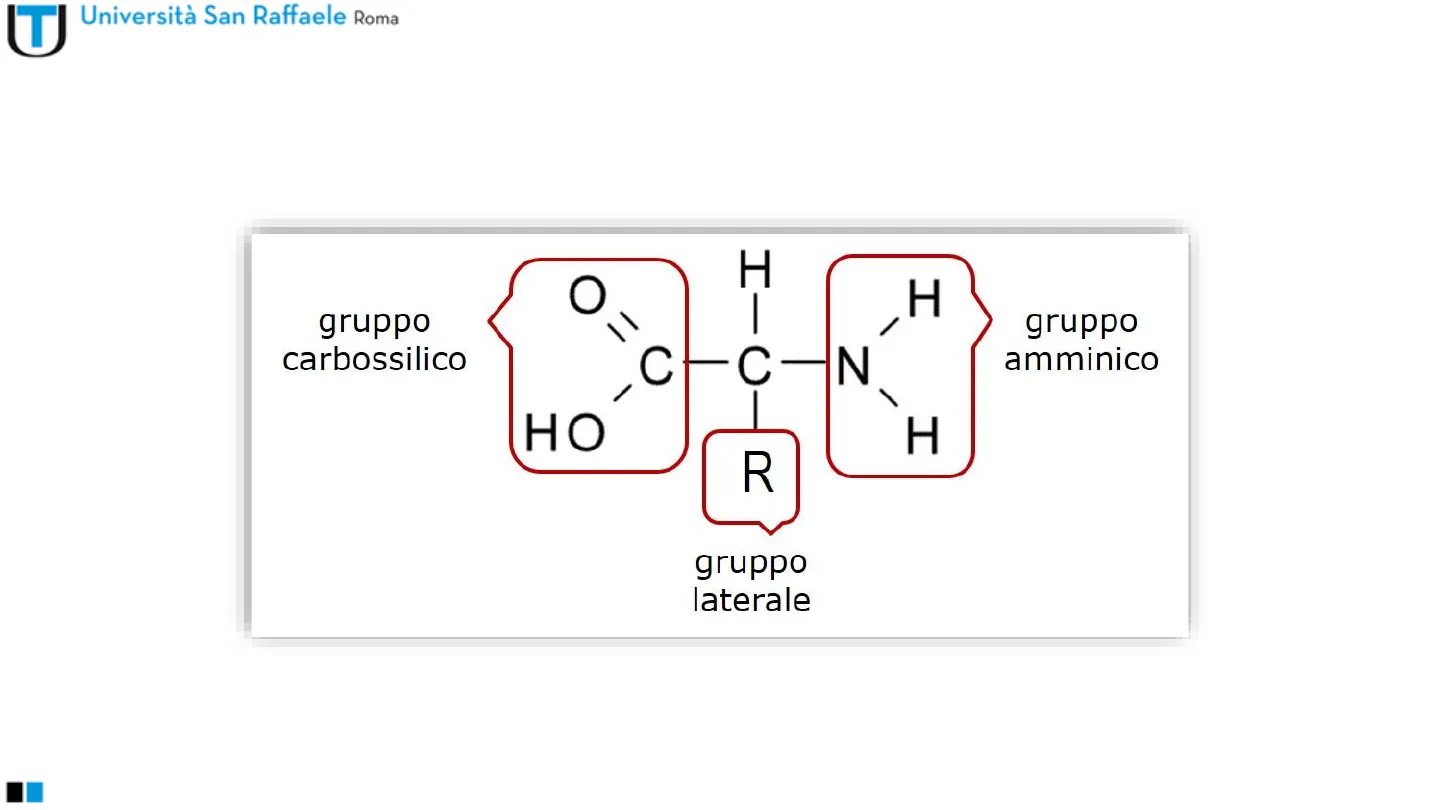
Università San Raffaele Roma Prof. ssa Michela Montorsi AMINOACIDI エ ー H gruppo carbossilico / gruppo amminico C -C-N / HO H R gruppo laterale La materia vivente 2 di 34
Catena laterale degli aminoacidi
Università San Raffaele Roma Prof. ssa Michela Montorsi AMINOACIDI Catena laterale propria di ciascun aminoacido La natura delle catene laterali conferisce proprietà diverse alle proteine in cui sono presenti
Aminoacidi carichi negativamente
CARICHI NEGATIVAMENTE O ,H ,H C-C-N C-C-N HO H HO H CH2 C , HO HO glutammato aspartato
Aminoacidi carichi positivamente
CARICHI POSITIVAMENTE H H H H O O H „H N-C-C C-C-N C-C-N `OH HO H HO H CH2 CH2 H CH2 N- NH , C I H-C = C CH2 N-C H arginina lisina istidina
Aminoacidi non polari
La materia vivente NON POLARI H H H H „H - HO H HO H - HO H CH2 alanina valina leucina metionina glicina serina treonina
Aminoacidi polari ma non carichi
H H H O H 0 H C-C-N HO H HO H CH2 HO H CH2 CH2 H_N O H_N OH asparagina glutammina エ ー H C-C-N HO H CH2 SH cisteina H H H H c-C -N C-C-N HO H HO H CH2 CH HO H OH HO CH H H H C -N C-C-N C-C-N O 1 HO H HO H CH HO H-C C - H H HN H H prolina isoleucina fenilalanina triptofano POLARI MA NON CARICHI H OS I 0=0 H $ H.C CH3 CH I- H H H H C-C-N CH2 HO CH2 C-C-N CH2 HỌC CH3 C CH3 0=0 H C-C-N c-C-N C-C-N HO CH2 C-C-N CH CH2 ,CH HỌC CH3 C-C-N H 0= H C-N. tirosina H H 1 H CH2 CH2 CH2 CH2 CH2 CH2 H_N `NH NH2 I. H I. I 0= CH2 H - 0=0 3 di 34
Classificazione degli aminoacidi
Università San Raffaele Roma Prof. ssa Michela Montorsi AMINOACIDI ESSENZIALI CONDIZIONATAMENTE ESSENZIALI NON ESSENZIALI
- Essenziali in ogni circostanza. L'organismo umano non è in grado di sintetizzarli
- Richiedono un apporto esogeno. La sintesi endogena non è sufficiente
- Sintetizzati dall'organismo in quantità sufficienti
Fenilalanina Isoleucina Leucina Lisina Metionina Triptofano Treonina Valina Istidina Arginina Cisteina Glutammina Glicina Prolina Tirosina Alanina Aspartato Asparagina Glutammato Serina La materia vivente 4 di 34
Peptidi
Formazione del legame peptidico
Università San Raffaele Roma Prof. ssa Michela Montorsi PEPTIDI H2N-CH - COOH + H2N > CH - COOH > H, N- CH - CO- NH > CH - COOH+ H2O I R R' I I R R Legame peptidico O R 1.24 A 1.46 Å 1.53 À C Ca N 0 Ca 1.32 Å Amino terminus H Carboxyl terminus - La materia vivente 5 di 34
Dettagli del legame peptidico
Università San Raffaele Roma Prof. ssa Michela Montorsi LEGAME PEPTIDICO Gruppo laterale Gruppo amminico Estremità N-terminale Estremità C-terminale R 0 - R H I-Z H H H. C OH C. H C N. C. + H2O N C H OH OH H I H ® H R Gruppo carbossilico Legame peptidico Primo amminoacido Secondo amminoacido Peptide Figura 3.17 Il legame peptidico si forma dalla condensazione del gruppo carbossilico del primo amminoacido con il gruppo amminico del secondo. La reazione è una classica reazione di sintesi disidratativa. EdiSES Wolfe, Russell Elementi di biologia cellulare EdiSES La materia vivente 6 di 34 O=U + N C C -I
Proteine
Livelli di organizzazione delle proteine
Università San Raffaele Roma Prof. ssa Michela Montorsi Met Leu Gly Pro Tyr Pro Se Glu --- a. Struttura primaria: la sequenza degli amminoacidi in una proteina Ala-Met Tyr Prof late prof Içer Ser Se b. Struttura secondaria: le regioni di una catena polipeptidica organizzate in alfa elica, foglietti beta o avvolgimento casuale Gruppo eme C. Struttura terziaria: la struttura tridimensionale complessiva assunta dalla catena polipeptidica Polipeptide della ß-globina Polipeptide della B-globina d. Struttura quaternaria: è la disposizione delle diverse catene polipetidiche in una proteina costituita da più di una catena polipeptidica Polipeptide dell'a-globina Polipeptide dell'a-globina Figura 3.18 I quattro livelli di organizza- zione nella struttura di una proteina. La proteina mostrata in (c) è una delle subunità che formano la molecola dell'emo- globina; il gruppo eme (in rosso) è un gruppo che con- tiene ferro capace di legare l'ossigeno. (d) Una molecola di emoglobina completa. Wolfe, Russell Elementi di biologia cellulare EdiSES La materia vivente PROTEINE EdiSES 7 di 34
Struttura primaria delle proteine
Università San Raffaele Roma Prof. ssa Michela Montorsi PROTEINE STRUTTURA PRIMARIA CITOPLASMA O NUCLEO aminoacidi liberi gene Catena proteica O DNA TRASCRIZIONE tRNA + aminoacido THUN mRNA TRNA Traduzione RNA ribosoma Data dalla sequenza aminoacidica > Specifica di ogni proteina Amino Acids (phe Leu Se Cvs Amino group NH2 H-C-COOH R Acidic carboxyl group R group Amino Acid La materia vivente 8 di 34
Struttura secondaria delle proteine: alfa-elica
Università San Raffaele Roma Prof. ssa Michela Montorsi a. H b. N R Gruppo laterale di un amminoacido N R c H H N- Legame idrogeno CIN R Legame idrogeno H c o H R C Legame peptidico N O c c H . N R H C o N R C R .N . C o N R c c Figura 3.20 L'o-elica, un esempio di struttura secondaria nelle pro- teine. (a) Un modello di o-elica che rappresenta gli atomi come sfere e i legami covalenti come bastoncini tra i vari atomi. La struttura portante della catena di amminoacidi è mantenuta nella sua conformazione a spirale dalla disposi- zione regolare di molti legami idrogeno. (b) Nelle rappre- sentazioni schematiche delle proteine, l'o-elica è spesso rappresentata come un cilindro. In questo caso sono mo- strati anche i legami peptidici e i legami idrogeno. I gruppi laterali si proiettano all'esterno dai lati La materia vivente STRUTTURA SECONDARIA a-elica P. N H I legami a idrogeno mantengono l'avvolgimento ad elica O H PROTEINE H I-Z 9 di 34
Struttura secondaria delle proteine: foglietto beta
Università San Raffaele Roma Prof. ssa Michela Montorsi a. Un filamento B Gruppo laterale dell'amminoacido O H B c R N C c R N C c R N C C C N c N C c R O O I legami a idrogeno tengono insieme le catene vicine nel foglietto ß-ripiegato o H H Legame idrogeno- o c N c N C c N c N c C R c c c c B H H o o Figura 3.21 Il filamento ß, un esempio di struttura secondaria nelle proteine. (a) Un singolo filamento B; la freccia è rivolta nella direzione dell'estremità C-terminale della catena amminoacidica. Nelle rappresentazioni schematiche delle proteine, la singola freccia è utilizzata per rappresentare proprio i filamenti B. (b) Un foglietto ß formato dall'allineamento fianco a fianco di due filamenti ß e mantenuto saldamente in po- sizione da numerosi legami idrogeno. La catena polipeptidica si ripiega su se stessa. La metà dei gruppi laterali è proiettata al di sopra del foglietto, l'altra metà al di sotto di esso La materia vivente 10 di 34 b. Un foglietto B formato da due filamenti B In questo foglietto B i due filamenti ₿ corrono in direzioni opposte [foglietto B antiparallelo), ma in un foglietto B i due filamenti B possono anche disporsi nella stessa direzione (foglietto ß parallelo). o B C R N C C R N C R N C c N C O N C C N R R R R c R R N N R R N R R H PROTEINE STRUTTURA SECONDARIA foglietto B 8
Struttura terziaria delle proteine
Università San Raffaele Roma Prof. ssa Michela Montorsi PROTEINE STRUTTURA TERZIARIA Dipende dalle interazione tra i gruppi laterali Legame a idrogeno Legame ionico CH2 C-NHỊ O ö C-CH2 0% CH CH2 HỌC CH3 S CH HC H HỌC CH3 CH2 HO-C CH2 Ponte disolfuro Interazione idrofobica Organizzazione tridimensionale complessiva La materia vivente 11 di 34 O S
Esempi di struttura terziaria: Lisozima e Ribonucleasi A
Università San Raffaele Roma Prof. ssa Michela Montorsi PROTEINE STRUTTURA TERZIARIA Lisozima Modello a spazio pieno di lisozima Figura 3.22 La struttura terziaria della proteina lisozima, in cui le o- eliche sono raffigurate come cilindri, i filamenti ß come frecce e le regioni ad avvolgimento casuale come linee. Il lisozima è un enzima che si trova nel muco nasale, nelle lacrime e in altre secrezioni del corpo; è in grado di distruggere la parete dei batteri poiché scompone le mo- lecole della parete. I legami disolfuro sono disegnati con tratteggio giallo. Per confronto, a fianco è mostrato un modello a spazio pieno di lisozima. Figura 3.23 Denaturazione e rinaturazione della ribonucleasi A, un enzima rilasciato nel tratto digestivo. Si noti che tutte le regioni ad ox-elica e filamento ß perdono la loro organizzazione quando la proteina è denaturata. I ponti disolfuro (in giallo) aiutano la proteina a recuperare la propria forma nativa durante la rinaturazione. (Non tutti i legami disolfuro sono mostrati in figura). a. Ribonucleasi A, forma nativa b. Forma denaturata Denaturazione Rinaturazione EdiSES Wolfe, Russell Elementi di biologia cellulare EdiSES Ld IlIdlelid viveIlle 12 di 34
Struttura quaternaria delle proteine
Prof. ssa Michela Montorsi Università San Raffaele Roma PROTEINE STRUTTURA QUATERNARIA Formata dall'unione di più catene polipeptidiche emoglobina collagene La materia vivente 13 di 34
Funzioni delle proteine
Università San Raffaele Roma Prof. ssa Michela Montorsi Anticorpi Accumulo Ormoni Strutturali DIFESA RISERVA DI MOLECOLE VEICOLANO SEGNALI REGOLATORI TRA LE CELLULE SOSTEGNO FUNZIONI PROTEINE CATALIZZATORI Enzimatiche RICEVONO SEGNALI DALL'AMBIENTE EXTRACELLULARE Recettori PROTEINE CANALE REGOLANO L'ATTIVITA' DI ALTRE MOLECOLE MOVIMENTO CELLULARE Trasporto Regolatori Motrici La materia vivente 14 di 34
Acidi nucleici
Tipi di acidi nucleici
Università San Raffaele Roma Prof. ssa Michela Montorsi ACIDI NUCLEICI 2 tipi di acidi nucleici: RNA acido desossi ribonucleico acido ribonucleico 00. O pentosio 5' base P 0 0 3' 2' HO OH = ribosio H = deossiribosio NH2 nucleoside nucleoside monofosfato (NMF) nucleoside difosfato (NDF) nucleoside trifosfato (NTF) H = citosina O H H B I R R H = uracile H = timina La materia vivente basi puriniche NH2 N N 7 80 B N NH2 I R R H =adenina O N 6 0 11 0 € A = legame glicosidico H = guanina basi pirimidiniche O 15 di 34 DNA
Componenti degli acidi nucleici
Università San Raffaele Roma Prof. ssa Michela Montorsi ACIDI NUCLEICI Gruppi fosfato 6.C. 7 N 5 C HC N1 Base azotata (è mostrata 8 C CH N 2 l'adenina) 9 3N O O O Ò- H H Zucchero (ribosio o desossiribosio) H 3. C. C2. nel ribosio HÒ nel H desossiribosio Nucleoside (zucchero + base azotata) Nucleoside monofosfato (adenosina o desossiadenosina monofosfato) Nucleoside difosfato (adenosina o desossiadenosina difosfato) Nucleoside trifosfato (adenosina o desossiadenosina trifosfato) EdiSES Wolfe, Russell Elementi di biologia cellulare EdiSES Pirimidine 0 O NH, H C H C CH3 C H N C N C N C C. N H N H N H H H H Uracile Timina Citosina Purine NH2 0 C N N N C N C-H C-H C C H Z H2N N H H Adenina Guanina Figura 3.27 Le basi pirimidiniche e puriniche dei nucleotidi e degli acidi nucleici. Le frecce rosse indicano il sito dove le basi azotate legano lo zucchero ribosio o desossiribosio per formare i nucleotidi. La materia vivente 16 al 34 NH2 I O O O O O-P-O-P-O-P-OCH2 4º C H OH H. N N H