Biosintesi dei carboidrati: gluconeogenesi e meccanismi di regolazione
Documento sulla biosintesi dei carboidrati, focalizzandosi sulla gluconeogenesi e i suoi precursori. Il Pdf di Chimica, adatto per l'Università, analizza i meccanismi di regolazione che coinvolgono l'ATP e il glucagone, illustrando i processi biochimici con diagrammi esplicativi.
Mostra di più34 pagine

Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
Biosintesi dei Carboidrati
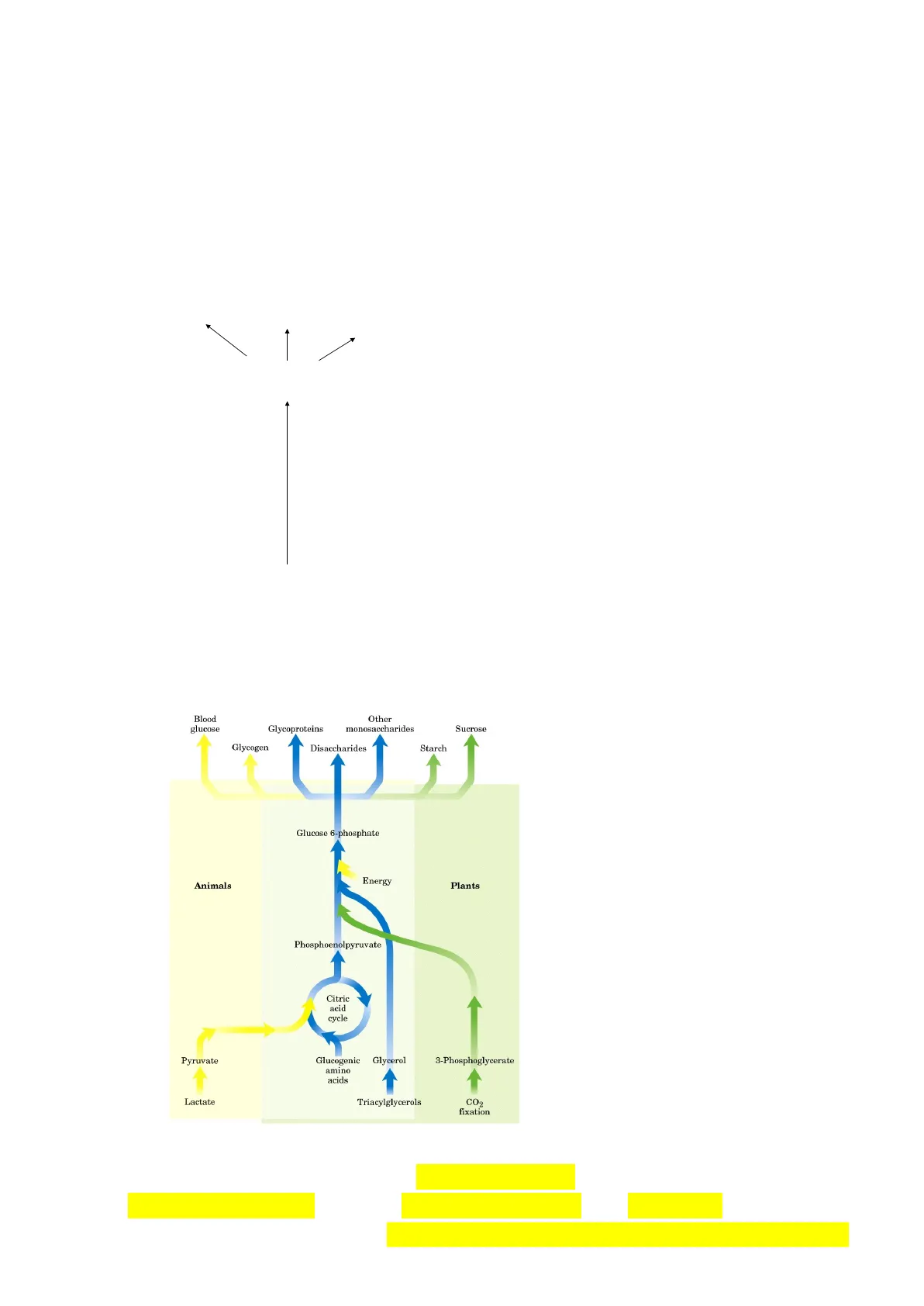
Biochimica BIOSINTESI DEI CARBOIDRATI Glicogeno Glucosio .. Glucosio-6P Gluconeogenesi (nel fegato) Precursori non saccaridici Sintesi di carboidrati da precursori semplici Blood glucose Other monosaccharides Glycoproteins Sucrose Glycogen Disaccharides Starch Energy Animals Plants Phosphoenolpyruvate Citric acid cycle Pyruvate Glucogenic amino acids Glycerol 3-Phosphoglycerate Lactate Triacylglycerols CO2 fixation
La sintesi del glucosio prende il nome di gluconeogenesi, e la sede in cui questo processo avviene è il fegato, il quale produce il glucosio che distribuirà poi attraverso un torrente circolatorio agli altri organi (il cervello, il cuore, il muscolo, il rene e altri organi), che lo consumano.
Precursori della Gluconeogenesi
Glucose 6-phosphateAvviene a partire da precursori semplici e non saccaridici, in genere molecole piccole convertite in glucosio 6-fosfato, che sarà un buon punto di partenza per la sintesi di glucosio, glicogeno e di altri carboidrati.
(per fare gluconeogenesi stessi enzimi della glicolisi + altri ... )
Di seguito sono elencati i principali precursori semplici del glucosio:
- Il lattato: il muscolo quando si contrae produce il lattato, il quale va nel fegato, che lo riconverte in glucosio per venir poi trasferito al muscolo. Il muscolo manda via un prodotto di "scarto" e in cambio riceve glucosio. Il vantaggio è che i costi energetici per la sintesi del glucosio sono a carico del fegato e non del muscolo. Il lattato viene convertito in piruvato, che viene convertito in ossalacetato che è il punto di partenza per la sintesi del glucosio-6- fosfato. Il glucosio 6-fosfato può servire poi per produrre glucosio che viene immesso nel sangue, glicogeno, glicoproteine, disaccaridi, altri monosaccaridi, e nelle piante anche amido e saccarosio.
- Altri precursori sono gli amminoacidi glucogenici. Infatti, alcuni amminoacidi possono servire per produrre glucosio. Tanto è vero che nel digiuno protratto si demoliscono le proteine ottenendo questi scheletri carboniosi che possono essere inviati nel ciclo di Krebs o essere precursori dell'ossalacetato che serve per fare il glucosio. Gli amminoacidi glucogenici sono quelli che una volta deaminati permettono ai loro scheletri carboniosi di entrare nel ciclo di Krebs o quelli che in qualche modo possono generare piruvato.
- Il glicerolo è il prodotto dalla degradazione dei trigliceridi (tessuto adiposo) insieme agli acidi grassi. Gli acidi grassi, però, non possono essere utilizzato per la sintesi del glucosio. Perché questi ultimi per entrare nel ciclo di krebs dovrebbero essere demoliti a gruppi acetilici con la beta-ossidazione e entrare sotto forma di acetil-CoA. Ma l'acetil- CoA subentra 2-3 tappe dopo quando il CO2 che esce e, dato che gli atomi di C del gruppo acetile sono due, essi fuoriescono sotto forma di CO2 quindi non ci sarebbe più C per costruire glucosio. Invece il glicerolo può essere convertito in diidrossiacetone fosfato ed entrare nella via gluconeogenica, producendo glucosio.
- Le piante sono capaci di sintetizzare glucosio a partire da CO2 e acqua, perché sono in grado di svolgere la fotosintesi e il ciclo di Kelvin, che consente loro di sintetizzare i precursori per poi fare la sintesi dei carboidrati.
Bypass nella Gluconeogenesi
Primo bypass 1,3-Bisphosphoglycerate ADP ADP ATP ATP Glycolysis pathway Gluconeogenesis pathway 2-Phosphoglycerate 1 Phosphoenolpyruvate CO2 GDP GTP ADP Oxaloacetate NADH ATP MDH NAD+ Malate Malate First bypass NAD+ MDH NADH Oxaloacetate acetyl-CoA ADP CO2 ATP Alanine Pyruvate Pyruvate Alanine
In questa immagine in discesa è rappresentata la glicolisi (demolizione glucosio), mentre in salita è rappresentata la gluconeogenesi (biosintesi del glucosio). Tutte le frecce grigie indicano la glicolisi e si nota che si alternano frecce singole e doppie. Ad esempio, nel passaggio dal glucosio al glucosio-6-fosfato c'è una freccia singola che indica che la reazione è irreversibile. In totale nel processo abbiamo tre reazioni irreversibile con l'equilibrio spostato verso destra. Mentre tutte le altre tappe che hanno doppia freccia, quindi sono reversibili, sono in comune sia nella glicolisi che nella gluconeogenesi. Per eseguire il percorso al contrario, quindi in salita, questi passaggi essendo irreversibili non possono essere percorsi per cui servono dei bypass.
PEP CO2 PEP carbossichinasi OSS. OSS. PIR CO2 PIR carbossilasi/biotina (allosterico) (reaz anaplerotica) 3-PhosphoglycerateBlood glucose Glycoproteins Other monosaccharides Sucrose Glycogen Disaccharides Starch Glucose 6-phosphate Animals Energy Plants Phosphoenolpyruvate Citric acid cycle Pyruvate Glucogenic amino acids Glycerol 3-Phosphoglycerate Lactate Triacylglycerols fixation
Ci sono tre reazioni nella via della glicolisi che consumano energia, esoergoniche e irreversibili, dove sono necessari dei bypass:
- Primo bypass, il piruvato può venir convertito in fosfoenolpiruvato non con una sola reazione come nella glicolisi, ma con tante, e con un grande consumo di energia che serve a superare questo salto energetico.
(Nel citosol deve abbondare Nad+ e nel mitocondrio NADH) (quando serve il glucosio? Quando siamo sotto sforzo oppure quando ce n'è poco, Il muscolo produce lattato se sei allenato il lattato va nel fegato che lo sfrutta per fare il glucosio) Fase di recupero da sforzo bruci grassi per ottenere ATP che servirà al ciclo di KREBS che non lo alimento con glucosio, ma con grassi
- Secondo bypass, si trova a livello della fosfofrutto-chinasi, in cui una fosfatasi consente di superare il secondo salto energetico.
Quando esce un gruppo fosfato c'è un delta G favorevole e non serve ATP
- Terzo bypass, un'altra fosfatasi consente di convertire il glucosio 6-fosfato in glucosio.
Le tre tappe irreversibili della glicolisi sono sostituite da altre tappe ugualmente irreversibili. Di conseguenza, anche la gluconeogenesi è un processo spontaneo: anche le vie anaboliche sono spontanee. La gluconeogenesi avviene nel citosol (in questo caso degli 6 epatociti), dove avviene anche la glicolisi.
Il fegato deve fare entrambe le vie, quindi glicolisi e gluconeogenesi saranno strettamente collegate.
Dettagli del Primo Bypass
Nel primo bypass il piruvato può entrare nei mitocondri e venir convertito in ossalacetato [avevamo già parlato di conversione del piruvato in ossalacetato quando avevamo parlato di reazioni anaplerotiche nel ciclo di Krebs (reazioni che servono a ripristinare il ciclo di krebs degli intermedi sottratti per le biosintesi). La reazione è catalizzata dall'enzima piruvato carbossilasi, entra CO2 e serve ATP. L'ossalacetato viene poi convertito in malato (reazione del ciclo di Krebs) dall'enzima malato deidrogenasi mitocondriale. Mentre nel ciclo di Krebs la reazione è all'equilibrio e produce NADH, qui si consuma NADH per ottenere malato, il quale può uscire dal mitocondrio e andare incontro alla reazione opposta a quella che è avvenuta all'interno del mitocondrio (da malato a ossalacetato). Il NADH servirà per una tappa che sta più in alto. Abbiamo portato fuori dal mitocondrio una molecola di ossalacetato, che può essere convertita in fosfoenolpiruvato dalla fosfoenolpiruvato carbossichinasi (reazione del ciclo di Krebs al contrario). Avevamo già visto che è possibile produrre fosfoenolpiruvato dall'ossalacetato, ma è possibile anche la reazione opposta. Se avviene al contrario, ci sarà un consumo di GTP. Siamo passati da una molecola relativamente povera di energia (piruvato) a una relativamente ricca di energia (fosfoenolpiruvato). Con il primo bypass è stata superata la prima barriera energetica a spese di una molecola di ATP, di GTP e in più è stata portata fuori dal mitocondrio una molecola di NADH. Un'altra cosa da osservare è che il passaggio da piruvato ad ossalacetato comporta il passaggio da una molecola a 3 atomi di C a una molecola con 4 atomi di C, questi atomi vengono forniti dalla CO2. Noi non siamo in grado di fissare il carbonio della CO2, mentre le piante sì. Infatti, se entra una molecola di CO2, ne esce sempre una. La via procede sfruttando esattamente le stesse reazioni della glicolisi (ma al contrario): dal fosfoenolpiruvato al 2-fosfoglicerato, al 7 3-fosfoglicerato, e infine al 1,3- bifosfoglicerato. Mentre glicolisi si consuma NAD+, nella gluconeogenesi si consuma il NADH. Inoltre, nella glicolisi questa via produceva ATP, mentre qui esso viene consumato.
Ciclo di Krebs e Reazioni Anaplerotiche
Il ciclo di Krebs è una via anfibolica (catabolica e anabolica) Pyruvate Glucose I Fatty acids, sterols pyruvate carboxylase Acetyl-CoA PEP carboxykinase Oxaloacetate Citrate Phosphoenolpyruvate (PEP) PEP carboxylase Nei batteri Glutamine Proline Arginine 1 Malate a-Ketoglutarate Glutamate Serine Aspartate Asparagine Glycine malic enzyme I Cysteine Purines Phenylalanine Pyrimidines Pyruvate Tyrosine Tryptophan Porphyrins, heme Reazioni anaplerotiche (rosso): vie che riforniscono il ciclo degli intermedi sottratti per le varie sintesi
Le due vie anaplerotiche del ciclo di Krebs sono il piruvato carbossilasi e la fosfoenolpiruvato (PEP) carbossilasi. Il ciclo di Krebs è una via anfibolica (sia catabolica che anabolica) e gli intermedi possono essere sottratti per fare biosintesi. Ma essendo un ciclo, senza questi intermedi, non potrebbe più girare, per cui serve qualcosa che vada a "ripristinare" questi ultimi. Le reazioni che si occupano di ripristinare gli intermedi prendono il nome di reazioni anaplerotiche, ed erano 4. Due di queste reazioni sono quelle appena descritte e servono per ottenere l'ossalacetato essenziale per la biosintesi del glucosio.
Confronto Glicolisi e Gluconeogenesi
Glicolisi Gluconeogenesi Consumato subito PEP AGO = - 31,4 KJ/mol AGº = 0.9 KJ/mol AG = - 25 KJ/mol GTP ATP ATP PIR irreversibile irreversibile Esia glicolisi che gluconeogenesi hanno delta G negativo, quindi con .... Succinyl-CoAIl primo bypass il passaggio da PEP a piruvato è fortemente esoergonica con produzione di ATP e G standard =- 31,4 KJ/mol (se deltaG è negativo vuol dire che la reazione è spontanea ed è talmente spostata verso destra che questo passaggio in discesa serve per produrre ATP). La freccia in blu invece rappresenta la via percorsa in salita della gluconeogenesi. Vediamo che da piruvato a fosfoenolpiruvato si consuma una molecola di ATP e una di GTP. II G standard in questo caso è -25 KJ/mol; quindi, anche nel caso della gluconeogenesi G è negativo, per cui il processo è irreversibile e spontaneo. Tutto ciò è reso possibile dall'accoppiamento energetico, l'accoppiamento dell'ATP e GTP. Inoltre, vediamo che il fosfoenolpiruvato che si genera viene subito consumato dalle tappe che sono sopra. Consumando il fosfoenolpiruvato si trascina la reazione verso destra. Questa è la ragione reale per cui il deltaG diventa -25 KJ/mol, se andassimo a considerare il deltaG standard sarebbe solo 0,9 KJ/mol.
Ruolo del NADH nel Mitocondrio
QUAL'E' LA RAGIONE PER CUI BISOGNA PORTARE FUORI IL NADH DAL MITOCONDRIO? La concentrazione di NADH nel citosol è bassa, mentre è alta nel mitocondrio perché al suo interno avvengono reazioni che necessitano di questa molecola come il ciclo di Krebs (che produce molto NADH). Non è solo il ciclo di Krebs a produrre NADH. Anche durante la beta-ossidazione e la demolizione degli aminoacidi nel processo di deaminazione ossidativa viene prodotto il NADH. Mentre il NADH per la biosintesi del glucosio serve nel citosol, quindi serve un meccanismo di trasporto. Viene sfruttato il meccanismo che abbiamo visto quando nella glicolisi si produce NADH, e quel NADH per portare i propri elettroni sulla catena respiratoria, deve essere portato dentro. Quindi quando la cellula deve fare la biosintesi del glucosio questo meccanismo va al contrario e il NADH viene portato fuori. Quindi il sistema della malato deidrogenasi citosolica serve a questi due scopi, per cui il passaggio del NADH dipende dalle necessità metaboliche.