Cromatina: organizzazione, compattamento del DNA e tecniche epigenetiche
Slide di Università sulla cromatina, la sua organizzazione e i vari livelli di compattamento del DNA. Il Pdf descrive le tecniche epigenetiche, con un focus sull'analisi della metilazione del DNA, ed è utile per lo studio della Biologia a livello universitario.
Mostra di più15 pagine
Visualizza gratis il Pdf completo
Registrati per accedere all’intero documento e trasformarlo con l’AI.
Anteprima
CROMATINA
Dal punto di vista spaziale, la molecola di DNA è lunga più di 1 mt ed è formata da circa 3 * 109 basi azotate. Questa molecola è contenuta all'interno del nucleo, con diametro di circa 5um; l'alloggiamento del DNA nel nucleo è permesso in quanto il DNA stesso subisce un compattamento di circa 10'000 volte.
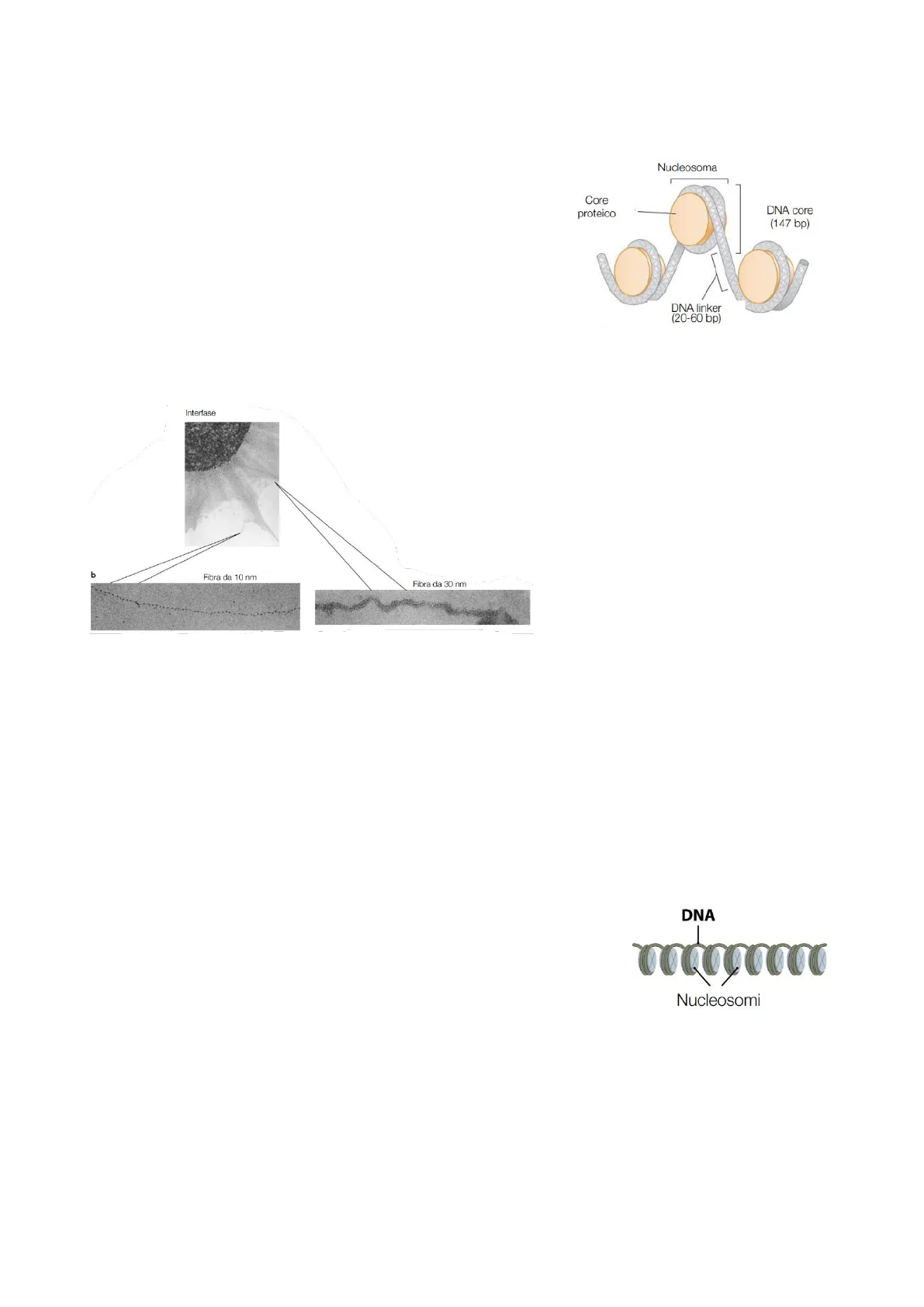
Nucleosoma Core proteico DNA core (147 bp) DNA linker (20-60 bp)
Utilizzando la microscopia elettronica è possibile rilevare fibre di DNA presentanti diversi gradi di compattamento:
Interfase b
Fibra da 10 nm
Fibra da 30 nm
- il primo livello di compattamento, ossia quello base, del DNA è rappresentato dalla fibra a 10 nm;
- il secondo livello di compattamento è rappresentato dalla fibra a 30 nm;
- l'ultimo grado di compattamento del DNA è rappresentato dal cromosoma.
Durante l'interfase le tre forme coesistono; successivamente si avrà la predominanza del compattamento cromosomico, il quale permette di fatto che la lunga molecola di DNA sia contenuta nel piccolo spazio nucleare.
GRADO DI COMPATTAMENTO
NUCLEOSOMA- FIBRA A 10nm
Il nucleosoma è l'unità strutturale fondamentale della cromatina. È il primo livello d'impacchettamento del DNA con un rapporto di compattamento di 6 volte; di fatto l'avvolgimento del DNA attorno ai nucleosomi rappresenta la fibra a 10 nm. Questa conformazione della cromatina è anche detta a collana di perle.
DNA Nucleosomi
Il complesso ha una lunghezza di 6nm e un diametro di 11 nm.Strutturalmente il nucleosoma è formato da un core proteico, attorno il quale il DNA ci si avvolge per circa 1,65 volte. Il DNA che si avvolge attorno al nucleosoma è detto DNA core, lungo 147 bp, mentre il DNA che non si complessa col nucleosoma è detto DNA linker, con lunghezza variabile dalle 20 alle 60 bp.
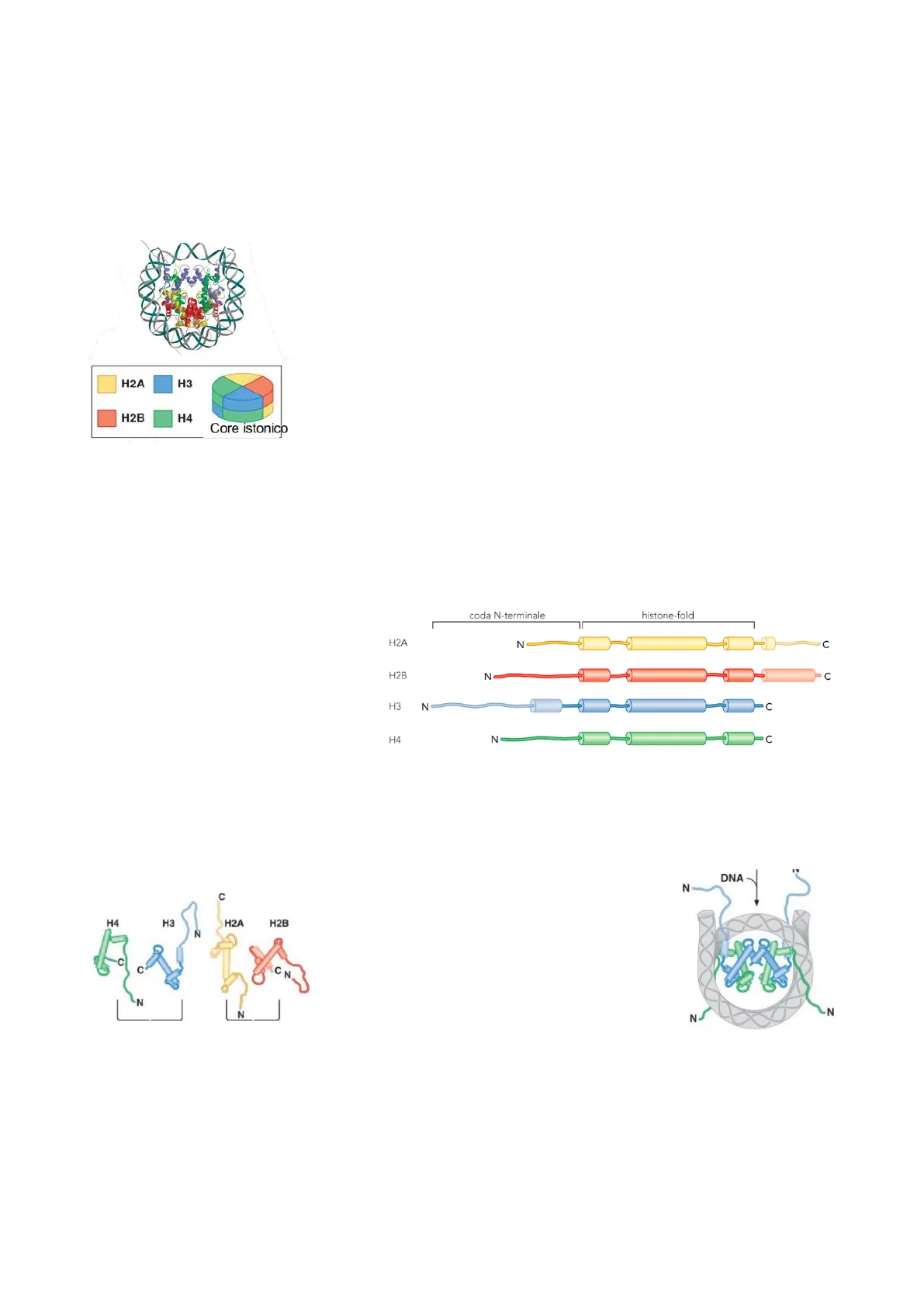
H2A H3 H2B H4 Core istonico
Il core proteico è formato da 8 proteine dette istoni, le cui sequenze amminoacidiche sono altamente conservate nell'evoluzione a causa del ruolo fondamentale che ricade sulla proteina stessa. La maggior parte degli amminoacidi istonici interteragiscono col DNA o con altre proteine istoniche.
Nelle 8 proteine formanti il core, se ne possono distinguere 4 tipologie, presenti con quantità doppie: si ha H2A, H2B, H3 e H4; il core istonico prende anche il nome di ottamero.
Gli istoni, oltre che avere un peso molecolare estremamente simile tra di loro, presentano un alto contenuto di aa basici, quali lisina e arginina, in quanto il DNA ha un carattere negativo.
Similitudini possono trovarsi anche nell'organizzazione strutturale; gli istoni presentano infatti:
- un dominio C-terminale;
- un dominio centrale, fondamentale per il folding del complesso;
- un dominio N-terminale, dove avvengono per lo più la maggior parte delle coda N-terminale histone-fold H2A N C H2B N C H3 N C H4 N C interazioni col DNA in quanto meno strutturato rispetto agli altri domini.
ASSEMBLAGGIO NUCLEOSOMA
La formazione del core istonico prevede più passaggi.
Il primo passaggio consiste nella H4 H3 H2A H2B formazione di due dimeri diversi: dimero N H3-H4 e dimero H2A-H2B. C CN Successivamente il dimero H3-H4 si lega IN ad un altro dimero a formare il tetrametro N H3-H4. È proprio al livello di questo tetramero che si avrà un primo legame col DNA.
DNA N NJ N CUna volta istaurato questa interazione, si ha il legame dei dimeri H2A-H2B a formare l'ottamero istonico, sul quale è avvolto il DNA.
N N N N N
FIBRA A 30 nm
È il livello successivo di impacchettamento della fibra a 10 nm; questo livello successivo è raggiunto in quanto vi è il legame dell'istone H1 al DNA linker, ossia quella porzione di DNA compresa tra i nucleosomi. Con H1 aumenta la lunghezza del DNA arrotolato attorno alla struttura proteica.
H1
In particolare, H1 prende contatti sia con il DNA linker che con gli istoni del core, permettendo l'avvicinamento dei nucleosomi stessi a formare una fibra solenoide di diametro 30nm.
DNA nucleosoma core istonico DNA linker zigzag DNA linker
Questa conformazione è il secondo livello d'impacchettamento del DNA, con un rapporto d'impacchettamento di 40 volte.
La modalità con la quale si forma strutturalmente questa fibra non è ancora ben chiaro; sono stati proposti due modelli: a solenoide e a zigzag.
fibra 30 nm
La fibra a 30nm è stabilizzata grazie alle code istoniche all'N- terminale, che mediano le interazioni tra nucleosomi. È da sottolineare come modificazioni post-traduzionali sulle code istoniche influenzano la capacità di formazione della fibra di 30 nm.
FIBRA CROMATINICA
Rappresenta un'ulteriore condensazione della fibra a 30nm ottenuta grazie ad un apparato scaffold composto da circa 30 proteine non istoniche. L'interazione con queste proteine porta alla formazione di strutture definite anse della cromatina.
fibra cromatinica DNA nudo = ansa di DNA scaffold cromosomico 30 nm 10 nm DNA nudo
CROMOSOMA
Centromero Cinetocore Proteine non istoniche Microanse
La successiva condensazione della fibra cromatinica, durante la divisione mitotica, dà origine al cromosoma metafasico, caratterizzato da un diametro compreso tra 700 e 1400 nm (circa 1um).
Concetto fondamentale riguardo la cromatina è che in ogni singola cellula che compone l'organismo si ha sempre lo stesso DNA; ciò che varia da tipo cellulare in tipo cellulare è l'espressione dei geni.
La varianza d'espressione è ottenuta grazie al grado d'accessibilità al DNA stesso da parte dell'apparato trascrizionale; rendendo il DNA non accessibile in quanto fortemente condensato non viene permessa la trascrizione di quei determinati geni.
Vi è un'accessibilità differenziale ai geni a seconda del tipo cellulare considerato.
TRASCRIZIONE
Durante l'interfase, è possibile distinguere due diverse cromatine:
- La maggior parte della cromatina, circa il 90%, si trova sotto forma di eucromatina. Essa è la forma aperta, decondensata e potenzialmente attiva dal punto di vista trascrizionale in quanto accessibile al macchinario della trascrizione.
- Il restante 10% della cromatina si trova in forma di eterocromatina, caratterizzata da una maggiore condensazione. Essendo la forma più condensata della cromatina, l'eterocromatina è caratterizzata da un'espressione genica ridotta o totalmente assente in quanto non accessibile all'apparato trascrizionale.Di solito questa forma della cromatina è ancorata all'involucro nucleare o ai nucleoli; è spesso associata ai telomeri e ai centromeri.
La conformazione della cromatina influenza quindi la trascrizione: il DNA che risulta essere attivamente trascritto è organizzato nella fibra di 10 nm o non è totalmente libero dagli istoni.
Con il termine epigenetica si intende lo stato della cromatina; la regolazione epigenetica ha lo scopo di aumentare l'accessibilità di sequenze di DNA, in particolar modo i promotori e geni; questo avviene in quanto l'associazione del DNA con i nucleosomi è transitoria e dinamica.
Il carattere dinamico e transitorio porta a non porter descrivere lo stato epigenetico dell'organismo in quanto differisce da cellula in cellula sia dal punto di vista spazio-istologico che dal punto di vista temporale. Un esempio è la pelle, tessuto eterogeneo caratterizzato da più strati cellulari; le cellule residenti nei vari strati cellulari differiscono le une dalle altre a livello epigenetico, in quanto esprimono geni differenti e in differenti momenti della vita cellulare stessa. L'espressione genica della pelle durante il periodo dello sviluppo è differente rispetto all'espressione genica della pelle adulta, a sua volta differente da quella di una pelle anziana. Anche con il cancro, soprattutto nelle prime fasi, si verifica un cambiamento al livello dell'espressione epigenetica tissutale.
Fattore di trascrizione Enhancer Promotore Gene X RNA polimerasi
La trascrizione del gene è regolata da elementi esterni alla sequenza del gene stesso; tra di essi si riconosce il promotore e gli enhancer. In particolare, quest'ultimi hanno la funzionalità di aumentare o ridurre l'attività trascrizionale del promotore.
Il promotore si trova a circa 5kb a monte del gene, posto in sua prossimità; l'enhancer invece è una sequenza che si trova più distante dall'inizio del gene.
Si distinguono enhancer prossimali, situati a1-5 kb dal gene, e enhancer distali, che possono arrivare fino a 1000 kb di distanza; un tipico enhancer ha una lunghezza di circa 100 bp e si trova a 10-20 kb dal gene. Può verificarsi che l'enhancer faccia parte di un altro cromosoma e che la trascrizione sia permessa solo in seguito a interazioni inter-cromosomiche.
La trascrizione è permessa solo quando la regione dell'enhancer è portata, grazie alla formazione di un loop, a interagire col gene e il proprio promotore. La regolazione della trascrizione avviene quindi al livello tridimensionale.
Per identificare nuove regioni enhancer si usano vari saggi:
Promoter POL Gene Enhancer
- report assay: si usa un sistema modello rappresentante un genoma, il quale è costruito in vitro sfruttando i plasmidi batterici. Tramite clonaggio molecolare è possibile inserire nel vettore la porzione di DNA d'interesse. Di fatto si prende la sequenza enhancer, si amplifica per PCR e si inserisce in un vettore; si useranno poi dei sistemi per verificare se la sequenza in studio è o meno unenhancer, verificando se è avvenuta l'interazione con la regione del promotore. Di solito si usa come indicatore GFP. Questo è un saggio abbastanza vecchio, ideato inizialmente per lo studio dei promotori
- delezione con CRISPR/Cas9: il sistema CRISPR/Cas9 è in grado di lavorare verso siti specifici del genoma. In particolare, permette di stabilire se quella sequenza sia o meno un enhancer studiandone la propria attività espressionale direttamente in situ. Dopo l'azione di editing, tramite qPCR si valuta se l'espressione del gene target sia diminuita o meno; se si verifica una notevole diminuzione del tasso d'espressione molto probabilmente la sequenza sulla quale ha agito CRISPR/Cas9 è un enhancer del gene target.
Si riconoscono diversi meccanismi di regolazione per la trascrizione, i quali agiscono modificando l'accessibilità del DNA stesso.
METILAZIONE DEL DNA
È una modificazione chimica che avviene al livello del DNA stesso, in particolar modo al livello della citosina.
I H H H - N N DNA metilasi A H A CH3 N 5 3 3 2 2 6 1 H N CH3 N 1 I Desossiribosio (gruppo metilico) Desossiribosio 5-metilcitosina (5mC) È un processo catalizzato dalla DNA metilasi, la quale attacca un gruppo metilico in posizione 5 della C; si forma la 5-metilcitosina. Il gruppo metilico è preso dal donatore S- adenosil metionina (SAM). SAM è un intermedio biochimico estremamente importante nel metabolismo; il metabolismo ha influenza Citosina (nel DNA) sull'epigenetica.
La metilazione delle citosine avviene per lo più in zone della cromatina definite isole CpG, in cui dinucleotide citosina-guanina è presente con una frequenza del 20%; nel genoma umano sono presenti circa 25.000 isole CpG, di cui metà si trovano all'interno dei promotori.
La metilazione a livello di isole CpG è associata alla repressione dell'espressione genica ed a uno stato condensato della cromatina.
Nei promotori dei geni housekeeping, ossia tutti quei geni che sono espressi in maniere costitutiva, in tutte le cellule ed in ogni momento, le isole CpG sono ipometilate.
Nei promotori dei geni che hanno un pattern di espressione tessuto-specifica, le isole CpG possono essere ipometilate o metilate, a seconda della necessità cellulare.
Nei promotori dei geni non trascritti del cromosoma X inattivato e nei geni autosomici sottoposti ad imprinting le isole CpG sono metilate.
Si riconoscono diverse ipotesi riguardo i meccanismi con i quali si và a reprimere la trascrizione del DNA metilato.
.O 1 H 6 N 5